相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、实验是科学研究的一种重要手段。下列实验装置能达到实验目的的是

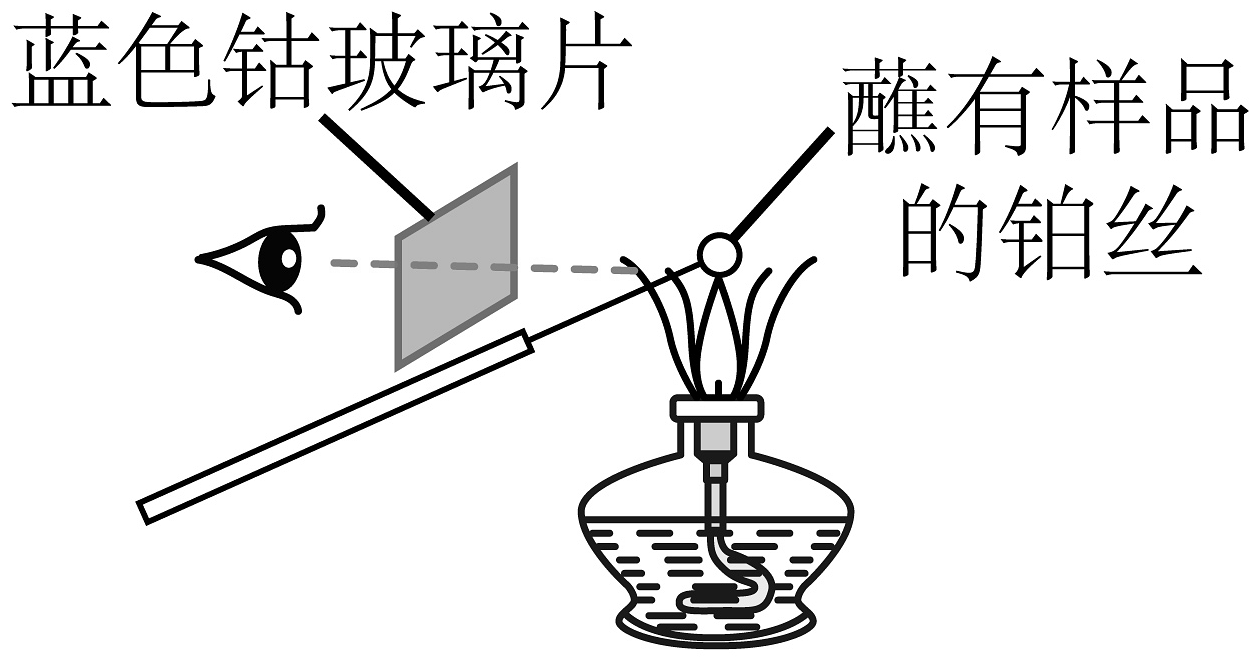
A.Na的燃烧
B.检验化合物中是否含钾元素


C.制备Fe(OH)3胶体
D.验证NaHCO3和Na2CO3的热稳定性
A、A B、B C、C D、D -
2、下列反应的离子方程式书写正确的是A、向NaOH溶液中通入少量CO2:2OH-+CO2=+H2O B、铜片插入AgNO3溶液中: C、Fe与稀硫酸反应: D、碳酸氢钠溶液与少量Ca(OH)2溶液反应:+OH-=+H2O
-
3、部分常见含氯物质的分类与相应化合价关系如图所示。下列推断不合理的是
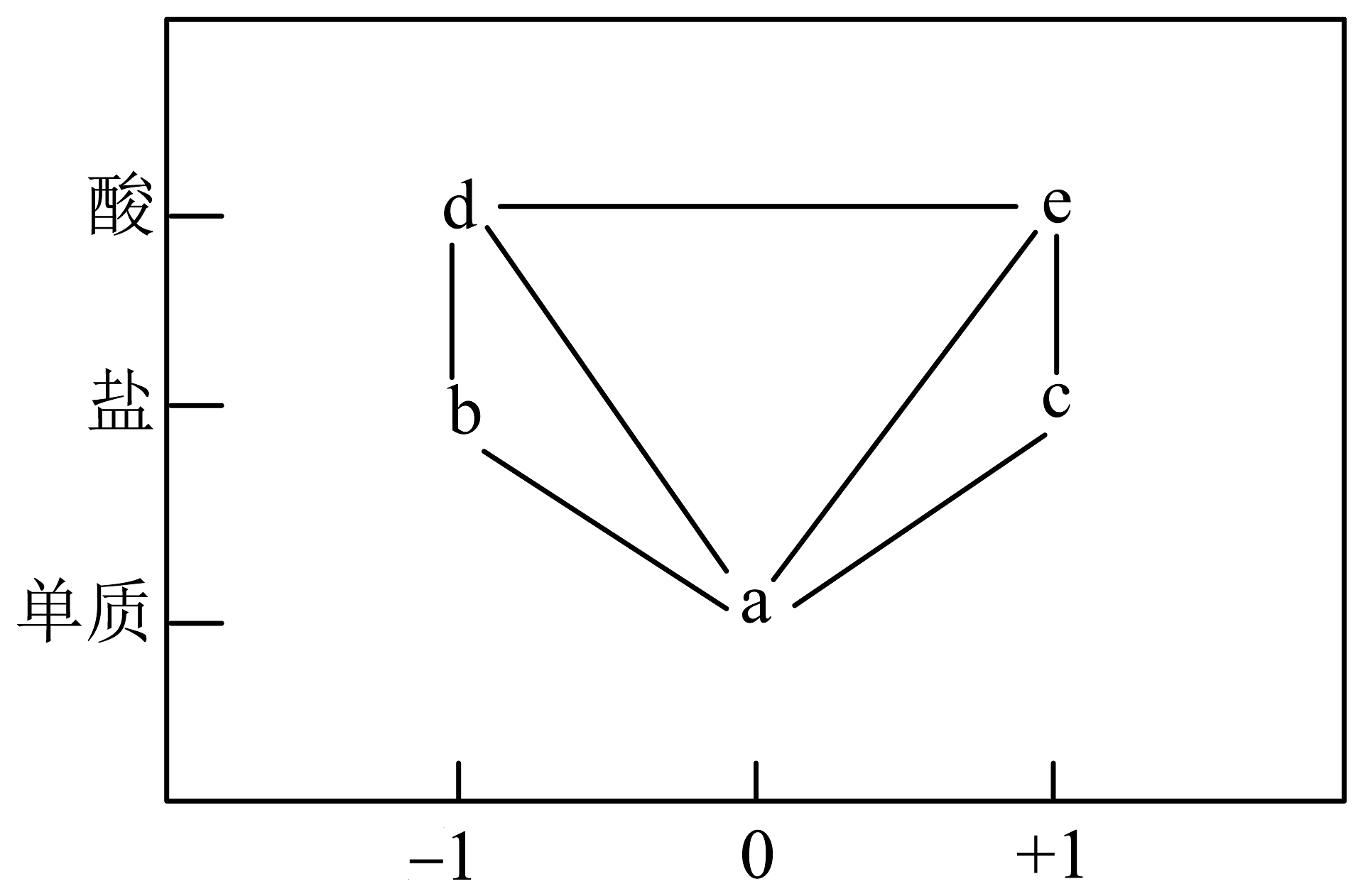 A、a既可被氧化,也可被还原 B、c可能为漂白液或漂白粉有效成分 C、d的浓溶液可与c的固体反应生成b与e D、a与水反应产生d和e
A、a既可被氧化,也可被还原 B、c可能为漂白液或漂白粉有效成分 C、d的浓溶液可与c的固体反应生成b与e D、a与水反应产生d和e -
4、V(钒)能形成多种不同颜色的离子,其转化关系如下图。下列说法不正确的是
 A、V(钒)有+2、+3、+4、+5等多种化合价 B、由图中转化可知,I-比V3+还原性强 C、可加入氧化剂实现VO溶液由黄色转化为蓝色 D、图中每步转化都涉及氧化还原反应
A、V(钒)有+2、+3、+4、+5等多种化合价 B、由图中转化可知,I-比V3+还原性强 C、可加入氧化剂实现VO溶液由黄色转化为蓝色 D、图中每步转化都涉及氧化还原反应 -
5、Fe3+、、Al3+和X四种离子,以物质的量之比2:4:1:1大量共存于同一溶液中,X可能是A、Na+ B、OH- C、Cl- D、
-
6、工业上冶炼锰的反应原理可用化学方程式表示。对于该反应的说法正确的是A、MnO2发生氧化反应 B、Al2O3是还原产物 C、1molMnO2分子被还原时转移4mol电子 D、Al元素得电子
-
7、用NA表示阿伏加德罗常数的值,下列说法正确的是A、11.2LCO2含有的分子数为0.5NA B、1molCO2和NO2的混合物中含的氧原子数为2NA C、1molNa2O2中含有离子的个数为4NA D、Na2O2可用作防毒面具或潜水艇供氧剂,每生成1molO2需转移4mol电子
-
8、下列溶液中能大量共存的离子组是A、使石蕊变红色的溶液中:Fe2+、K+、、 B、酸性澄清透明溶液中:Cu2+、Na+、Cl-、 C、含有大量Ba2+的溶液中:K+、Cl-、、 D、含有大量OH-的溶液中:Na+、、、
-
9、NA表示阿伏加德罗常数的值。下列说法正确的是A、28g氮气所含的氮原子数为 B、5.6gFe与足量的Cl2反应,转移的电子数为 C、标准状况下,22.4L硫酸含有的分子数为 D、17gNH3含有的电子数为
-
10、分类法可用于预测物质性质及其变化规律。下列物质的分类与性质预测对应关系不正确的是
选项
物质
类别
性质预测
A
Na2O
碱性氧化物
能够与酸反应生成盐和水
B
CO
还原剂
能与Fe2O3等氧化剂反应
C
K2CO3
钾盐
能与酸反应
D
HClO
酸
能与NaOH反应生成盐
A、A B、B C、C D、D -
11、下列说法错误的是A、ClO2具有氧化性,可以用于自来水杀菌消毒 B、金属钠着火可用泡沫灭火器灭火 C、新制的氯水能使紫色石蕊试液先变红后褪色 D、过氧化钠可在呼吸面具中作为氧气的来源
-
12、下列物质中能产生丁达尔效应的是A、云、雾 B、酒精溶液 C、Fe(OH)3悬浊液 D、水
-
13、下列实验装置图正确且能达到相应实验目的的是
 A、图甲装置验证铁的析氢腐蚀 B、图乙装置可在待镀铁件表面镀铜 C、图丙用于中和反应反应热的测定 D、图丁是外加电流的阴极保护法防止钢闸门生锈
A、图甲装置验证铁的析氢腐蚀 B、图乙装置可在待镀铁件表面镀铜 C、图丙用于中和反应反应热的测定 D、图丁是外加电流的阴极保护法防止钢闸门生锈 -
14、是一种重要的化工原料,25℃时, , ; , 。(1)、写出CuS在水中的沉淀溶解平衡式:。的水解方程式:。(2)、常温下,NaHS溶液显(填“酸性”“中性”或“碱性”),溶液中含硫微粒的浓度由大到小的顺序为。(3)、常温下,水溶液中和的浓度变化如图所示,下列说法正确的是___________(填标号)。
 A、将硫化氢通入水中,溶液中的变化: B、点溶液中可大量存在的离子: C、将NaHS固体加到水中,水的电离程度减小 D、点时加入少量硫化钠固体,始终不变(4)、常温下,实验室常用硫酸铜溶液除去硫化氢,是一个弱酸制强酸的特例。其反应原理为 , 该反应的平衡常数为(保留3位有效数字)。(5)、硫化物也常用于除去废水中的重金属离子。向含的废水中加入沉淀剂FeS,发生反应的离子方程式为 , 当反应达到平衡时,。
A、将硫化氢通入水中,溶液中的变化: B、点溶液中可大量存在的离子: C、将NaHS固体加到水中,水的电离程度减小 D、点时加入少量硫化钠固体,始终不变(4)、常温下,实验室常用硫酸铜溶液除去硫化氢,是一个弱酸制强酸的特例。其反应原理为 , 该反应的平衡常数为(保留3位有效数字)。(5)、硫化物也常用于除去废水中的重金属离子。向含的废水中加入沉淀剂FeS,发生反应的离子方程式为 , 当反应达到平衡时,。 -
15、废物利用利国利民,回收处理钒铬渣(含有及等),并利用废渣提取钒铬的工艺流程如图:

已知:①25℃时,的溶度积常数为。
②氧化焙烧步骤中分别转化为。
③酸性溶液中,的氧化性强于。
回答下列问题:
(1)、“氧化焙烧”该步骤不能使用陶瓷容器,其原因是 , 其涉及的化学方程式为。(2)、加快“氧化焙烧”的速率,可以采取的措施是。(3)、水浸产生的滤渣1的成分是(用化学式表示)。(4)、“除杂”后,Cr元素主要以存在,结合离子方程式,利用相关原理解释其原因:。(5)、写出“还原”步骤中发生反应的离子方程式:。(6)、在“还原”步骤中,选硫酸酸化而不选盐酸酸化,其原因是。 -
16、已知制备光气的反应为 , 将等物质的量的和充入密闭容器中,平衡体系中,平衡混合物的平均摩尔质量在不同温度下随压强的变化曲线如图所示。下列说法正确的是
 A、温度: B、平衡常数: C、的平衡转化率: D、点时,若 , 则CO的平衡转化率为
A、温度: B、平衡常数: C、的平衡转化率: D、点时,若 , 则CO的平衡转化率为 -
17、下列实验装置及现象正确的是
 A、图甲:浓氨水与浓硫酸反应 B、图乙:测量锌与稀硫酸反应的反应速率 C、图丙:滴定结束时的刻度,读数为12.20mL D、图丁:验证与KI的反应是可逆反应
A、图甲:浓氨水与浓硫酸反应 B、图乙:测量锌与稀硫酸反应的反应速率 C、图丙:滴定结束时的刻度,读数为12.20mL D、图丁:验证与KI的反应是可逆反应 -
18、下列关于实验操作的误差分析不正确的是A、测定中和反应反应热时,如果搅拌器改为铜质的,则测得的偏大 B、用量气法测锌与稀硫酸反应产生的氢气体积时,装置未冷却至室温即读数,则测得的反应速率偏大 C、用洁净的玻璃棒蘸取新制的氯水滴在pH试纸上,来测定氯水的pH D、用标准盐酸滴定未知浓度NaOH溶液,开始滴定时酸式滴定管尖端处有气泡,滴定终点时气泡消失,则测得的NaOH溶液浓度偏大
-
19、设为阿伏加德罗常数的值。下列说法正确的是A、0.1molCu与足量的S完全反应,转移的电子数为 B、的溶液中数等于 C、电解水时,若阴阳两极产生气体的总体积为22.4L,则转移的电子数为 D、氯化铵水溶液中与数之和大于
-
20、尿素在工业、农业、医药等诸多领域应用广泛。(1)、工业上利用合成氨工艺联合生产尿素,原理如图1所示。

①若反应器I和II中各有1molH2O参加反应,理论上可获得molH2。
②反应器IV中主要通过两步完成,其能量变化如图2所示,第一步反应的平衡常数表达式为K= , 总反应2NH3(g)+CO2(g)CO(NH2)2(s)+H2O(g),∆H=kJ·mol−1;反应器IV中还发生尿素水解、尿素缩合生成缩二脲[(NH2CO)2NH]等副反应,其他条件一定时,与尿素产率的关系曲线如图3所示,NH3过量对尿素产率的影响比CO2过量对尿素产率的影响大的原因是。
 (2)、电催化法合成尿素。一种新型异质结构Bi-BiVO4催化剂用于酸性介质中CO2和N2电化学合成尿素。反应过程中,电子能自发从BiVO4端转移到Bi端,在Bi-BiVO4催化剂这一极可能的反应机理如图4所示,反应部分历程及能量关系如图5所示。
(2)、电催化法合成尿素。一种新型异质结构Bi-BiVO4催化剂用于酸性介质中CO2和N2电化学合成尿素。反应过程中,电子能自发从BiVO4端转移到Bi端,在Bi-BiVO4催化剂这一极可能的反应机理如图4所示,反应部分历程及能量关系如图5所示。
①在Bi-BiVO4催化剂这一极发生的电极反应式为。
②反应过程中更倾向于生成交替加氢的中间体,原因是。
③电催化合成尿素成功的关键取决于CO2的还原路径,CO2的可能还原路径如图6所示,CO2在Bi-BiVO4催化剂作用下能还原成*CO的原因是。
