相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、我国古代四大发明之一黑火药的操作反应为: , 设NA为阿伏加德罗常数的值。下列说法正确的是A、每消耗32g S,该反应中转移的电子数目为 B、晶体中含有的离子数目为 C、溶液中含的数目为 D、标准状况下,中含有键的数目为
-
2、一种非天然氨基酸的结构如图所示,关于该化合物,说法不正确的是
 A、能使酸性溶液褪色 B、最多能与等物质的量的Na反应 C、既能与HCl反应又能与NaOH反应 D、分子中碳原子的杂化方式有和
A、能使酸性溶液褪色 B、最多能与等物质的量的Na反应 C、既能与HCl反应又能与NaOH反应 D、分子中碳原子的杂化方式有和 -
3、“光荣属于劳动者,幸福属于劳动者。”下列劳动项目与所述化学知识没有关联的是
选项
劳动项目
化学知识
A
用Na2S除去废水中Hg2+
Na2S具有还原性
B
将模具干燥后再注入熔融钢水
铁与水高温下会反应
C
喷洒波尔多液防治农作物病虫害
Cu2+可使蛋白质变性
D
船舶外壳安装锌块防锈蚀
锌的金属性比铁强
A、A B、B C、C D、D -
4、兴趣小组利用下列装置进行实验,能达到实验目的的是


A.制备NO
B.除去NO中的NO2


C.收集NO
D.吸收尾气中的NO
A、A B、B C、C D、D -
5、从海带灰中提取碘的实验过程如下,其中操作X为
 A、萃取分液 B、加热蒸馏 C、冷却结晶 D、趁热过滤
A、萃取分液 B、加热蒸馏 C、冷却结晶 D、趁热过滤 -
6、“二十四节气”是中国农耕文化的产物,每个节气都有对应的食物。下列说法正确的是A、清明吃艾饼,艾叶中的纤维素属于二糖 B、夏至吃面条,面条中的淀粉属于纯净物 C、立秋吃芝麻,芝麻中的油脂属于芳香烃 D、冬至吃饺子,饺子中的蛋白质可水解为氨基酸
-
7、我国科技发展取得巨大成就。下列说法不正确的是A、蛟龙号载人潜水器使用钛合金作外壳材料,的质子数为22 B、运载火箭使用肼()作燃料,肼的电子式为:
 C、神舟十九号载人飞船使用耐烧蚀树脂,该树脂为合成有机高分子材料
D、天和核心舱电推进系统腔体采用的氮化硼陶瓷属于新型无机非金属材料
C、神舟十九号载人飞船使用耐烧蚀树脂,该树脂为合成有机高分子材料
D、天和核心舱电推进系统腔体采用的氮化硼陶瓷属于新型无机非金属材料
-
8、中华文化源远流长,古人使用不同的材料制作乐器。下列乐器中,主要材质为硅酸盐材料的是




A.青铜编钟
B.木笙
C.陶埙
D.骨笛
A、A B、B C、C D、D -
9、瑞卢戈利(K)是一种小分子促性腺激素释放素受体拮抗剂,其结构如下:
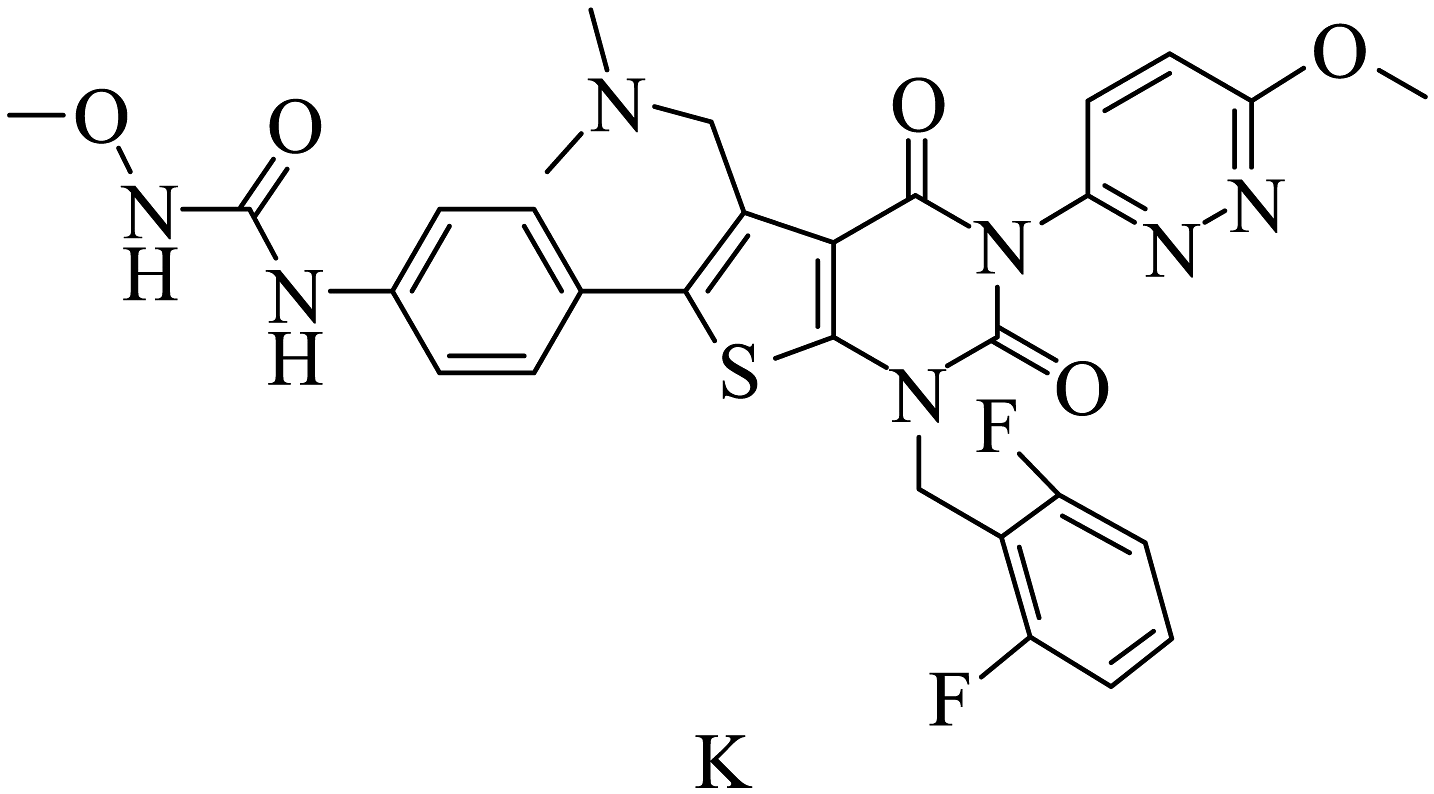
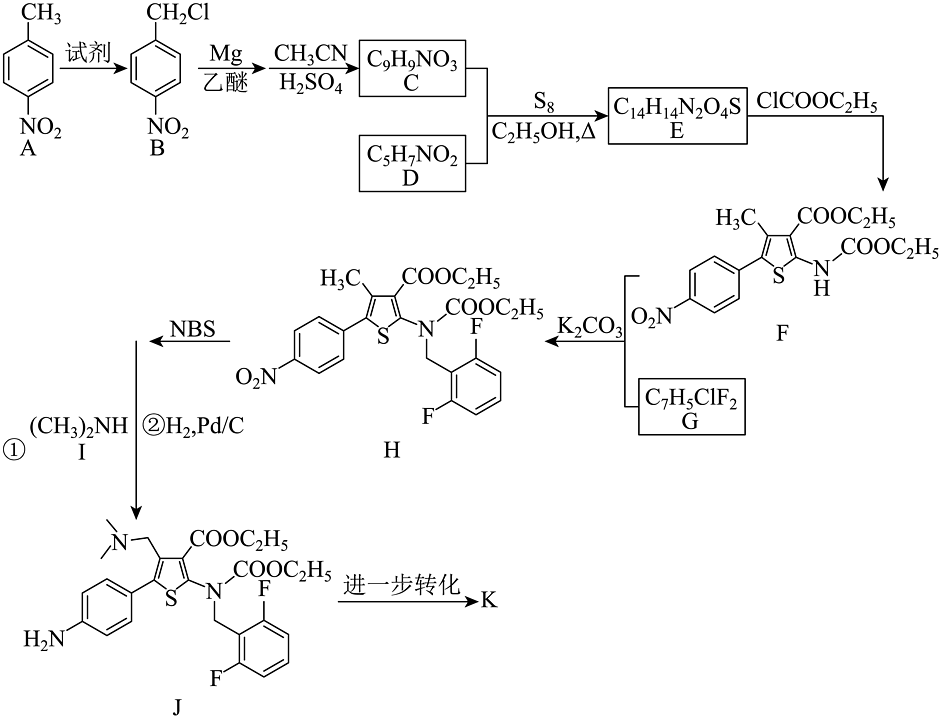
某研究小组按以下路线合成瑞卢戈利(部分反应条件已简化):
已知:①
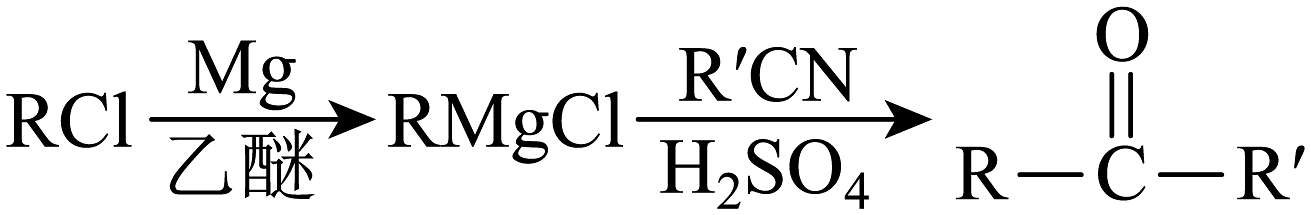
②
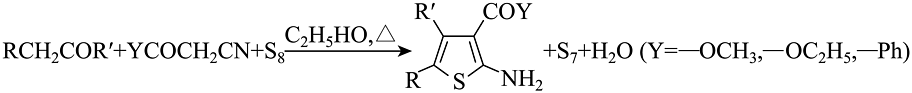
③

请回答:
(1)、化合物F的含氮官能团名称是。(2)、下列说法不正确的是___________。A、的反应中,试剂可用 B、反应过程中只发生取代反应 C、化合物I的碱性弱于 D、瑞卢戈利可在酸性或碱性条件下发生水解反应(3)、化合物G的结构简式是。(4)、的化学方程式是。(5)、写出4种同时符合下列条件的化合物C的同分异构体的结构简式。①谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,无氮氧单键;
②与过量反应生成邻苯二酚(
 )。(已知:
)。(已知: )。(6)、以氯苯、1-氯丁烷和溴乙酸为有机原料,设计化合物
)。(6)、以氯苯、1-氯丁烷和溴乙酸为有机原料,设计化合物 的合成路线(用流程图表示,无机试剂任选)。
的合成路线(用流程图表示,无机试剂任选)。 -
10、酚酞是实验室常用的指示剂,实验室利用邻苯二甲酸酐(结构如图甲所示)和苯酚合成酚酞的装置如图乙所示(省略加热和夹持仪器),操作过程如下:
a.取邻苯二甲酸酐3.0g于三颈烧瓶,再加入苯酚,混合均匀;
b.在搅拌的条件下,加入浓硫酸,加装冷凝管,在150℃下加热回流;
c.待烧杯中固体全部熔化为澄清液体混合物后即可停止加热,并冷却到室温;
d.边搅拌边冷却缓缓加入硫酸,静置,抽滤得到酚酞粗品(橘黄色固体)。
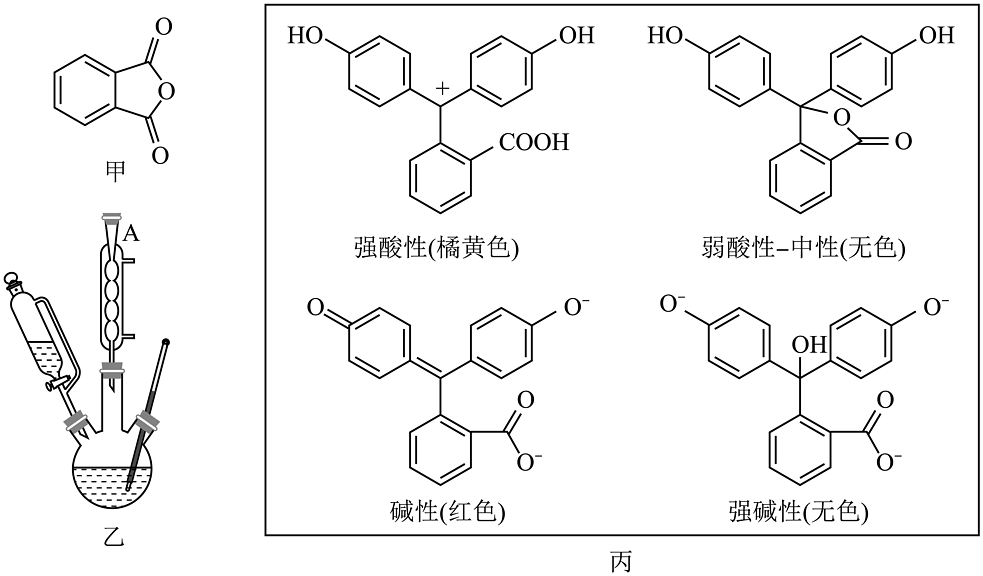
已知:
试剂
熔点/℃
沸点/℃
相关性质
邻苯二甲酸酐
131
284
粉末,遇水容易水解
苯酚
43
182
粉末
在不同酸碱性条件下,酚酞有不同的结构,从而呈现出不同的颜色,如图丙所示。
(1)、为使苯酚与邻苯二甲酸酐更充分地混合,在步骤a前还可以提前进行的操作是。(2)、已知酚酞粗品中硫元素以的形式存在,写出得到酚酞粗品的化学方程式:。(3)、步骤b加热可以采用的方式是;装置中仪器A的名称是;加热时间不宜过长,否则。(4)、可利用酚酞的四种结构之间的转化将获得的酚酞粗品按照如下方法提纯。取酚酞粗品,加入少量水搅拌,然后滴加足量的饱和溶液。一开始,溶液中有气泡产生,随后溶液变红,固体逐渐溶解(酚酞转化为易溶的结构)。补加一些水并继续搅拌一段时间,抽滤(第一次),滤饼用稀溶液洗涤(洗涤液与滤液合并)。将滤液转移到大烧杯中,在不断搅拌下,逐滴加入浓盐酸,直至B______,抽滤(第二次)。继续向滤液中加入浓盐酸,直至没有气泡产生,静置,析出白色的酚酞固体,再次抽滤(第三次)得到产物。a.现象B是。
b.未反应的苯酚主要在第(选填“一”“二”或“三”)次抽滤中除去。
(5)、使用酸碱指示剂时,我们通常只在溶液中添加数滴。结合酚酞的结构和性质,说明其不能多加的原因:。 -
11、
将、转化为其他高利用价值的化合物是目前的研究热点,回答下列问题。
I.的综合利用
(1)利用与的还原反应可以得到 , 该反应一般认为通过以下步骤进行:
则二氧化碳与氢气的还原总反应的热化学方程式为。
反应达到平衡后,降低温度,再次平衡时,的平衡转化率(选填“上升”或“降低”)。
(2)合成总反应的起始比例为 , 在、的条件下达到平衡,且已知平衡时体系中甲醇的物质的量分数为0.15,则的平衡转化率为(保留2位小数)。
(3)利用电化学手段同样可以实现的还原,则碱性电解池中被还原为甲醛的电极反应方程式为。研究发现,对于不同的金属电极,的还原产物不同(如图所示),从右图中可发现铜电极相较于其他金属电极的特点是。
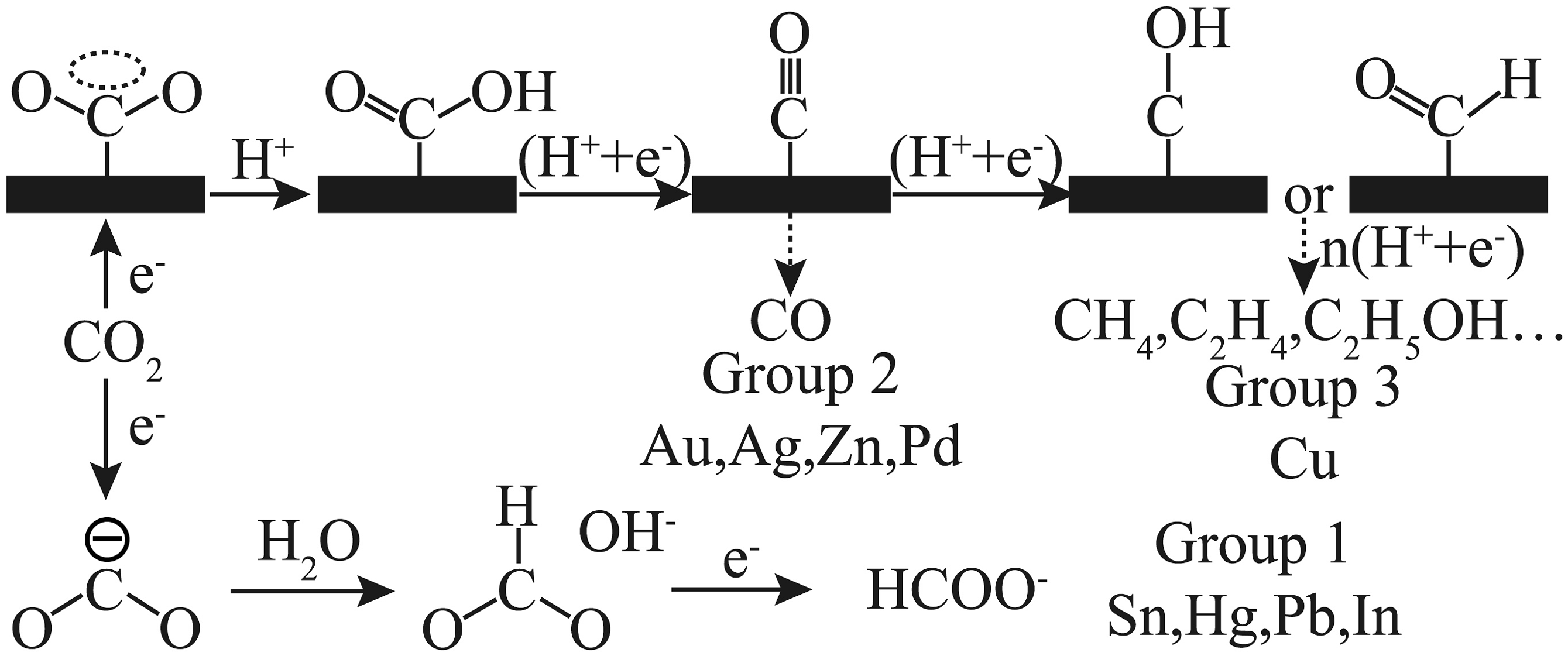
II.的综合利用
利用与反应可制备乙酸,有如下两个催化反应可选,其中使用进行催化的过程如图所示():
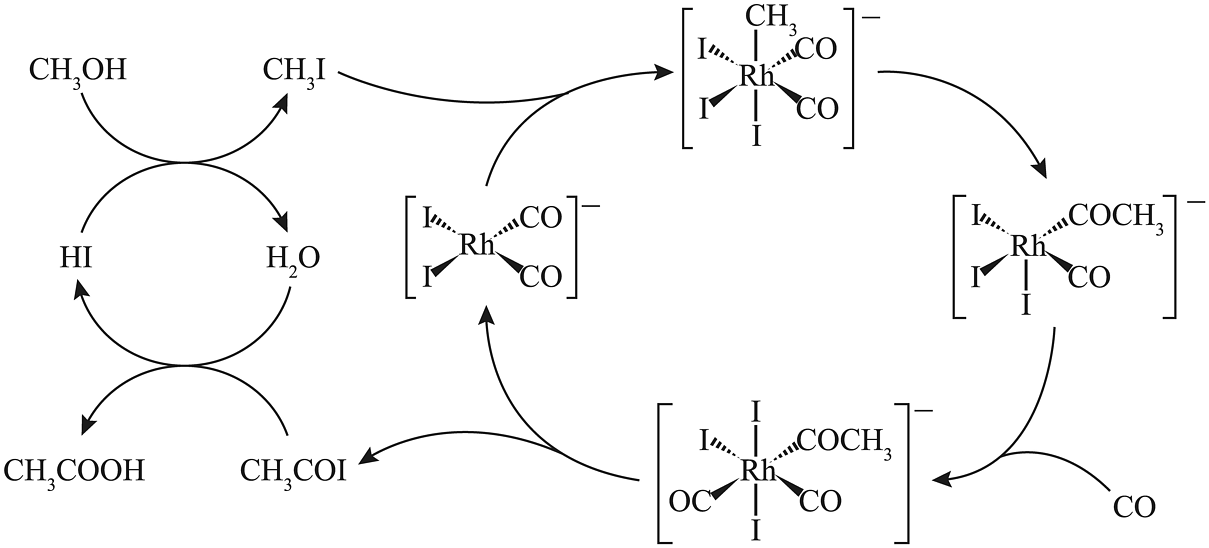
(4)在催化体系中,催化剂为。插入反应得以发生是因为。
(5)在反应物浓度一定时,该反应速率与速率常数成正比。已知该反应的速率常数与温度的关系为 , 其中为反应的活化能,和为常数。对于两种催化剂,其曲线如图所示。试分析哪种催化剂综合催化能力最强,并分析原因。
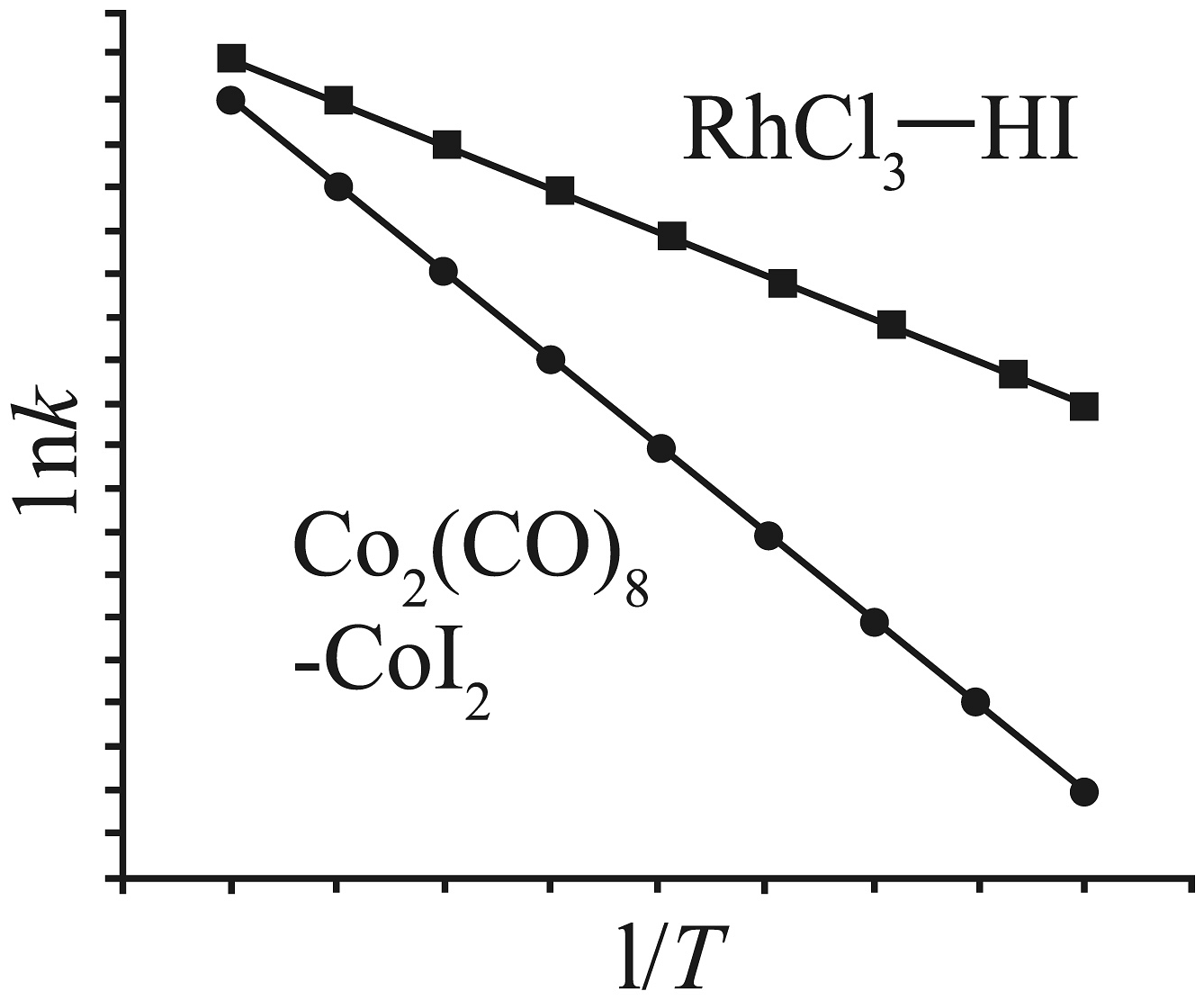
-
12、硫元素作为矿石中的常见元素,一直被人们所喜爱。请回答:(1)、关于VIA族原子结构的认知和描述,下面的说法正确的是___________。A、的最高价氧化物对应水化物的酸性弱于的 B、的基态电子排布为 C、VIA族元素的电负性从上到下逐渐减小 D、的氧化性比更强,因为在周期表中比更靠下(2)、小同学从实验室中取出一瓶硫化钠溶液,但是他发现,溶液呈橙黄色而非通常的无色。他经过实验,发现溶液可以表示为氢氧化钠和一种表观化学式为的化合物已知化合物中含有一负二价阴离子。
a.画出阴离子的结构:。
b.根据信息,写出将少量通入过量硫化钠溶液后能看到的现象:。
(3)、群青的化学式是 , 已知除了硫以外的其余元素都以最常见价态存在,从微粒结构的角度解释为何群青呈现蓝色:。(4)、已知相对分子质量越大,一般而言熔沸点越高,然而三氧化硫的熔点却高于七氧化二氯,请从分子结构的角度解释其原因:。(5)、在1793年,勒布朗提出了一种制碱的方案,在当时被称为勒布朗法。该方法流程如下: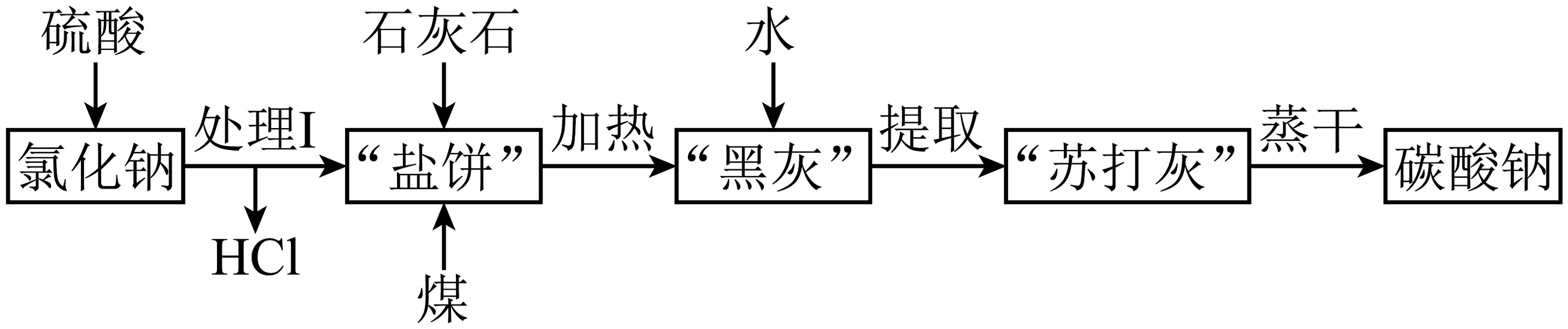
根据勒布朗法,回答:
a.“处理I”中,我们需要把混合物用低热蒸干,然后将熔融物置于明火中,请说明为何这样能够得到相对较纯的“盐饼”:。
b.在“提取”中,我们需要把“加热”得到的“黑灰”及时丢入水中,指出如果不及时丢入水中会导致的后果:。
c.“加热”中,使用的煤如果含氮量较高,会出现的问题是。写出“加热”过程的化学方程式:。
-
13、在我国青海、西藏等地有许多干涸盐湖盛产含钠盐的。是一种易溶于水的白色固体,其水溶液用硫酸酸化可得到【其分子结构可描述为】。纯净的为无色小片状透明晶体。将与甲醇、浓硫酸混合点燃,可以产生独特的绿色火焰。已知此反应的原理为:在浓硫酸的催化下与甲醇反应生成硼酸三甲酯;发生燃烧,生成的水和逸出体系,而生成的留在反应体系中。结合上述材料和所学知识,判断下列说法正确的是
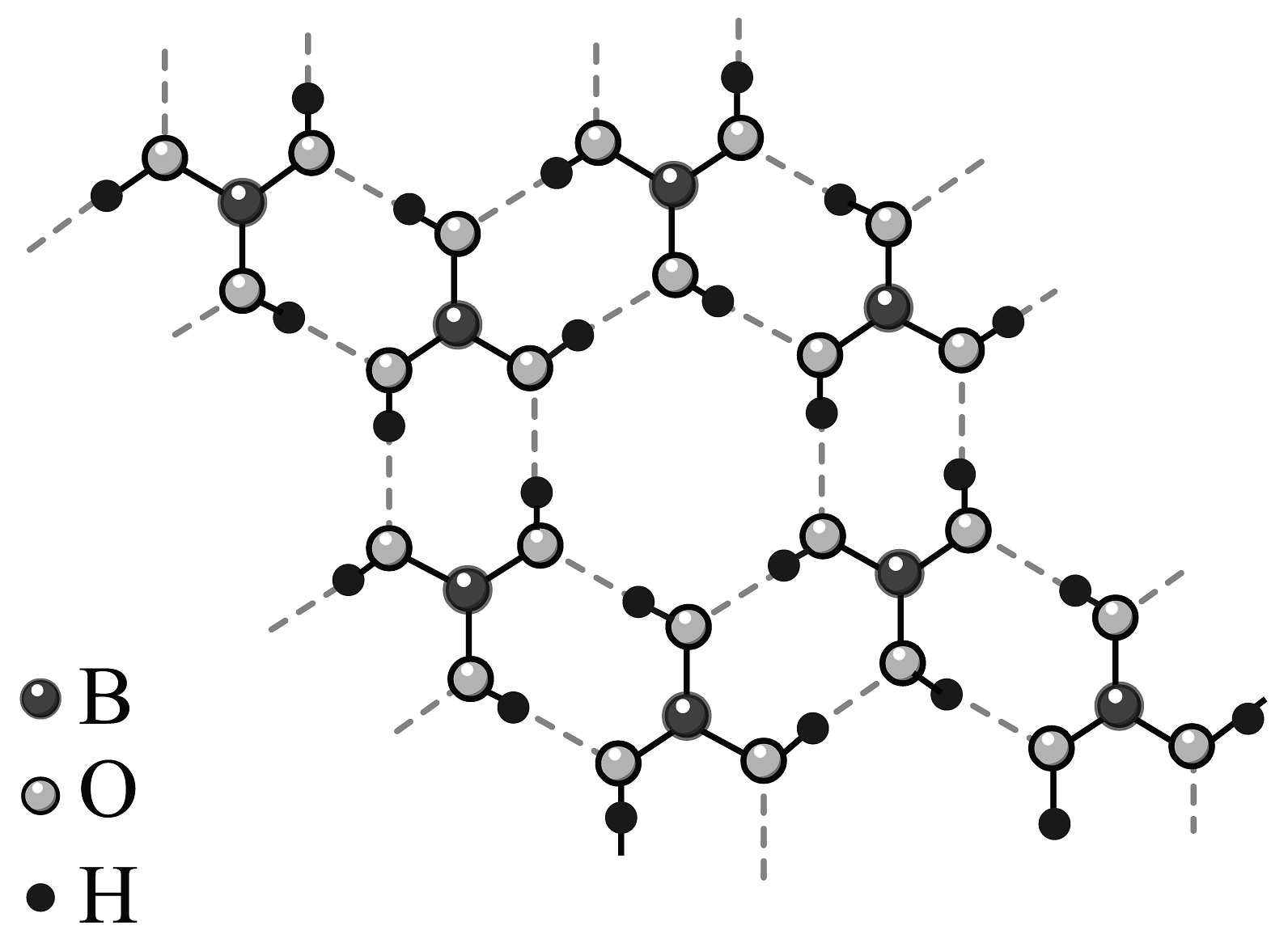 A、已知溶于浓可得到和少量 , 则中很可能含有和少量 B、已知的最常见晶体中有类似石墨的层状结构,且每层按如图所示的方式通过氢键形成无限网状结构,则其晶体类型为混合晶体 C、已知原亚硝酸三甲酯中的原子采取杂化,则硼酸三甲酯中亦采取杂化 D、题中所描述的燃烧反应进行一段时间后,火焰逐渐熄灭,如要使反应继续进行,需要添加甲醇并重新点燃
A、已知溶于浓可得到和少量 , 则中很可能含有和少量 B、已知的最常见晶体中有类似石墨的层状结构,且每层按如图所示的方式通过氢键形成无限网状结构,则其晶体类型为混合晶体 C、已知原亚硝酸三甲酯中的原子采取杂化,则硼酸三甲酯中亦采取杂化 D、题中所描述的燃烧反应进行一段时间后,火焰逐渐熄灭,如要使反应继续进行,需要添加甲醇并重新点燃 -
14、现有含和的混合溶液,已知 , , , , 则下列说法不正确的是A、向其中加入溶液,无沉淀生成 B、向其中加入溶液,有沉淀生成 C、向其中加入溶液,无沉淀生成 D、向其中加入溶液,有沉淀生成
-
15、连二亚硫酸钠与反应得到三氟甲磺酸钠。有文献报道其机理如下所示:
(i)
(ii)
(iii)
下列说法错误的是
A、根据VSEPR理论,的构型为折线型 B、反应体系中可能可以检测到的生成 C、的水解能力强于 D、反应ii的类型为取代反应 -
16、12000年前,地球上发生过一次大的灾变,气温骤降,导致猛犸灭绝,北美Clovis文化消亡。有一种假说认为,灾变缘起一颗碳质彗星撞击地球。2010年,几个研究小组发现,在北美和格陵兰该地质年代的地层中存在超乎寻常浓度的纳米六方金刚石,这被认为是该假说的证据。立方和六方金刚石的晶胞结构分别如下左图和下右图所示。近似认为两种晶胞中碳碳键键长相等且均为 , 每一个碳原子周围的四个碳原子均排布为正四面体。则下列说法正确的是
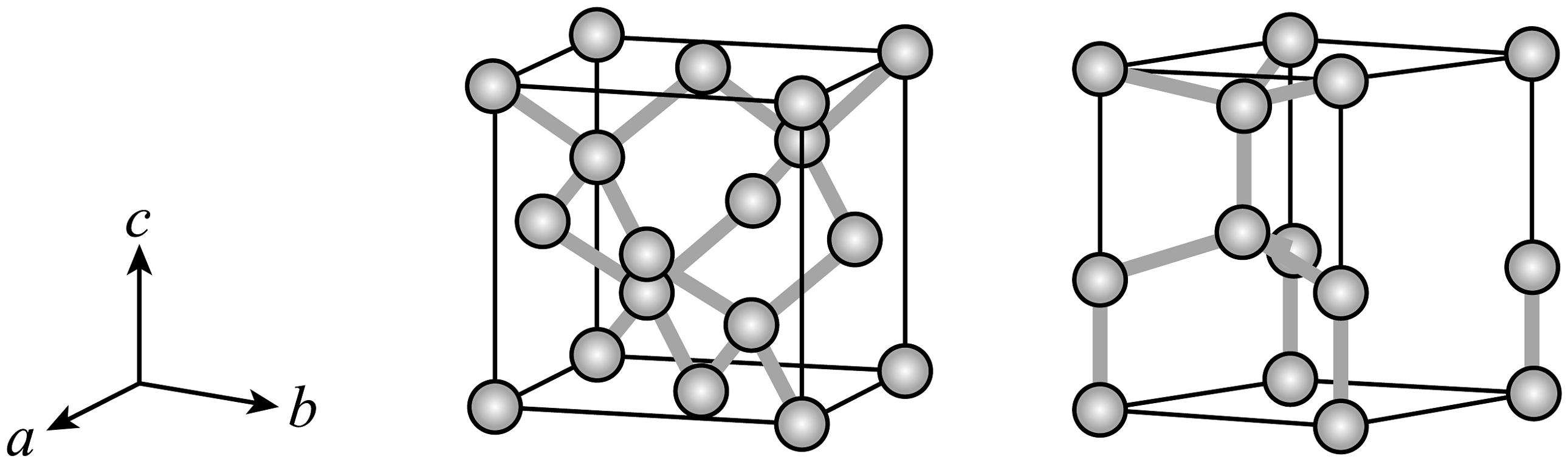 A、立方金刚石的晶胞参数 B、六方金刚石的晶胞参数 C、六方金刚石的晶胞参数 D、六方金刚石的密度比立方金刚石更大
A、立方金刚石的晶胞参数 B、六方金刚石的晶胞参数 C、六方金刚石的晶胞参数 D、六方金刚石的密度比立方金刚石更大 -
17、快速阅读下列材料,判断说法错误的一项是
Nature Chemistry在2025年发表的新型水系锌-碘电池研究引发关注。该电池正极采用的碳纳米管复合电极具备特殊的表面电荷分布,能对不同离子产生差异化的静电作用,进而精准调控离子在电极表面的吸附与反应活性。电池以含的水溶液为电解质溶液,充放电过程涉及、与之间复杂的转化,锌电极发生的溶解与沉积。放电时总反应为 , 正极存在副反应(未配平),且副反应程度与电极-电解液界面的电场强度、离子浓度梯度密切相关。碳纳米管复合电极对离子的吸附符合Langmuir吸附等温式: , 其中是吸附量,是饱和吸附量,为吸附平衡常数,为离子浓度。
A、放电时,正极发生的副反应的电极方程为: B、放电时,不论和消耗的速率之比如何变化,电路中每转移电子,负极减小的质量总是 C、若用铅酸蓄电池给该电池充电,电极应当与碳纳米管复合电极相接 D、碳纳米管复合电极对的吸附程度随着浓度的增大而线性增大 -
18、纳米碗是一种奇特的碗状共轭体系。高温条件下,可以由分子经过连续5步氢抽提和闭环脱氢反应生成。其中第一步反应的反应机理和能量变化如下。下列说法错误的是
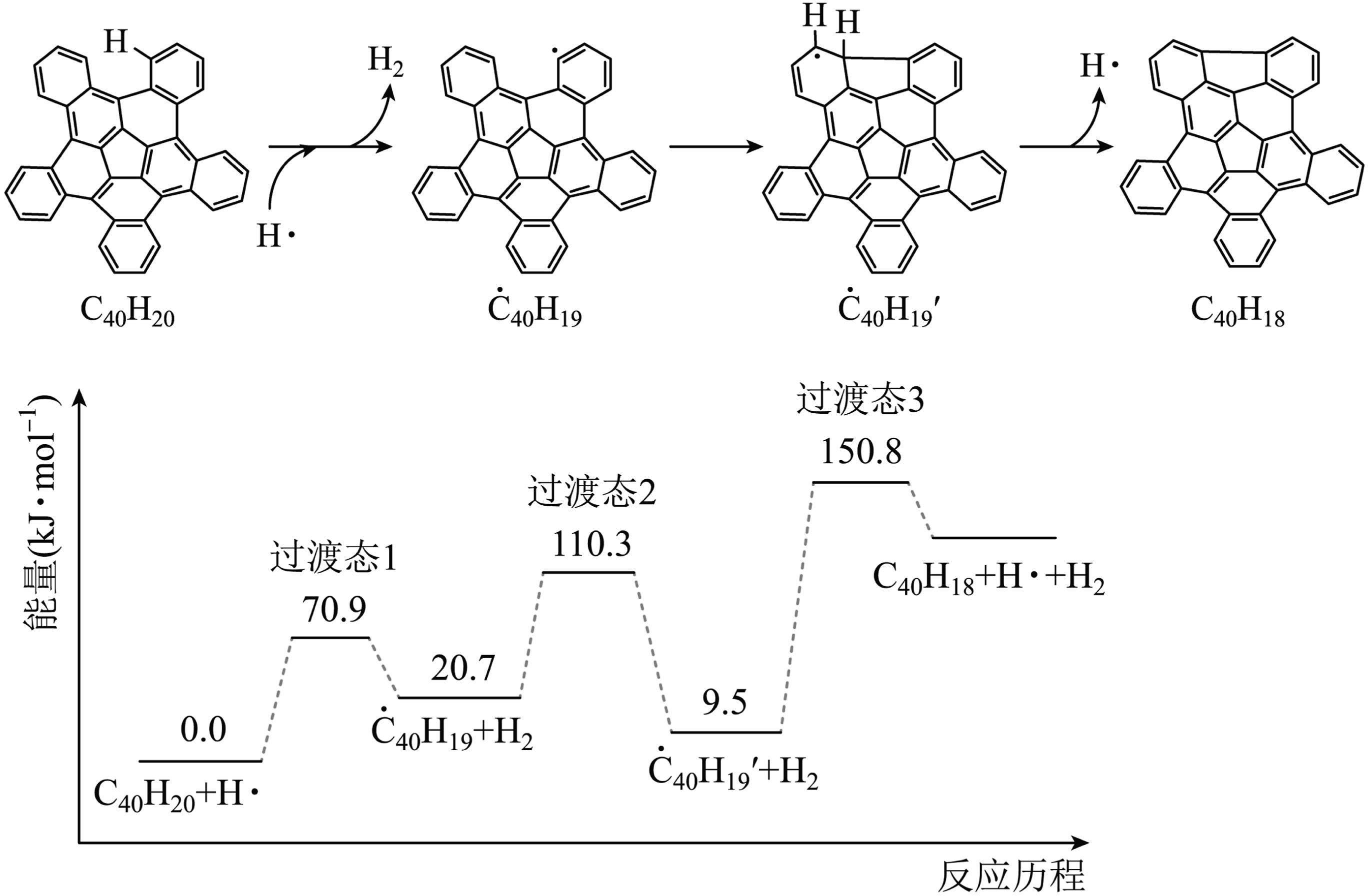 A、该反应共有3个基元反应,其中决速步反应为第三步 B、纳米碗中五元环结构的数目为5 C、反应过程中生成了具有手性异构的中间产物 D、生成的五步反应,每步反应的焓变近似相等
A、该反应共有3个基元反应,其中决速步反应为第三步 B、纳米碗中五元环结构的数目为5 C、反应过程中生成了具有手性异构的中间产物 D、生成的五步反应,每步反应的焓变近似相等 -
19、用如图所示的分馏装置使用乙酰乙酸乙酯( , A)制取脱氢醋酸(
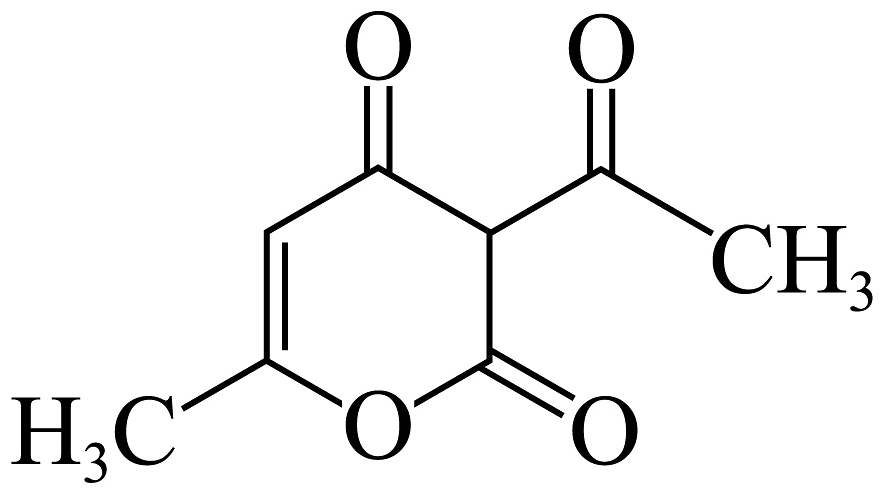 , B)时,发生可逆反应。
, B)时,发生可逆反应。已知的沸点为181℃,的沸点为270℃。以下说法错误的是
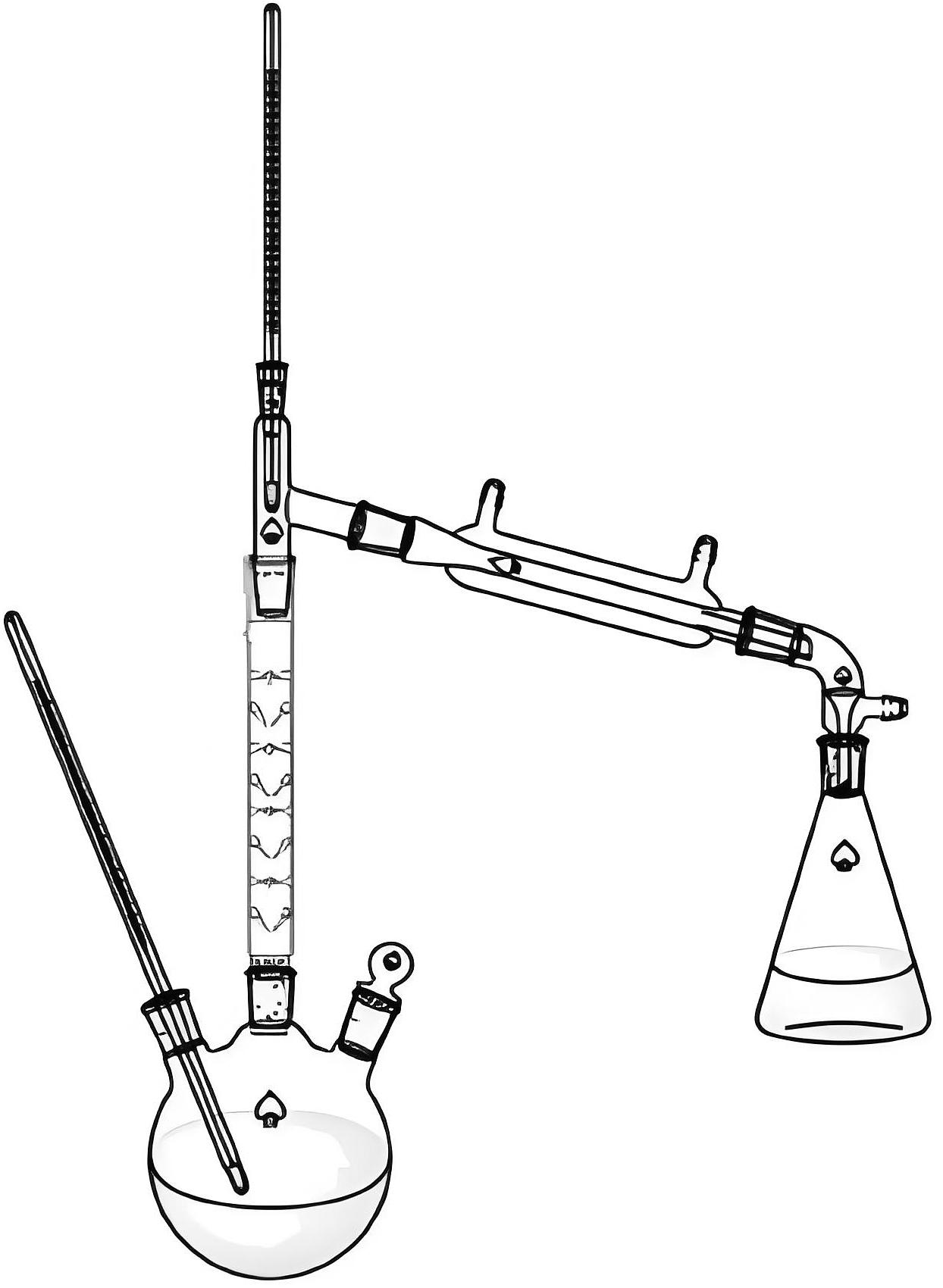 A、刺形分馏柱上缠绕棉绳的目的是减少热量散失 B、为确保实验安全,宜选用量程更大的水银温度计来代替酒精温度计 C、反应过程中除去乙醇有利于提高产率 D、可选用水作为脱氢醋酸重结晶的溶剂
A、刺形分馏柱上缠绕棉绳的目的是减少热量散失 B、为确保实验安全,宜选用量程更大的水银温度计来代替酒精温度计 C、反应过程中除去乙醇有利于提高产率 D、可选用水作为脱氢醋酸重结晶的溶剂 -
20、科学家曾在-100℃的低温下合成了如图所示的化合物 , 下列关于的说法错误的是
 A、分子的化学式为 B、分子中所有原子均共平面 C、分子中有1种化学环境的原子和2种化学环境的原子 D、温度升高时迅速分解,这可能与其键角较小而导致的不稳定性有关
A、分子的化学式为 B、分子中所有原子均共平面 C、分子中有1种化学环境的原子和2种化学环境的原子 D、温度升高时迅速分解,这可能与其键角较小而导致的不稳定性有关