相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、自然界中臭氧形成反应的能量变化如图所示。下列说法中正确的是( )
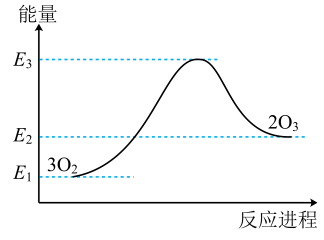 A、根据能量图可以判断为放热反应 B、臭氧比氧气稳定 C、O2的能量低于O3的能量 D、断开中的化学键吸收的能量大于形成中的化学键释放的能量
A、根据能量图可以判断为放热反应 B、臭氧比氧气稳定 C、O2的能量低于O3的能量 D、断开中的化学键吸收的能量大于形成中的化学键释放的能量 -
2、下列实验装置设计正确,且能达到实验目的的是( )
选项
A
B
C
D
实验目的
制取氨气
收集
制取
除去乙烯中混有的少量的
实验装置

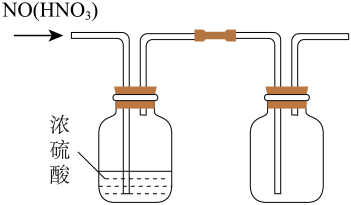
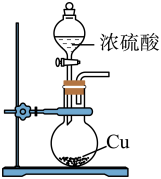
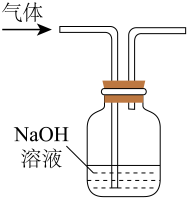 A、A B、B C、C D、D
A、A B、B C、C D、D -
3、草莽酸是合成治疗禽流感的药物达菲的原料之一,下列关于它的叙述正确的是( )
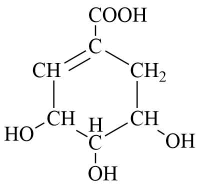 A、养莽酸和足量钠反应生成(标准状况) B、含有三种含氧官能团 C、能发生加成反应,取代反应和氧化反应 D、有机物中所有碳原子处于同一平面
A、养莽酸和足量钠反应生成(标准状况) B、含有三种含氧官能团 C、能发生加成反应,取代反应和氧化反应 D、有机物中所有碳原子处于同一平面 -
4、设为阿伏加德罗常数的值,下列叙述正确的是( )A、常温常压下,乙醇分子中含有的共价键数目为 B、环状(
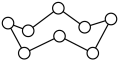 )分子中含有的键数目为
C、浓硫酸与足量铜加热反应,生成的分子数目为
D、光照条件下,将与充入一密闭容器内充分反应后,容器内气体的分子数目为
)分子中含有的键数目为
C、浓硫酸与足量铜加热反应,生成的分子数目为
D、光照条件下,将与充入一密闭容器内充分反应后,容器内气体的分子数目为
-
5、下列反应的离子方程式书写正确的是( )A、铜片与稀反应生成气体: B、溶液中加入稀硫酸: C、大理石溶于醋酸中: D、硫化亚铁溶于稀硝酸中:
-
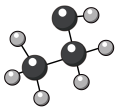
6、下列示意图与化学用语表述内容不相符的是( )
A
B
C
D
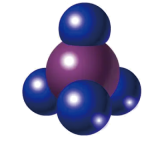

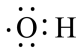
分子的空间填充模型
乙醇的球棍模型
聚异戊二烯的结构简式
羟基的电子式
A、A B、B C、C D、D -
7、我国践行科技兴国的发展战略,近年来收获了丰硕的科技成果。下列说法正确的是( )A、“北斗系统”组网成功,北斗芯片中的半导体材料为二氧化硅 B、“神舟”十六号飞船航天员穿的航天服使用了多种合成纤维 C、“祝融号”火星车利用正十一烷储能,正十一烷属于有机高分子化合物 D、“鲲龙”水陆两栖飞机实现海上直飞,其所用燃料航空煤油是纯净物
-
8、为常见的主族元素,根据下表信息回答问题。
元素
元素性质/原子结构信息
A
短周期元素原子半径最大(稀有气体不参与比较)
B
+3价阳离子的核外电子排布与氖原子相同
C
原子核外电子层与电子层的电子数相等
D
与同周期,化合价有等
E
原子结构示意图:
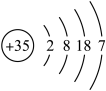 (1)、写出元素的原子结构示意图。(2)、A、B最高价氧化物对应水化物的碱性强弱:(填化学式)。(3)、用电子式表示和D形成化合物的过程:。(4)、元素在周期表中的位置 , 关于元素及其化合物的推断中,正确的是。
(1)、写出元素的原子结构示意图。(2)、A、B最高价氧化物对应水化物的碱性强弱:(填化学式)。(3)、用电子式表示和D形成化合物的过程:。(4)、元素在周期表中的位置 , 关于元素及其化合物的推断中,正确的是。a.与的最低负化合价相同
b.的单质可与和形成的化合物的水溶液发生置换反应
c.最高价氧化物对应水化物的酸性:
d.氢化物稳定性:
(5)、D和E形成的化合物①具有氧化性,其中体现氧化性的元素是(写元素符号) , 原因是。(6)、元素与同主族,比多2个电子层,与氧以比例形成的化合物②的物质类别为 , 任意写出一个能体现②的类别通性的反应方程式。(7)、第四周期ⅥA族的元素硒是一种人体必需的元素,关于硒元素及其化合物的有关说法正确的是(选填序号)a.硒原子的半径比硫原子的大 b.的稳定性比的强
c.能与溶液反应 d.可以使酸性高锰酸钾溶液褪色
-
9、利用催化技术可将汽车尾气中的和转化为和 , 化学方程式是:(1)、某温度下,在容积不变的密闭容器中通入和 , 测得不同时间的浓度如下表:
时间
0
1
2
3
……
3.60
3.05
2.85
2.76
……
用的浓度变化表示的平均反应速率为。
(2)、反应物初始浓度相同时,实验温度为和 , 进行以下实验:实验编号
实验目的
同种催化剂的比表面积
一段时间内的平均速率/
Ⅰ
对照实验
280
80
Ⅱ
研究催化剂比表面积对尾气转化速率的影响
a
120
Ⅲ
b
c
d
【实验分析与结论】
①补全表格a. , b. , c. , d.。
②测得 , 对比实验Ⅰ、Ⅱ,可得结论:。
③通过实验可得到“催化剂的比表面积相同时,温度升高,可增大尾气的转化速率”的结论,证据是。
-
10、甲酸被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
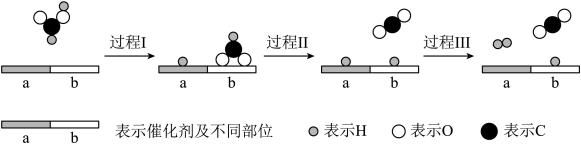 (1)、中官能团的名称是。(2)、常压下甲酸的沸点是。甲酸沸腾的过程中,外界提供的能量的作用是。(3)、过程Ⅰ中断裂的化学键是 , 过程Ⅲ中形成的化学键是。(4)、分解制氢的总反应方程式是 , 两种产物的电子式分别是、。(5)、分解制氢是一个可逆反应。在密闭容器中,通入蒸汽,一段时间后,核素存在于以下分子中:。
(1)、中官能团的名称是。(2)、常压下甲酸的沸点是。甲酸沸腾的过程中,外界提供的能量的作用是。(3)、过程Ⅰ中断裂的化学键是 , 过程Ⅲ中形成的化学键是。(4)、分解制氢的总反应方程式是 , 两种产物的电子式分别是、。(5)、分解制氢是一个可逆反应。在密闭容器中,通入蒸汽,一段时间后,核素存在于以下分子中:。 -
11、溴被称为“海洋元素”,以下是一种从苦卤浓缩液中提取溴的流程示意图:
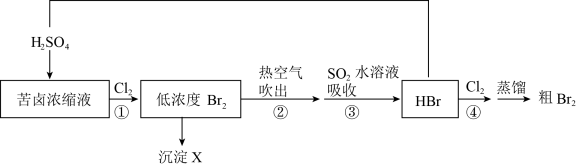
资料:常用提溴原料含溴量
提溴原料
天然海水
苦卤浓缩液
溴含量
0.045
7.270
(1)、选用苦卤浓缩液而不是天然海水作为提溴原料的原因是。(2)、海水中溴元素的存在形式是 , 写出①的离子方程式 , 该反应中两种单质的氧化性关系为 , 从原子结构角度解释原因:。(3)、③中发生反应的离子方程式是。(4)、低浓度经过操作②、③、④后得到的是。(5)、“蒸馏”操作利用的是物质哪种性质的差异性:。 -
12、某研究小组探究原电池的原理并进行实验。(1)、下列反应中,可通过原电池装置实现化学能直接转化为电能的是(选填序号)。
① ②
③ ④
(2)、甲同学用导线将电流表与片、片相连接,插入盛有稀硫酸的烧杯中进行实验Ⅰ,如图1所示。
①能证明化学能转化为电能的实验现象是:电流表指针偏转、。
②从构成原电池的基本要素来看,的作用是(选填序号,下同) , 稀硫酸的作用是。
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
(3)、乙同学想利用反应设计一个原电池,请在图2上标明所使用的用品。 (4)、氢氧燃料电池是一种新型发电装置(如图3所示),下列叙述不正确的是。
(4)、氢氧燃料电池是一种新型发电装置(如图3所示),下列叙述不正确的是。a.通氢气的一极是正极,发生氧化反应
b.电子由电极经溶液流向电极
c.总反应为

-
13、有机化学是以有机化合物为研究对象的学科,它的研究范围包括有机物的来源、结构、性质、合成和应用等。(1)、Ⅰ.下图是一些烃的球棍模型,回答以下问题:
上述模型①-④中,不正确的是(填序号) , 原因是(从原子结构角度予以说明)。 (2)、⑤的结构简式是。(3)、Ⅱ.餐厨垃圾在酶的作用下可获得乙醇,进一步反应可制备有机物C和高分子材料G,转化关系如下:
(2)、⑤的结构简式是。(3)、Ⅱ.餐厨垃圾在酶的作用下可获得乙醇,进一步反应可制备有机物C和高分子材料G,转化关系如下:
乙醇中含有的官能团名称是。(4)、反应ⅰ、ⅱ的化学方程式分别是、;反应类型分别是、。(5)、G的结构简式是。(6)、下列说法中,不正确的是(选填字母)。a.E、F均属于烃
b.的分子式为
c.反应ⅲ为取代反应 -
14、将形状和大小相同的条分别打磨后,与相同体积的盐酸和盐酸完全反应,放出气体的体积随时间的变化如图所示。下列说法中正确的是( )
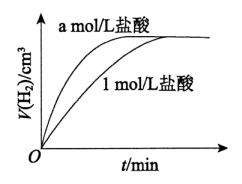 A、反应的离子方程式是: B、可推断: C、可推断:反应中镁过量 D、若用硫酸代替上述实验中盐酸,反应速率不变
A、反应的离子方程式是: B、可推断: C、可推断:反应中镁过量 D、若用硫酸代替上述实验中盐酸,反应速率不变 -
15、利用废铝箔(主要成分为 , 含少量等)制明矾的一种工艺流程如下:

资料:
下列说法中,不正确的是( )
A、①体现了铝能与碱溶液反应的性质 B、乙溶液中含有的离子有 C、由④可推测,室温下明矾的溶解度小于和的溶解度 D、均具有两性 -
16、酸性条件下,用进行脱硫处理的原理如下图所示。下列说法中,不正确的是( )
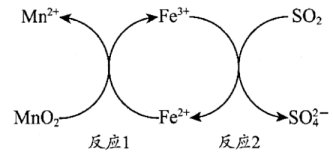 A、反应1中做氧化剂 B、反应1的产物有 C、反应2中做还原剂 D、反应2中做反应物
A、反应1中做氧化剂 B、反应1的产物有 C、反应2中做还原剂 D、反应2中做反应物 -
17、辛烷完全燃烧的反应是。用表示阿伏加德罗常数,下列说法中正确的是( )A、中含有碳氢键和碳碳单键 B、中含有氢氢键 C、参加反应,转移的电子数目为 D、常温常压下,中所含分子数为
-
18、下列事实不能用元素周期律解释的是( )A、酸性: B、氢化物稳定性: C、金属性: D、热稳定性:
-
19、下列说法中不正确的是( )A、淀粉遇碘单质变蓝 B、葡萄糖能水解 C、油脂属于酯类 D、糖类、油脂、蛋白质均含有元素
-
20、光气在农药、医药等领域都有许多用途。一定温度下,恒容密闭容器中,与在催化剂的作用下发生反应:。下列说法中能说明该反应已经达到化学平衡状态的是( )A、消耗的同时消耗 B、的浓度相等 C、的浓度不再变化 D、在密闭容器中共存