相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、利用下列实验装置进行实验,能达到实验目的的是( )
 A、用装置①验证乙醇消去反应生成乙烯 B、用装置②制备少量乙酸乙酯 C、用装置③验证石蜡分解产生不饱和烃 D、用装畳④鉴别邻二甲苯与环己烯
A、用装置①验证乙醇消去反应生成乙烯 B、用装置②制备少量乙酸乙酯 C、用装置③验证石蜡分解产生不饱和烃 D、用装畳④鉴别邻二甲苯与环己烯 -
2、某学者绘制了一种八角星元素周期表,每个八角星代表一个周期(第1周期除外),八角星的每个顶角对应一种元素。为原子序数依次增大的五种短周期主族元素,基态原子核外电子占据3个能级且成对电子数是末成对电子数的3倍。下列说法错洖的是( )
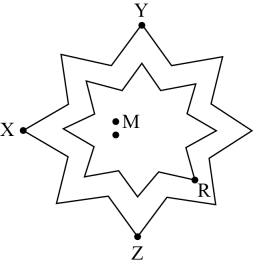 A、三种元素形成的化合物一定是离子化合物 B、分别与形成的最简单化合物的沸点: C、最高价氧化物的水化物之间均能两两反应 D、形成的两种常见化合物阴阳离子个数比均为
A、三种元素形成的化合物一定是离子化合物 B、分别与形成的最简单化合物的沸点: C、最高价氧化物的水化物之间均能两两反应 D、形成的两种常见化合物阴阳离子个数比均为 -
3、下列关于烃及其衍生物的说法正确的是( )A、甲烷、苯、葡萄糖均不能使酸性高锰酸钾溶液褪色 B、与组成上相差1个 , 一定互为同系物 C、石油的裂化、石油的分馏与煤的干馏均属于化学变化 D、乙醇是优良的有机溶剂,可用于提取某些中药的有效成分
-
4、蔡斯盐是最早发现的配合物,将乙烯气体通入溶液中,在氮化亚锡催化作用下即可制得。下列说法错误的是( )A、电负性: B、的电子式为
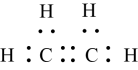 C、与互为同位素
D、蔡斯盐中化合价为+2
C、与互为同位素
D、蔡斯盐中化合价为+2
-
5、党的二十大报告对“传承中华优秀传统文化”提出了明确要求。中华优秀传统文化中蕴藏着诸多化学知识,下列诗句相关说法错误的是( )A、“采桑作蚕丝”中的蚕丝属于蛋白质,可通过灼烧鉴别真伪 B、“杨花榆荚无才思”中的榆荚又称榆钱,主要有机成分是纤维素 C、“蜂蜜酿成花已飞”中的蜂蜜含有果糖和葡萄糖,二者互为同分异构体 D、“蜡炬成灰泪始干”中的蜡主要成分为高级脂肪酸酯,属于高分子化合物
-
6、以钛铁矿(主要成分 , 钛酸亚铁)为主要原料制备绿矾和二氧化钛的生产工艺如下图。已知:。

回答下列问题:
(1)、中的化合价为 , 加硫酸时将钛铁矿粉碎的目的是。(2)、若在实验室中进行操作①,所使用的玻璃仪器有烧杯、、。(3)、检验绿矾中的方法为。(4)、流程中可循环利用的物质是。 -
7、氨基甲酸铵(NH2COONH4)是一种重要的医用氨化剂,有关该物质的信息如下表所示:
制备原理
放热反应
主要性质
①在潮湿的空气中转变为
②温度较高时容易分解生成、
③不溶于
某实验小组在实验室中利用下列装置合成少量的氨基甲酸铵。回答下列问题:
 (1)、盛放稀盐酸的仪器的名称是。(2)、装置B和C中试剂的名称分别是、。(3)、实验室制取氨气的化学方程式为。(4)、反应结束后,从三颈烧瓶中分离出产品,进行的实验操作是。(5)、装置E的作用有(写出两点)。若观察到E中出现大量气泡(浓硫酸足量),则可能的原因是。(6)、设计实验:检验制得的产品中是否混有?。
(1)、盛放稀盐酸的仪器的名称是。(2)、装置B和C中试剂的名称分别是、。(3)、实验室制取氨气的化学方程式为。(4)、反应结束后,从三颈烧瓶中分离出产品,进行的实验操作是。(5)、装置E的作用有(写出两点)。若观察到E中出现大量气泡(浓硫酸足量),则可能的原因是。(6)、设计实验:检验制得的产品中是否混有?。 -
8、聚丙烯酸乙酯可作为皮革的防裂剂和涂料的基液,其一种合成路线图如下,其中A的产量用来衡量一个国家石油化工发展水平。回答下列问题:
 (1)、A的结构简式为 , 与丙烯互为(填“同分异构体”、“同素异形体”或“同系物”)。(2)、丙烯酸中所含官能团的名称是。(3)、反应①~④中属于“原子经济性反应”(即原子利用率为100%)的是(填序号)。(4)、反应②的化学方程式为:。(5)、B与丙烯酸反应生成丙烯酸乙酯的化学方程式为: , 反应类型属于。(6)、写出一种与丙烯酸乙酯互为同分异构体的有机酸的结构简式:。
(1)、A的结构简式为 , 与丙烯互为(填“同分异构体”、“同素异形体”或“同系物”)。(2)、丙烯酸中所含官能团的名称是。(3)、反应①~④中属于“原子经济性反应”(即原子利用率为100%)的是(填序号)。(4)、反应②的化学方程式为:。(5)、B与丙烯酸反应生成丙烯酸乙酯的化学方程式为: , 反应类型属于。(6)、写出一种与丙烯酸乙酯互为同分异构体的有机酸的结构简式:。 -
9、2023年全国政府工作报告指出,推动重点领域节能降碳减污。一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。(1)、已知与的燃烧热分别为、 , , 写出与反应生成和的热化学方程式。(2)、一定温度下,在恒容密闭容器中与反应生成和。
①能说明该反应达到平衡状态的是(填字母)。
A.
B.容器内压强一定
C.气体平均相对分子质量一定D.气体密度一定
E.的体积分数一定②保持温度不变,再向容器中通入 , 则v(正)v(逆)(填“>”“<”或“=”)。
(3)、丙烷燃烧可以通过以下两种途径:途径I:
途径Ⅱ:
(a、b、c、d均为正值)
请回答下列问题:
判断等量的丙烷通过两种途径放出的热量,途径I放出的热量(填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。的反应中,反应物具有的总能量(填“大于”、“等于”或“小于”)生成物具有的总能量。b与a、c、d的数学关系式是。
-
10、硅锰电池是一种新型电池,因其供电稳定,存储量丰富而备受关注。硅锰电池的工作原理如图所示。下列说法正确的是( )
 A、电池工作时,通过质子交换膜由电极区移向电极区 B、放电时,导线上每通过电子,正极区溶液的质量增加 C、电池充电时,电极的电极反应式是 D、电池充电时,电极连接外接电源的正极
A、电池工作时,通过质子交换膜由电极区移向电极区 B、放电时,导线上每通过电子,正极区溶液的质量增加 C、电池充电时,电极的电极反应式是 D、电池充电时,电极连接外接电源的正极 -
11、一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。下列说法正确的是( )
 A、t1min时该化学反应达到平衡状态 B、在4min时v正>v逆 C、4min内,CO2的转化率约为71.4% D、4min内,CO的平均反应速率v(CO)=0.25mol•L-1•min-1
A、t1min时该化学反应达到平衡状态 B、在4min时v正>v逆 C、4min内,CO2的转化率约为71.4% D、4min内,CO的平均反应速率v(CO)=0.25mol•L-1•min-1 -
12、铝土矿(主要成分为 , 还含有、)是工业上制备金属铝的主要原料,工业上提取铝的工艺流程如下:

对于上述工艺流程,下列说法不正确的是( )
A、沉淀A中有 B、试剂a可以用氨水,目的是使三价铁离子完全转化为除去 C、步骤③发生的离子反应方程式是(过量) D、工业上用电解熔融的方法制备金属铝,铝是阴极产物 -
13、短周期主族元素X、Y、Z、W的原子序数依次增大。X的单质在空气中所占体积分数最大,Y是地壳中含量最多的金属元素,Z与X位于同一主族,W原子的最外层有7个电子。下列说法正确的是( )A、的最高价氧化物属于碱性氧化物 B、原子半径: C、简单气态氢化物的热稳定性: D、的含氧酸的酸性比的强
-
14、设为阿伏加德罗常数的值,下列有关说法正确的是( )A、常温常压下,含有分子的数目为 B、的溶液含有的数目为 C、与在密闭容器中充分反应,生成HI分子的数目为 D、和足量铁粉反应,转移电子的数目为
-
15、下列物质的转化能一步完成的是( )A、 B、 C、 D、
-
16、在海水资源的开发利用中,下列关于各工业体系的操作的叙述中错误的是( )
选项
工业体系
操作
A
镁工业:制备单质镁
高温条件下,用氢气还原氧化镁
B
溴工业:制备单质溴
用氯气氧化海水中的溴离子
C
淡水工业:制备蒸馏水
用太阳能将海水蒸发再液化得到初步的淡水
D
氯碱工业:制备含氯消毒剂
用得到的和石灰乳反应制漂白粉
A、A B、B C、C D、D -
17、相同条件下,下列各热化学方程式中ΔH最小的是( )
①2A(l)+B(l)=2C(g) ΔH1 ②2A(g)+B(g)=2C(g) ΔH2
③2A(g)+B(g)=2C(l) ΔH3 ④2A(l)+B(l)=2C(l) ΔH4
A、ΔH1 B、ΔH2 C、ΔH3 D、ΔH4 -
18、工业上用焦炭还原石英砂可以制粗硅(含碳化硅),再进一步制备高纯度硅。下列说法正确的是( )A、制粗硅的化学方程式为: B、晶体硅的导电性介于导体和绝缘体之间,常用作光导纤维 C、石英砂的成分是 , 可用作太阳能电池 D、碳化硅具有类似金刚石的结构,可用作耐高温材料
-
19、下列有关糖类、油脂、蛋白质的说法正确的是( )A、蛋白质由C、H、O三种元素组成 B、利用淀粉水解一步反应得到乙醇 C、油脂属于高分子化合物 D、可用灼烧法来鉴别蚕丝和棉织物
-
20、下列化学用语表示正确的是( )A、甲烷的结构式:CH4 B、HCl的电子式:
 C、Cl-的结构示意图:
C、Cl-的结构示意图: D、硫酸钾的电离方程式:K2SO4=2K++
D、硫酸钾的电离方程式:K2SO4=2K++