相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列工业生产中采用的措施与目的相符合的是( )A、高炉炼铁时通过加入过量铁矿石提高化学反应速率 B、硫酸工业中用热交换器,以维持反应条件、节约能源 C、合成氨中循环利用、 , 以提高产率、降低成本 D、海带提碘时通过浓缩提高 , 以减少氧化剂的用量
-
2、下列各组材料组成如图装置,能形成原电池且M做正极的是( )
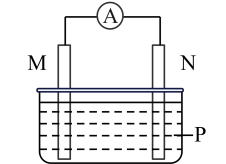
选项
M
N
P
A
稀硫酸
B
蔗糖溶液
C
溶液
D
溶液
A、A B、B C、C D、D -
3、食品添加剂是指为改善食品品质和色、香、味以及防腐、保鲜和加工工艺的需要而加入食品中的人工合成或天然物质。下列食品添加剂中,其使用目的与反应速率有关的是( )A、抗氧化剂 B、调味剂 C、着色剂 D、营养强化剂
-
4、下列有关酸雨的说法中不正确的是( )A、硫酸型酸雨形成的主要原因是生活生产中含硫燃料的大量燃烧 B、汽车尾气中的主要源自于汽油中的含氮物质 C、用天然气代替含硫的煤作燃料,可有效控制酸雨的形成 D、酸雨能直接破坏农作物、腐蚀建筑物及工业设备
-
5、用表示阿伏加德罗常数的值,下列说法中正确的是( )A、0.01mol中含有的质子数为 B、4.48L与的混合物所含分子数为 C、3.2g与的混合物中所含氧原子数为 D、标准状况下,22.4L和的混合气体中含碳原子数为
-
6、工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:①;②。该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需。其主要原因是( )A、过量 B、与铁矿石接触不充分 C、炼铁高炉的高度不够 D、上述反应有一定的限度
-
7、生产、生活中处处有化学。下列说法正确的是( )A、草木灰与硫酸铵混用可提高肥效 B、喝牛奶可缓解重金属盐中毒的毒性 C、石油分馏时获取的馏分均为纯净物 D、用来做燃料的煤和天然气是可再生能源
-
8、中国古代文献和诗句中涉及许多化学知识。下列说法错误的是( )A、《天工开物》记载“矿灰形者,取入缸中,浸三个时,漉入釜中”包含过滤操作 B、《梦溪笔谈》记载“方家以磁石磨针,则能指南”,磁石的主要成分是 C、“爆竹声中一岁除,春风送暖入屠苏”中爆竹爆炸发生的反应为氧化还原反应 D、“青蒿一握,以水二升渍,绞取法”,屠呦呦对青蒿素的提取属于物理变化
-
9、从科技前沿到日常生活,化学无处不在。下列说法错误的是( )A、在三星堆“祭祀坑”提取到丝绸制品残留物,其中丝绸主要成分为蛋白质 B、2022年北京冬奥会吉祥物“冰墩墩”使用的聚乙烯属于有机高分子材料 C、“天和”核心舱中使用陶瓷基复合材料中的氮化硼属于硅酸盐材料 D、“空气捕捉”法能实现从空气中捕获二氧化碳,利于碳中和
-
10、利用浊度计探究一定条件下反应物浓度对硫代硫酸钠()溶液与硫酸溶液反应速率的影响。浊度计用于测量浑浊度的变化,产生的沉淀越多,浑浊度(单位为NTU)值越大。
反应原理:
用图1所示装置进行如下表所示的5个实验,分别测量混合后溶液达到浑浊度为375NTU的过程中,浑浊度随时间变化情况。实验①~⑤所得数据如图2曲线①~⑤所示。
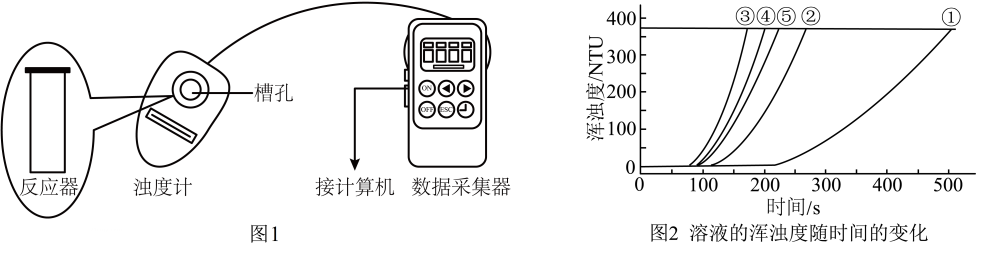
实验编号
溶液
溶液
蒸馏水
V/mL
V/mL
V/mL
①
0.1
1.5
0.1
V1
10
②
0.1
2.5
0.1
V2
9
③
0.1
3.5
0.1
3.5
8
④
0.1
V3
0.1
2.5
9
⑤
0.1
V4
0.1
1.5
10
(1)、。(2)、实验①③的目的是。(3)、分析数据可得以下三个结论:结论1:其它条件相同时,浓度越大,反应速率越大;
①结论2:;
②结论3:其它条件相同时,浓度改变对反应速率的影响程度大于浓度改变对反应速率的影响程度。证据是。
(4)、已知浑浊度为375NTU时,产生S的质量为g,则实验①反应开始到500s,用浓度变化表示的平均反应速率为。 -
11、已知氨气可与灼热的氧化铜反应得到氮气和金属铜,小组同学称取a g氧化铜,用下图装置(省略夹持装置)进行实验。
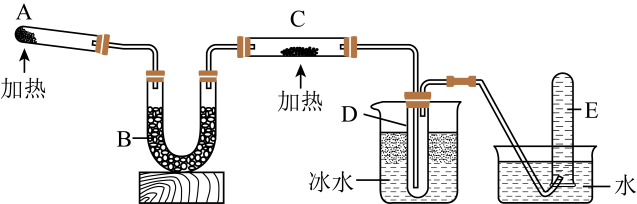 (1)、装置A中发生反应的化学方程式为。(2)、装置B中的试剂为(填标号)。
(1)、装置A中发生反应的化学方程式为。(2)、装置B中的试剂为(填标号)。①浓硫酸 ②无水氯化钙 ③碱石灰 ④五氧化二磷
(3)、装置D中收集到的物质是。(4)、装置C中观察到的现象为 , 发生反应的氧化剂和还原剂的物质的量之比为。(5)、同学查阅资料,发现氧化亚铜()也是红色固体,并提出猜想:装置C中的固体产物可能是Cu和的混合物。①氨气还原氧化铜生成氧化亚铜的化学方程式为。
②装置C中充分反应后,冷却,称量C中固体的质量为b g。当<b<(用含a的式子表示),证明C中固体是Cu和的混合物。
-
12、丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料。一种合成方法如下:
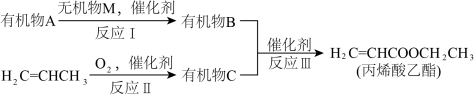
已知:有机物A是一种植物生长调节剂。
(1)、有机物A的电子式为。(2)、丙烯酸乙酯中含有的官能团名称为。(3)、有机物C的结构简式为。(4)、反应Ⅰ的化学方程式为。(5)、反应Ⅰ、Ⅱ、Ⅲ中,原子利用率为100%的是。(6)、46 g有机物B与36 g有机物C在一定条件下发生反应Ⅲ,如果实际产率是72%,则可得到丙烯酸乙酯的质量为g。(7)、某实验小组用以下装置制备丙烯酸乙酯:
①球形干燥管c除起冷凝作用外,它的另一重要作用是。
②待收集到一定量产物后停止加热,取下试管b并振荡、静置,可观察到(填实验现象)。
③分离试管b中的液体混合物,采用的方法为。
-
13、研究化学反应的原理,对掌握物质的应用有重要的意义。(1)、Ⅰ.硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

工业上用为原料制备粗硅。①反应的化学方程式为。
②的用途是(任写一种)。
(2)、反应Ⅲ生成2 mol Si(s)时,(填“吸收”或“放出”)热量。(3)、在2L密闭容器中投入过量Si(s)和3 mol HCl(g)发生反应Ⅰ,经过t min反应达到平衡状态,测得容器中HCl的平衡浓度为0.6 mol·L。①反应开始到t min,用HCl浓度变化表示的平均反应速率为mol⋅L⋅min。
②为加快反应速率,可采取的措施为(任写一种)。
③下列叙述不能说明反应Ⅰ一定达到平衡状态的是(填标号)。
a. b.硅的质量保持不变
c.HCl的质量分数保持不变 d.保持不变
(4)、Ⅱ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。
电极X为(填“正极”、“负极”)。(5)、电池工作时,质子通过交换膜(填“从左到右”、“从右到左”)迁移(6)、正极的电极反应式为。 -
14、人类从自然界中获取各种化学物质。(1)、Ⅰ.从化石燃料可以获得多种有机物。
苯的分子式为。(2)、聚丙烯的结构简式为。(3)、下列物质中,与正丁烷互为同系物的是(填标号)。A.甲烷 B.乙烯 C.环己烷 D.异丁烷
(4)、Ⅱ.从矿石中可以获取多种材料。
常用的金属冶炼方法有:热分解法、高温还原法和电解法。铝的冶炼属于法。(5)、碳素钢是一种铁碳合金,碳素钢的硬度(填“大于”、“小于”)纯铁。(6)、下列材料中,属于有机高分子材料的是(填标号)A.玻璃 B.陶瓷 C.塑料 D.橡胶
(7)、Ⅲ.硫元素的化合价与其形成的物质类别关系如图所示。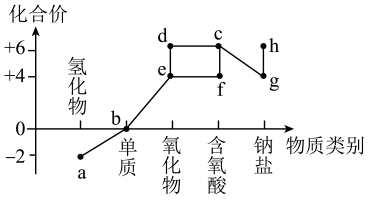
e的浓溶液使蔗糖炭化时,e的浓溶液主要表现性质。(8)、c气体使鲜花褪色时,c气体表现性质。(9)、g的固体与70%的e的浓溶液反应制备c气体时,发生(填“氧化还原反应”或“非氧化还原反应”)。(10)、工业上用过量氨水吸收c气体,反应的离子方程式为。 -
15、铝土矿的主要成分是 , 还有部分、以及少量不溶于酸碱溶液的其他杂质。工业上从铝土矿中提取铝可采取如下工艺:
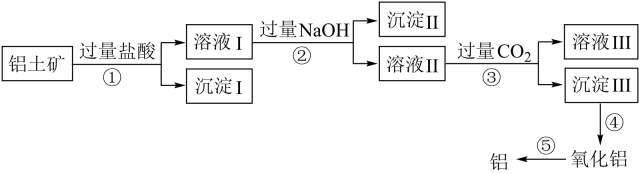
下列说法正确的是( )
A、沉淀Ⅰ只有 B、步骤②发生的反应为、 C、溶液Ⅲ中溶质主要为 D、步骤④操作用到的仪器主要有:坩埚、坩埚钳、泥三角、三脚架、酒精灯、玻璃棒 -
16、由和制备(熔点16.8℃,沸点44.8℃)的模拟装置如下图所示(加热和夹持装置省略),下列说法错误的是( )
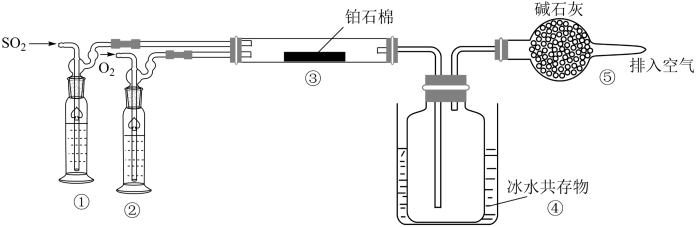 A、装置③中铂石棉用作反应的催化剂 B、装置①②的作用是干燥气体,并通过观察气泡监测气体流速 C、从装置⑤逸出的气体有和 D、装置④的作用是冷凝收集
A、装置③中铂石棉用作反应的催化剂 B、装置①②的作用是干燥气体,并通过观察气泡监测气体流速 C、从装置⑤逸出的气体有和 D、装置④的作用是冷凝收集 -
17、下列实验装置能达到实验目的的是( )A、制备并收集
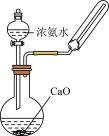 B、制备
B、制备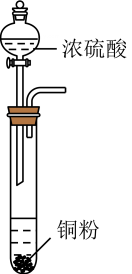 C、除去中的HCl
C、除去中的HCl D、制备并收集
D、制备并收集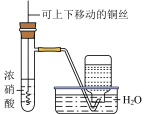
-
18、结构简式如下的有机物具有玫瑰香气,下列说法错误的是( )
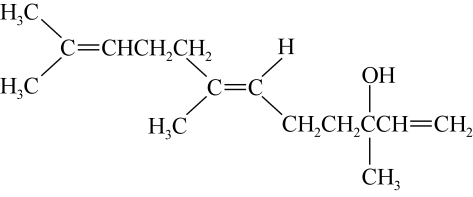 A、该有机物的分子式为 B、1mol该有机物在氧气中充分燃烧需消耗481.6 L(标准状况)氧气 C、该有机物既能发生取代反应,又能发生加成反应 D、该有机物既能跟溴的四氯化碳溶液反应,又能跟金属钠反应
A、该有机物的分子式为 B、1mol该有机物在氧气中充分燃烧需消耗481.6 L(标准状况)氧气 C、该有机物既能发生取代反应,又能发生加成反应 D、该有机物既能跟溴的四氯化碳溶液反应,又能跟金属钠反应 -
19、为阿伏加德罗常数的值,下列说法正确的是( )A、6.4 g铜粉与过量硫粉反应,铜失去的电子数目为 B、1 mol Fe溶于过量稀硝酸,转移电子数为 C、标准状况下,2.24 L乙炔中含有的共用电子对数目为 D、标准状况下,4.48 L 中含有的分子数目为
-
20、如图为铜锌原电池示意图,下列说法正确的是( )
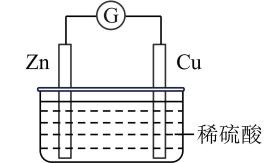 A、电池工作时,电能转化为化学能 B、锌片作负极,发生还原反应 C、铜电极的电极反应式为 D、电子从铜电极经导线流向锌电极
A、电池工作时,电能转化为化学能 B、锌片作负极,发生还原反应 C、铜电极的电极反应式为 D、电子从铜电极经导线流向锌电极