相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、沙子的主要成分是 , 属于酸性氧化物,部分性质与、类似。下列关于性质的预测正确的是( )A、能与水反应生成硅酸 B、属于酸性氧化物,不与任何酸反应 C、能与氢氧化钠溶液反应生成和 D、是良好的半导体材料
-
2、下列实验装置能达到实验目的的是( )
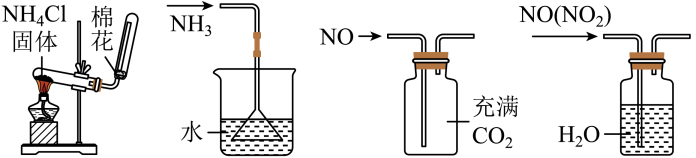 A、制备氨气 B、防止倒吸 C、收集气体 D、除去中的
A、制备氨气 B、防止倒吸 C、收集气体 D、除去中的 -
3、北京大学和中国科学院的化学工作者已成功研制出碱金属与形成的球碳盐 , 实验测知该物质在熔融状态下能导电,具有良好的超导性。下列有关分析不正确的是( )A、中含有离子键 B、中含有非极性共价键 C、该晶体熔化过程中破坏了离子键 D、与互为同位素
-
4、浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是( )A、吸水性 B、脱水性 C、酸性 D、强氧化性
-
5、如图是某食品包装袋,下列说法不正确的是( )
配料:猪肉、鸡肉、水、淀粉、蛋液、白砂糖、植物蛋白、食用盐。食品添加剂:增稠剂、水分保持剂、食用香精、增味剂、山梨酸钾、红曲红、亚硝酸钠、猪骨提取物。
A、谷氨酸钠是增味剂的一种 B、山梨酸钾是一种营养强化剂 C、红曲红是一种着色剂 D、亚硝酸钠是一种护色剂和防腐剂 -
6、化学与生活紧密相关。下列有关说法不正确的是( )A、乙醇具有还原性,利用乙醇与酸性反应检验“酒驾” B、能使蛋白质变性,可用于游泳池的消毒 C、葡萄糖可以使新制的氢氧化铜转化成砖红色沉淀,可以用来检测病人尿液中的葡萄糖 D、广告标“品牌八宝粥用糯米、红豆、桂圆等制作,未加糖。”糖尿病患者可放心食用
-
7、自然资源的综合利用对人类极其重要,下列资源的开发利用中,不涉及化学变化的是( )A、煤的气化 B、煤的干馏 C、石油的分馏 D、石油的裂化
-
8、下列做法的目的与反应速率无关的是( )A、高炉炼铁前先将铁矿石粉碎 B、食盐中添加碘酸钾 C、在糕点包装内放置小包除氧剂 D、医护人员冷藏存放“新冠”疫苗
-
9、化学科学需要借助化学专用语言描述。下列有关化学用语正确的是( )A、乙烯的结构简式: B、羟基的电子式: C、四氯化碳分子的空间填充模型:
 D、乙酸分子的球棍模型
D、乙酸分子的球棍模型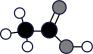
-
10、据我国古代第一部药物学专著《神农本草经》记载:“石硫黄(即硫黄)能化金银钢铁,奇物”。硫与某些金属单质化合所得的产物可能是( )A、 B、 C、 D、
-
11、开发新材料是现代科技发展的方向之一。下列有关材料属于新型无机非金属材料的是( )




A.口罩中使用的聚丙烯熔喷布
B.宇航服中使用的合成纤维
C.“瑞雪祥云”礼仪服智能发热使用的石墨烯
D.飞机风挡使用的有机玻璃
A、A B、B C、C D、D -
12、A、B、C、D、E、F、G、H为中学化学常见的有机物,一定条件下能发生下图所示的转化关系:
已知:①A是石油化工重要的基本原料,相对分子质量为28;
②C是一种液体燃料,E的分子式为;
③G遇碘水后显蓝色,H是G水解的最终产物。
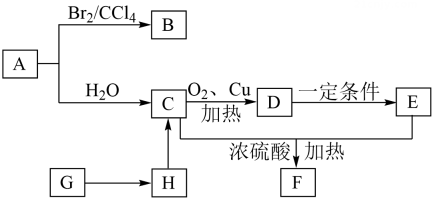 (1)、写出A的电子式:。(2)、G的分子式: , B中官能团的名称: , E中官能团的结构简式:。(3)、写出C→D的反应方程式并指明反应类型。(4)、写出H→C的方程式:。(5)、将H的溶液与新制氢氧化铜悬浊液混合加热,可观察到的现象是: , 实验室用C和E反应制备F时,所加碎瓷片的作用是:。(6)、有机物I是A的同系物,分子量比A大14,与A具有相同的官能团。一定条件下I与加成的产物可能有(写结构简式)。
(1)、写出A的电子式:。(2)、G的分子式: , B中官能团的名称: , E中官能团的结构简式:。(3)、写出C→D的反应方程式并指明反应类型。(4)、写出H→C的方程式:。(5)、将H的溶液与新制氢氧化铜悬浊液混合加热,可观察到的现象是: , 实验室用C和E反应制备F时,所加碎瓷片的作用是:。(6)、有机物I是A的同系物,分子量比A大14,与A具有相同的官能团。一定条件下I与加成的产物可能有(写结构简式)。 -
13、用合成燃料甲醇()是碳减排的新方向。现进行如下实验:某温度下在体积为1L的密闭容器中,充入2mol和6mol发生反应:
, 请回答下列问题:
(1)、能判断该反应已达化学平衡状态的标志是____(填字母)。A、百分含量保持不变 B、容器中浓度与浓度之比为3:1 C、容器中混合气体的密度保持不变 D、的生成速率与的生成速率相等(2)、现测得和的浓度随时间变化如图所示,回答下列问题:
①从反应开始到平衡,氢气的平均反应速率。
②平衡时甲醇的体积分数为 , 反应过程中的最大转化率为。
(3)、下图是以为电解质溶液的甲醇燃料电池示意图: , 通入氧气的电极为燃料电池的极(填“正”或“负”),随着电池工作,电解质溶液的如何变化。
A.变大 B.变小 C.不变 D.无法判断
-
14、人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,探究其相关性质。
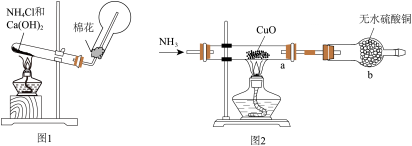 (1)、Ⅰ.实验室制取氨气。
(1)、Ⅰ.实验室制取氨气。
图1装置中生成的化学方程式为。(2)、仪器b的名称是 , b中无水硫酸铜的作用是。(3)、实验中观察到a中粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为。(4)、若向a中通入标准状况下3.36L的氨气,最终得到铜的质量为g(保留小数点后一位)。(5)、Ⅲ.按下图装置进行其他性质实验,A、B容器的容积相同。
先打开旋塞1,B瓶中的现象是 , 原因是;稳定后,关闭旋塞1。再打开旋塞2,B瓶中的现象是。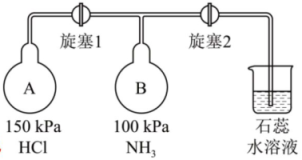
-
15、腈纶织物广泛用作衣物、床上用品等。腈纶是由丙烯腈()聚合而成的,丙烯腈可以由丙烯()与氨、氧气反应制得,而丙烯主要来自石脑油的裂解,例如:。(1)、X的分子式是为 , 写出X可能的结构简式和名称。(2)、丙烯腈也可以由某不饱和烃A与一定条件下发生加成反应得到,写出该反应的化学方程式。(3)、合成纤维(如腈纶等)部分取代了棉、麻等天然纤维。天然纤维中含有的纤维素属于糖类物质,绿色植物将二氧化碳和水变成糖类的过程称为作用,写出由二氧化碳和水生成葡萄糖的化学方程式:。
-
16、铝是一种重要金属,从铝土矿(主要成分为 , 、等)中冶炼的工业生产流程如下图:(是酸性氧化物,不溶于盐酸)
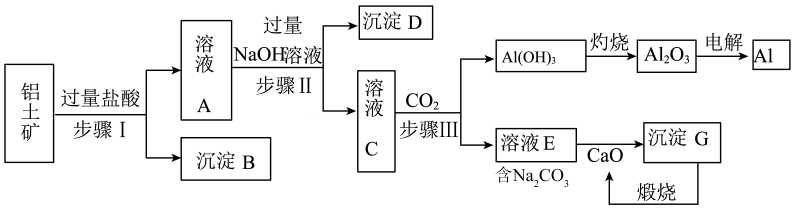 (1)、步骤Ⅰ中,为了提高铝土矿利用率可采取的措施有(任写一种);沉淀B为(填化学式)。(2)、步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是 , 该方法要用到的玻璃仪器有除了烧杯,还有。(3)、步骤Ⅲ中向溶液C中通入少量 , 。(4)、生产过程中,除可以循环使用外,还可以循环使用的物质有、(填化学式)。(5)、经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中的纯度(质量分数)(用含a、b的最简式表示)。
(1)、步骤Ⅰ中,为了提高铝土矿利用率可采取的措施有(任写一种);沉淀B为(填化学式)。(2)、步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是 , 该方法要用到的玻璃仪器有除了烧杯,还有。(3)、步骤Ⅲ中向溶液C中通入少量 , 。(4)、生产过程中,除可以循环使用外,还可以循环使用的物质有、(填化学式)。(5)、经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中的纯度(质量分数)(用含a、b的最简式表示)。 -
17、实验室制取下列气体,所选反应试剂、制备装置与收集方法都合理的是( )
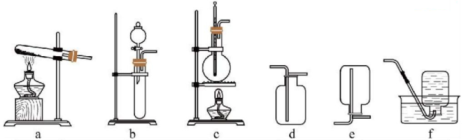
选项
气体
反应试剂
制备装置
收集方法
A
、
a
f
B
、稀硫酸
b
e
C
、浓硝酸
c
d
D
、70%硫酸
b
f
A、A B、B C、C D、D -
18、已知有机物M、N、W能发生下列反应,下列说法不正确的是( )
 A、M的一氯代物有3种 B、W分子中所有碳原子不可能共平面 C、该反应原子利用率为100% D、M、N分子中碳碳双键的数目比为3:1
A、M的一氯代物有3种 B、W分子中所有碳原子不可能共平面 C、该反应原子利用率为100% D、M、N分子中碳碳双键的数目比为3:1 -
19、把一定质量的铜完全溶解于某浓度的硝酸中收集到0.3mol和0.2mol。向反应后的溶液中加入足量溶液充分反应,经过滤、洗涤后,把所得沉淀加热至质量不再减少为止,得到固体质量为( )A、24g B、36g C、40g D、44.1g
-
20、海水资源综合利用的部分过程如下图所示,下列说法错误的是( )
海水
→淡化:淡水
→制盐工业:粗盐→精盐
→制溴工业:
→制镁工业:
A、蒸馏海水可获得淡水 B、为除粗盐中的、、 , 可依次加入足量的、、溶液 C、在制溴工业中,通过氧化、还原、再氧化的步骤实现了溴的富集 D、在制镁工业中,可用贝壳为原料生产石灰乳以沉淀