相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、为阿伏加德罗常数的值,下列叙述正确的是( )A、常温常压下,28gCO和的混合气体中所含分子的数目为 B、常温常压下,2.3g钠在足量的氧气中燃烧时,转移的电子数为 C、标准状况下,11.2L氯气所含的原子数为 D、常温常压下,溶液中含有的钾离子数为
-
2、下列有关钠及其化合物的说法错误的是( )A、金属钠长期暴露在空气中,最终转化为氢氧化钠 B、在实验室中,钠保存在石蜡油或煤油中 C、和的阴、阳离子个数比均为1∶2 D、向饱和氯化钠溶液中先通入过量氨气再通入过量二氧化碳可得到碳酸氢钠晶体
-
3、下列转化过程中,要加入氧化剂才能实现的是( )A、 B、 C、 D、
-
4、下列叙述正确的是( )A、Cu的摩尔质量为64g B、的摩尔质量为 C、标准状况下,1molHCl和的体积相同 D、任何条件下,气体摩尔体积都约为
-
5、下列属于氧化还原反应的是( )A、 B、 C、 D、
-
6、下列关于胶体叙述错误的是( )A、光线透过雾霾时,可以观察到丁达尔效应 B、依据分散质粒子的直径大小可将分散系分为溶液、胶体和浊液 C、按照分散剂的不同,胶体可分为液溶胶、气溶胶和固溶胶 D、向饱和溶液中滴加过量的NaOH溶液可以制备胶体
-
7、下列氧化物属于酸性氧化物的是( )A、CO B、CO2 C、Na2O D、Na2O2
-
8、化学与生产、生活密切相关,下列说法错误的是( )A、小苏打既是制作糕点的膨松剂,又是治疗胃酸过多的一种药剂 B、二氧化氯()臭氧()具有强氧化性,可以用于自来水消毒 C、当火灾现场存放有大量活泼金属时,可以用水来灭火 D、维生素C具有还原性,能帮助人体将食物中摄取的转化为而吸收
-
9、实验室用下图所示装置进行氯气性质的探究并制备无水FeCl3查阅相关资料可知:无水FeCl3在空气中易潮解,加热易升华。
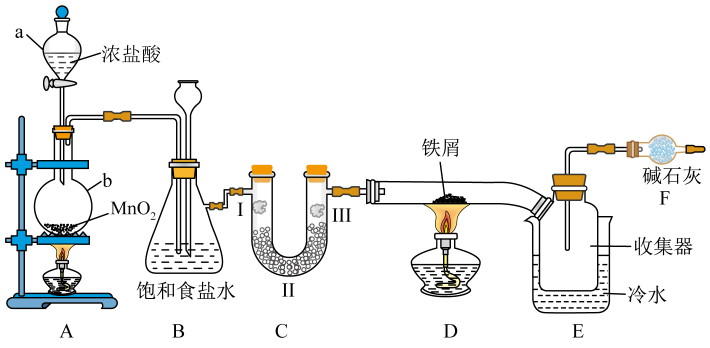 (1)、仪器b的名称为(2)、若实验时使用的17.4gMnO2 完全反应,产生的Cl2在标准状况下的体积为。(3)、装置B的作用是 , 同时用作安全瓶(监测实验时装置C中是否发生堵塞);若装置C发生堵塞,则装置B中将观察到的现象是。(4)、装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质是(填字母)。
(1)、仪器b的名称为(2)、若实验时使用的17.4gMnO2 完全反应,产生的Cl2在标准状况下的体积为。(3)、装置B的作用是 , 同时用作安全瓶(监测实验时装置C中是否发生堵塞);若装置C发生堵塞,则装置B中将观察到的现象是。(4)、装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质是(填字母)。A
B
C
D
Ⅰ
干燥的有色布条
湿润的有色布条
干燥的有色布条
湿润的有色布条
Ⅱ
碱石灰
无水氯化钙
无水氯化钙
浓硫酸
Ⅲ
湿润的有色布条
干燥的有色布条
湿润的有色布条
干燥的有色布条
(5)、装置D中生成的FeCl3大部分进入收集器,少量沉积在D装置的右端,要使沉积的FeCl3进入收集器,操作是(6)、实验结束时,应先熄灭(填“A”或“D”)处酒精灯;E中冷水的作用是。(7)、装置F的作用。 -
10、某家用防疫用品“84消毒液”的包装说明如下,请回答下列问题:
【产品名称】84消毒液
【有效成分】NaClO
【规格】1000mL
【物质的量浓度】4.0
注:①按一定比例稀释后使用
②不得与酸性产品(如洁厕灵)同时使用。
(1)、“84”消毒液可由Cl2与NaOH溶液反应制得,Cl2与NaOH溶液反应的化学方程式为(2)、欲将“84消毒液”原液稀释配制成450mL c(NaClO)=0.100mol·L-1的溶液。①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、、。
②配制时,需要取用mL“84消毒液”原液。
③下列操作会使溶液中NaClO浓度偏低的是。
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)、利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是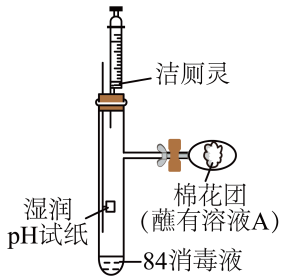
-
11、过氧化钙(CaO2)微溶于水,可作医用防腐剂、消毒剂,以下是制备CaO2的一种方法。回答下列问题:

回答下列问题:
(1)、CaO2中氧元素化合价。(2)、步骤Ⅱ中反应的化学方程式是(有NH4Cl生成):。(3)、反应在冰水浴中进行,目的是为了防止NH3·H2O分解和。(答1条即可)(4)、待CaO2·8H2O结晶析出后通过(填操作名称)分离。(5)、CaO2久置于空气中会生成CaCO3 , 为测定某CaO2样品的纯度,取10g样品加入足量稀盐酸,测得生成CO2的质量为1.1g,则样品中CaO2的质量分数为。 -
12、回答下列问题(用NA表示阿伏加德罗常数的值)(1)、40.5g某金属氯化物MCl2中含0.6molCl- , 则该氯化物的摩尔质量为。(2)、标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为。(3)、从400mL2.0mol/L的Al2(SO4)3溶液中取出20mL,将这20mL溶液用水稀释到100mL,所得溶液中SO的物质的量浓度为。(4)、在0.3L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示。

该混合液中CaCl2的物质的量为。
-
13、根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:(1)、SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:。(2)、现有:①熔融KOH;②稀硫酸;③氨水;④明矾(KAl(SO4)2·12H2O);⑤蔗糖;⑥铜;⑦H2S;其中能导电的是(填序号,下同);属于电解质的是。写出④在水溶液中的电离方程式:。(3)、酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐。
①NaH2PO2为。(填序号)
A.正盐 B.酸式盐 C.碱式盐
②写出H3PO2溶液与足量NaOH溶液反应的化学方程式。
-
14、现有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH、Ba2+、CO、Cl-、SO。现取两份各200mL溶液进行如下实验:
①第一份加足量NaOH溶液,加热,收集到气体1.7g;
②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。
根据上述实验,以下推测正确的是( )
A、一定存在NH、CO、SO , 一定不存在Ba2+、Cl- B、一定存在NH、CO、Cl-、SO , 可能存在K+ C、若溶液中存在NH、Cl-、CO、SO、K+五种离子,则c(K+)>0.1mol·L-1 D、c(SO)=0.1mol·L-1 , c(NH)<c(SO) -
15、为除去粗盐中的Ca2+、Mg2+、SO及泥沙等杂质,某同学设计了一种制备精盐的实验方案,流程如图,下列说法正确的是( )
 A、第①步操作A是溶解,第⑦步操作C是过滤 B、第③步作用是除掉Ca2+ C、第⑥步不可以调至第④步和第⑤步之间 D、第①⑤⑦步操作都用到漏斗
A、第①步操作A是溶解,第⑦步操作C是过滤 B、第③步作用是除掉Ca2+ C、第⑥步不可以调至第④步和第⑤步之间 D、第①⑤⑦步操作都用到漏斗 -
16、把aL含硫酸铵和硝酸铵的混合液分成2等份,一份需用bmol烧碱刚好把铵全部反应,另一份与氯化钡溶液完全反应时,消耗2cmol氯化钡。由此可知原溶液中NO离子的物质的量浓度为(注:SO+Ba2+=BaSO4↓、NH+ OH-=NH3·H2O)( )A、 mol/L B、 mol/L C、 mol/L D、 mol/L
-
17、甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。下列各组物质按照甲、乙、丙的顺序不符合要求的是( )
 A、H2O2 、H2O、O2 B、NaOH、Na2CO3、NaNO3 C、CO2、CaCO3、CaO D、Fe2O3、FeCl3、Fe(OH)3
A、H2O2 、H2O、O2 B、NaOH、Na2CO3、NaNO3 C、CO2、CaCO3、CaO D、Fe2O3、FeCl3、Fe(OH)3 -
18、下列关于氯及其化合物的说法中正确的是( )A、Cl2的化学性质非常活泼,因此不能用钢瓶贮存液氯 B、新制氯水在密闭无色玻璃瓶中放置数天后酸性减弱 C、向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有HClO D、H2在Cl2中燃烧,火焰呈苍白色,工业上利用该原理生产盐酸
-
19、除去下列物质中的杂质(括号内为杂质),选用试剂及操作方法均正确的一组是( )
选项
待提纯的物质
选用的试剂
操作的方法
A
CO2(HCl)
氢氧化钠溶液
洗气
B
Cu(Fe)
稀盐酸
溶解、过滤、洗涤、干燥
C
FeSO4(H2SO4)
氢氧化钠溶液
过滤
D
N2(CO)
氧气
点燃
A、A B、B C、C D、D -
20、室温下,某容积固定的密闭容器由可移动的活塞隔成甲、乙两室,向甲中充入34gH2和O2的混合气体,向乙中充入1mol 空气,此时活塞的位置如图所示。下列有关说法错误的是 ( )
 A、甲室H2、O2的体积比为1:2 B、甲室混合气体的分子总数约为2NA C、甲室混合气体的密度是同温同压时H2密度的8.5倍 D、若将甲室H2、O2的混合气体点燃引爆,恢复原室温后,最终活塞停留的位置在刻度2处
A、甲室H2、O2的体积比为1:2 B、甲室混合气体的分子总数约为2NA C、甲室混合气体的密度是同温同压时H2密度的8.5倍 D、若将甲室H2、O2的混合气体点燃引爆,恢复原室温后,最终活塞停留的位置在刻度2处