相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列离子方程式中,正确的是( )A、用氯化铁溶液腐蚀覆铜板: B、氯气溶于水发生反应: C、向氯化铝溶液中滴加氨水: D、向硫酸氢钠溶液中加入至硫酸根离子恰好沉淀完全:
-
2、下列各组离子在对应条件下能大量共存的是( )A、在pH=1的溶液中:、、、 B、无色澄清溶液:、、、 C、遇酚酞变红的溶液:、、、 D、遇石蕊变红的溶液:、、、
-
3、下列溶液中浓度与50 mL 1.5 mol/L Na2SO4溶液中浓度相等的是( )A、75 mL 1 mol/L的FeSO4溶液 B、25 mL 3 mol/L K2SO4溶液 C、150 mL 0.5 mol/L的溶液 D、150 mL 0.5 mol/L的H2SO4溶液
-
4、表示阿伏加德罗常数的值,下列说法正确的是( )A、3.36 L NH3气体中含氮原子个数为 B、与NaOH反应时,每消耗1 mol Cl2转移电子数目为 C、48 g由O2和O3组成的混合气体中含有的原子数为 D、常温常压下,1 mol/L的NaCl溶液中含有个
-
5、工业废水中含有重铬酸根离子(),有毒,必须处理达标后才能排放。工业上常用绿矾()做处理剂,反应的原理为:。下列关于该反应的说法中,正确的是( )A、氧化剂是 B、每处理1 mol , 需要消耗 56 g C、氧化性强弱: D、每处理0.1 mol , 转移电子数为
-
6、用下列装置进行实验,能达到实验目的的是( )
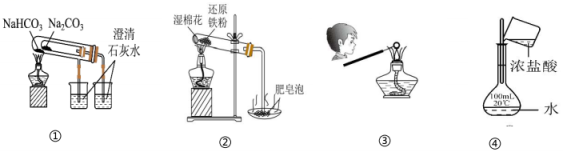 A、用图①比较Na2CO3和NaHCO3的稳定性 B、用图②装置进行铁与水蒸气的反应,点燃肥皂泡检验氢气 C、用图③装置乙检验草木灰中含有 D、用图④浓盐酸配制一定物质的量浓度的稀盐酸
A、用图①比较Na2CO3和NaHCO3的稳定性 B、用图②装置进行铁与水蒸气的反应,点燃肥皂泡检验氢气 C、用图③装置乙检验草木灰中含有 D、用图④浓盐酸配制一定物质的量浓度的稀盐酸 -
7、下列物质或试剂加到紫色石蕊溶液中,不能使其褪色的是( )A、新制氯水 B、久置氯水 C、过氧化钠 D、漂白粉
-
8、下列关于钠及其化合物的性质及用途的说法不正确的是( )A、相同温度时,在水中的溶解性:NaHCO3<Na2CO3 B、向碳酸钠中加入少量水后,碳酸钠会结块变为晶体,并伴随有吸热现象 C、过氧化钠可在呼吸面具中作为氧气的来源 D、存有金属钠的现场发生火灾时,不能用水来灭火
-
9、34号元素硒(Se)是人体必需的微量元素,其最外层有6个电子。下列有关说法不正确的是( )A、Se元素位于元素周期表第四周期第ⅥA族 B、H2Se的还原性比H2O的还原性强 C、和互为同位素 D、原子中质子数为34,中子数为78
-
10、微纳米材料研究所研发的纳米量级碳酸钙直径约为30 nm,下列有关说法正确的是( )A、纳米量级碳酸钙是一种胶体 B、若将纳米量级碳酸钙均匀分散到蒸馏水中,不能透过滤纸 C、若将纳米量级碳酸钙加入稀盐酸中,不会有二氧化碳产生 D、若将纳米量级碳酸钙均匀分散到蒸馏水中,会产生丁达尔效应
-
11、下列物质在水溶液中的电离方程式不正确的是( )A、 B、 C、 D、
-
12、下列反应属于氧化还原反应的是( )A、 B、 C、 D、
-
13、下列物质能导电且属于电解质的是( )A、NaCl固体 B、石墨 C、KNO3溶液 D、熔融的MgCl2
-
14、下列仪器与名称对应且书写正确的是( )A、三脚架
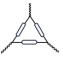 B、坩埚
B、坩埚 C、长颈漏斗
C、长颈漏斗 D、圆底烧瓶
D、圆底烧瓶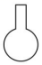
-
15、下列物质属于酸性氧化物的是( )A、CO2 B、Na2O2 C、NO D、Fe2O3
-
16、氯酸锶为白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。可溶于水,是一种常见的可溶性强碱。
下图为实验室制取氯酸锶的实验装置图,反应的化学方程式:。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
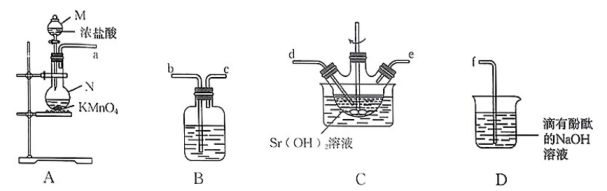 (1)、仪器M的名称是 , 仪器N的名称是。(2)、仪器接口的连接顺序为a→。(3)、D中发生反应的化学方程式为。(4)、使浓盐酸顺利滴下的操作方法为 , 再打开分液漏斗下端活塞。(5)、装置B中所装试剂名称为 , 其作用是。(6)、实验过程中发现装置D中溶液褪色,分析可能的原因:(答出两点)。
(1)、仪器M的名称是 , 仪器N的名称是。(2)、仪器接口的连接顺序为a→。(3)、D中发生反应的化学方程式为。(4)、使浓盐酸顺利滴下的操作方法为 , 再打开分液漏斗下端活塞。(5)、装置B中所装试剂名称为 , 其作用是。(6)、实验过程中发现装置D中溶液褪色,分析可能的原因:(答出两点)。 -
17、硫酸亚铁铵晶体俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制溶液。请回答下列问题:(1)、配制溶液过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需。(2)、用电子天平(精确度为)称量晶体g。(3)、定容时发现液面超过了刻度线,处理的方法是。(4)、下列操作将导致所配制的溶液浓度偏小的是(填序号)。
①摩尔盐放置过程中失去了部分结晶水
②定容后振荡容量瓶发现液面低于刻度线,继续加蒸馏水定容
③定容时仰视容量瓶刻度线
④容量瓶注入溶液前有少量蒸馏水
(5)、已知溶液的密度大于水,用溶液和等质量的水混合,所得溶液的浓度(填“大于”、“小于”或“等于”)。 -
18、物质的量是宏观量与微观量相互联系的桥梁,回答下列问题。(1)、等质量的和所含分子个数比为;常温常压下,等体积的和两种气体所含原子个数比为 , 质量比为。(2)、将6L标准状况下的氯化氢气体溶于100mL水中(水的密度近似为),得到密度为的盐酸,则该盐酸的物质的量浓度是(列出计算式)。(3)、铜有两种常见的氧化物CuO和。某学习小组用电子天平称取固体,加热至完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuOg,g。

-
19、完成下列填空:
现有物质:①铜 ②干冰 ③盐酸 ④液态硫酸 ⑤蔗糖 ⑥固体 ⑦红褐色的氢氧化铁胶体。
(1)、属于分散系的是(填序号,下同);能够导电的是;写出属于酸式盐的物质溶于水后的电离方程式:。(2)、⑦区别于溶液和浊液的本质特征为 , 利用效应可区分胶体和溶液。(3)、氢氧化铁胶体可用于净水的原因是。 -
20、一个密闭容器中间有一可自由滑动的隔板(厚度不计),隔板将容器分成左右两室,左室充入 , 右室充入一定量的CO和 , 隔板位置如图Ⅰ,并持续用电火花引燃右室气体,充分反应后恢复至起始温度,隔板位置如图Ⅱ。右室中生成的物质的量为( )
 A、 B、 C、 D、
A、 B、 C、 D、