相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列有关铁及其化合物的说法正确的是( )A、在自然界中,不可能有游离态的铁存在 B、磁铁矿的主要成分是Fe2O3 C、铁是地壳中含量最多的金属元素,因此在日常生活中应用最广 D、人体内的血红蛋白中含有铁元素
-
2、某废镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体():
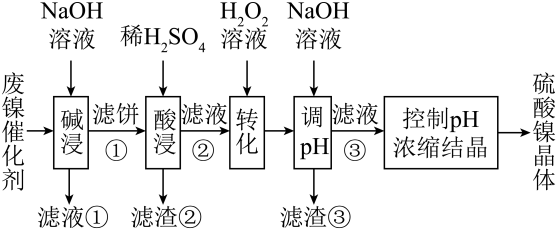
回答下列问题:
(1)、 “碱浸”中的两个作用分别是除去油脂和溶解Al和Al2O3 , 写出Al和NaOH溶液反应的化学方程式(2)、滤液②中含有的金属离子是(填离子符号)(3)、“转化”中可替代的最佳物质是____。(填字母)A、酸性溶液 B、 C、硝酸 D、新制氯水(4)、调pH范围为3.2~7.2,沉淀出滤渣③的成分是Fe(OH)3 , 调pH除去的杂质离子是(填离子符号)
(5)、滤液③的主要离子是Ni2+ , 检验滤液是否含有Fe3+的试剂是(填化学式)(6)、将分离出硫酸镍晶体后的母液收集、循环使用,其意义是。 -
3、钠是一种非常活泼、具有广泛应用的金属。(1)、钠的原子结构示意图为 , 钠在反应中容易电子(填“得到”或“失去”)。(2)、汽车安全气囊的气体发生剂可由金属钠生产。某汽车安全气囊内含、和等物质。
ⅰ.当汽车发生较严重的碰撞时,引发分解 , 从而为气囊充气。产生的Na立即与发生置换反应生成 , 化学方程式是。
ⅱ.是冷却剂,吸收产气过程释放的热量。起冷却作用时发生反应的化学方程式为。
ⅲ.一个安全气囊通常装有 , 其完全分解所释放的为mol。(保留两位小数)
(3)、工业通过电解NaCl生产金属钠: , 过程如下:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入从而把熔点降至约580℃。
①把NaCl固体加热至熔融状态,目的是。
②粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是。
-
4、海洋是资源的宝库,蕴藏着丰富的氯、溴、碘等元素。氯、溴、碘是典型的非金属元素,都能与大多数金属化合生成盐,故统称为卤素;卤素单质都具有氧化性。(1)、氯在元素周期表中的位置(2)、氯气是重要的化工产品,工业可以由电解氯化钠溶液得到,同时还生成NaOH和H2。写出该电解过程的离子方程式(3)、氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱顺序为:。试写出:
在NaBr和KSCN的混合溶液中滴加少量(CN)2 , 请写出发生反应的离子方程式。
(4)、 NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:I.上述反应的还原剂是
II.根据上述反应,鉴别某白色固体是NaNO2还是NaCl。可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉溶液 ④白酒 ⑤食醋(稀的醋酸溶液),你认为必须选用的物质有(填字母)。
A .③⑤ B.①②⑤ C.①②④
III.某厂废液中,含有2%~5%的NaNO2直接排放会造成污染,下列试剂能使NaNO2转化为N2防止污染的是。(填字母)
A.NaCl B. C. D.浓
-
5、氯元素可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并比较其氧化性。
已知:氯气与碱溶液反应,在低温和稀碱溶液中主要产物是ClO-和Cl- , 在75℃以上和浓碱溶液中主要产物是ClO3-和Cl-

回答下列问题:
(1)、 甲中盛放浓盐酸的仪器名称是 , 甲中发生的反应的化学方程式是(2)、乙中的试剂为(3)、丙中发生反应的化学方程式是(4)、丁采用冰水浴冷却的目的是(5)、戊的作用是尾气吸收,可选用试剂 ____(填字母)。A、H2SO4 B、NaOH C、NaCl D、Ca(OH)2(6)、反应结束后,取出丙中试管,经冷却结晶、、洗涤、干燥,得到KClO3晶体。(7)、取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显紫色。可知该条件下KClO3的氧化能力NaClO(填“大于”或“小于”)。 -
6、下列实验操作、现象及结论均正确的是( )
选项
实验操作
现象
结论
A
取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液
溶液颜色变红
溶液X含有Fe3+
B
向饱和的Na2CO3溶液通入CO2
产生白色沉淀
溶解度:NaHCO3<Na2CO3
C
向Fe2O3、CuO、Fe的混合粉末中加入过量稀盐酸
析出红色固体
反应后溶液中阳离子只有H+和Fe2+
D
向煮沸的NaOH溶液中滴入几滴饱和FeCl3溶液,继续加热
溶液变成红褐色
制得Fe(OH)3胶体
A、A B、B C、C D、D -
7、实验室模拟以含铁废渣(主要成分为FeO、Fe2O3 , 杂质为Cu2(OH)2CO3、CuO)为原料制备七水硫酸亚铁(FeSO4·7H2O)的流程如图所示。下列说法错误的是( )
 A、“除铜”步骤的反应类型有置换反应和化合反应 B、含铁废渣中的FeO、Fe2O3、CuO均属于碱性氧化物 C、实验室需要500 mL0.1 mol•L-1FeSO4溶液,需要称取7.6 g FeSO4·7H2O配制 D、铜器生锈[主要成分为Cu2(OH)2CO3]的反应原理为:2Cu+O2+H2O+CO2=Cu2(OH)2CO3
A、“除铜”步骤的反应类型有置换反应和化合反应 B、含铁废渣中的FeO、Fe2O3、CuO均属于碱性氧化物 C、实验室需要500 mL0.1 mol•L-1FeSO4溶液,需要称取7.6 g FeSO4·7H2O配制 D、铜器生锈[主要成分为Cu2(OH)2CO3]的反应原理为:2Cu+O2+H2O+CO2=Cu2(OH)2CO3 -
8、设NA为阿伏加德罗常数的数值,下列说法正确的是( )A、足量Cl2与2.8 g Fe充分反应,转移的电子数为0.1NA B、常温常压,1.6 g的氧气和臭氧混合气体中,含有氧原子的数目为0.1NA C、22.4L CO2中含有原子数为3NA D、100 mL 0.1 mol·L-1的H2SO4溶液中含有的氧原子数为0.04NA
-
9、化学是以实验为基础的科学。下列实验操作能达到实验预期目的的是( )
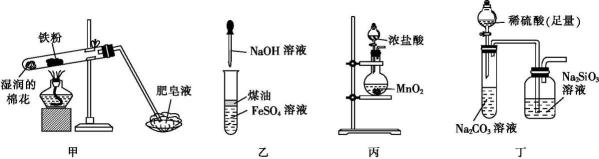 A、图甲:验证铁粉与水蒸气反应 B、图乙:制取Fe(OH)2沉淀并长时间观察其颜色 C、图丙:制取少量氯气 D、图丁:验证C和Si的非金属性强弱
A、图甲:验证铁粉与水蒸气反应 B、图乙:制取Fe(OH)2沉淀并长时间观察其颜色 C、图丙:制取少量氯气 D、图丁:验证C和Si的非金属性强弱 -
10、如图中a、b、c、d、e、f为含Cl元素的物质。下列说法不正确的是
 A、a溶液的酸性比d强 B、b、c均能用于自来水消毒 C、f露置于空气中会转化成d D、实验室可利用e的固体制备氧气,每生成1 mol O2转移2mol e-
A、a溶液的酸性比d强 B、b、c均能用于自来水消毒 C、f露置于空气中会转化成d D、实验室可利用e的固体制备氧气,每生成1 mol O2转移2mol e- -
11、配制100mL1.00mol/LNaCl溶液,部分实验操作示意图如下。

下列说法不正确的是( )
A、该实验中用到的玻璃仪器有:烧杯、玻璃棒、100mL容量瓶、胶头滴管等 B、上述实验操作步骤的正确顺序为②①④③ C、容量瓶用蒸馏水洗涤后,不必经过干燥即可使用 D、定容时,俯视观察刻度线,会引起溶液的浓度偏低 -
12、NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法中正确的是( )
 A、25℃时,NaHCO3在水中的溶解度比Na2CO3的大 B、工业上可用石灰乳与Cl2反应制取漂粉精 C、Cl2和H2在点燃的条件下安静燃烧,产生淡蓝色火焰 D、如图所示转化反应都是氧化还原反应
A、25℃时,NaHCO3在水中的溶解度比Na2CO3的大 B、工业上可用石灰乳与Cl2反应制取漂粉精 C、Cl2和H2在点燃的条件下安静燃烧,产生淡蓝色火焰 D、如图所示转化反应都是氧化还原反应 -
13、下列有关物质的性质与用途不具有对应关系的是( )A、铁粉能与O2反应,可用作食品保存的吸氧剂 B、纳米Fe3O4能与酸反应,可用作铁磁性材料 C、FeCl3具有氧化性,可用于腐蚀印刷电路板上的Cu D、聚合硫酸铁能水解并形成胶体,可用于净水
-
14、下表中对“陈述”的解释错误的是( )
选项
陈述
解释
A
NaHCO3用于治疗胃酸过多
NaHCO3可与盐酸反应
B
向Na2O2与H2O反应后的溶液中滴入MgCl2溶液,产生白色沉淀
Na2O2与水反应生成氢氧化钠,OH-与Mg2+反应生成Mg(OH)2
C
金属钠应保存在煤油中隔绝空气
常温下,金属钠露置在空气中会生成过氧化钠
D
过氧化钠可用作航天员的供氧剂
能和、反应生成
A、A B、B C、C D、D -
15、下列选项不能用来证明Cl的非金属性比I的非金属性强的是( )A、ICl中I是+1价,Cl是-1价 B、稳定性:HCl > HI C、酸性:HCl < HI D、Fe3+可以氧化I- , 但不能氧化Cl-
-
16、下列离子方程式中,正确的是( )A、铁与稀盐酸的反应:2Fe+6H+=2Fe3+ +3H2↑ B、硫酸铜与氢氧化钡的反应:Ba2++SO42-=BaSO4↓ C、石灰石与盐酸的反应:CO32- +2H+ =H2O+CO2↑ D、硝酸银与氯化钠的反应:Ag+ + Cl- =AgCl↓
-
17、实验安全是保证科学研究的前提,下列操作符合实验室安全要求的是( )A、钠着火可用干粉泡沫灭火器进行灭火 B、实验后将多余的固体钾扔在有水的废液缸里 C、未佩戴防护眼镜,近距离俯视观察金属钠与水的反应 D、大量氯气泄漏,应迅速离开现场,向高处去。
-
18、生活中处处是化学,下列说法错误的是( )
选项
A
B
C
D
生活中
的化学

树林中的丁达尔效应

维生素C片

节日烟火

氢氧化钠片
化学原理
(或用途)
树林中存在分散质粒子直径介于1 nm~100 nm的分散系
能将人体中摄取的不易吸收的铁离子转化为易吸收的亚铁离子,是因其具有还原性
属于金属元素的焰色试验
常用来治疗胃酸过多
A、A B、B C、C D、D -
19、杭州亚运会主火炬用了一种全球大型赛事中从未使用过的燃料—“零碳甲醇”,甲醇(CH3OH)是太阳能的最佳载体,也被成为“液态阳光”。当H2O经太阳光光解制成H2 , 空气中的CO2加H2又能生成CH3OH。在这一过程中,实现了零污染零排放,并可以循环使用,是迄今为止人类制备CH3OH最清洁环保的方式之一。下列叙述不正确的是( )A、CO2是酸性氧化物 B、H2O既是氢化物也是氧化物 C、CH3OH、H2都属于非电解质 D、H2O光解制H2的反应属于氧化还原反应
-
20、辉铜矿主要成分Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2 , 以及少量SiO2、Fe2O3等杂质。研究人员开发综合利用这两种资源,用同槽酸浸湿法冶炼工艺,制备硫酸锰和碱式碳酸铜。主要工艺流程如下:已知:①MnO2有较强的氧化性,能将Cu+氧化成Cu2+
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4。
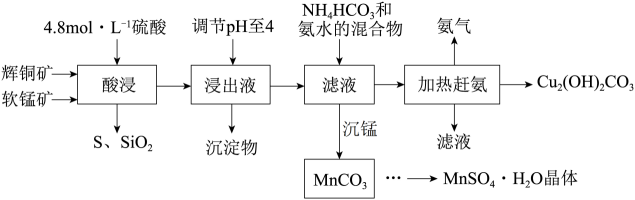 (1)、实验室配制250mL4.8mol/L的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要。(2)、酸浸时,为了提高浸取率可采取的措施有(任写一点)。(3)、酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式。(4)、调节浸出液pH=4的作用是。(5)、本工艺中可循环使用的物质是(写化学式)。(6)、获得的MnSO4·H2O晶体后常用酒精洗涤,优点是。(7)、用标准的BaCl2溶液测定样品中MnSO4·H2O质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略)其可能原因有(任写一种)。
(1)、实验室配制250mL4.8mol/L的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要。(2)、酸浸时,为了提高浸取率可采取的措施有(任写一点)。(3)、酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式。(4)、调节浸出液pH=4的作用是。(5)、本工艺中可循环使用的物质是(写化学式)。(6)、获得的MnSO4·H2O晶体后常用酒精洗涤,优点是。(7)、用标准的BaCl2溶液测定样品中MnSO4·H2O质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略)其可能原因有(任写一种)。