相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
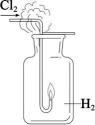
1、下列实验装置正确且能达到对应实验目的的是( )
Ⅰ
 Ⅱ
Ⅱ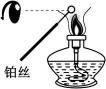 Ⅲ
Ⅲ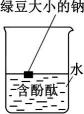 Ⅳ
Ⅳ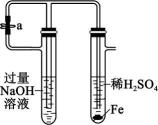 A、图Ⅰ:H2在Cl2中安静地燃烧 B、图Ⅱ:检验待测物中含有钾元素 C、图Ⅲ:观察金属钠与水的反应 D、图Ⅳ:制备并观察Fe(OH)2的颜色
A、图Ⅰ:H2在Cl2中安静地燃烧 B、图Ⅱ:检验待测物中含有钾元素 C、图Ⅲ:观察金属钠与水的反应 D、图Ⅳ:制备并观察Fe(OH)2的颜色 -
2、高铁酸钾(K2FeO4)作净水剂时会产生Fe3+ , 该过程既能消毒杀菌,也能吸附水中悬浮物。制备K2FeO4的一种方法的化学原理可用离子方程式表示为:
3ClO− + 2Fe3+ + 10OH− = 2FeO42− + 3Cl− + 5H2O
下列说法错误的是( )
A、K2FeO4中铁元素的化合价为+6价 B、ClO−作氧化剂,Fe3+被还原 C、0.6 mol ClO−参与反应时生成0.4 mol FeO42− D、K2FeO4净水时会生成Fe(OH)3胶体 -
3、下列物质中均既含有离子键又含有共价键的是( )
①NH4Cl ②H2O2 ③HI ④MgCl2 ⑤NaF ⑥KOH
A、①④ B、③⑤ C、②④ D、①⑥ -
4、右图是元素周期表中磷元素的相关信息,根据图示信息可推知下列选项错误的是( )
 A、磷原子的核电荷数为15 B、红磷、白磷是磷元素的同位素 C、P4的摩尔质量约为124 g·mol−1 D、内层电子总数是M层电子数的2倍
A、磷原子的核电荷数为15 B、红磷、白磷是磷元素的同位素 C、P4的摩尔质量约为124 g·mol−1 D、内层电子总数是M层电子数的2倍 -
5、下列离子反应方程式错误的是( )A、向氧化钠中滴加稀盐酸:Na2O + 2H+ = 2Na+ + H2O B、铝锅不能煮碱性的食物:2Al + 2Na+ + 2OH− + 6H2O = 2Na[Al(OH)4]+ 3H2↑ C、向稀盐酸中滴加碳酸钠溶液:CO32− + 2H+ = CO2↑ + H2O D、氢氧化钡溶液与稀硫酸反应:Ba2+ + 2OH− + 2H+ + SO42− = BaSO4↓ + 2H2O
-
6、溶液导电能力取决于自由移动离子的浓度、离子所带电荷数和离子种类。若忽略离子种类对溶液导电能力的影响,离子浓度越大,所带电荷数越多,溶液导电能力越强。下列溶液的导电性最强的是( )A、1.5 mol·L−1 Na2SO4溶液 B、2.0 mol·L−1 MgCl2溶液 C、1.5 mol·L−1 HCl溶液 D、2.5 mol·L−1 Ba(OH)2溶液
-
7、在无色溶液中,下列离子能大量共存的是( )A、NH4+、Al3+、OH−、SO42− B、Ba2+、Mg2+、Cl−、NO3− C、Na+、H+、MnO4−、OH− D、Fe2+、Na+、Cl−、NO3−
-
8、NA表示阿伏加德罗常数的值。下列说法正确的是( )A、0.5 mol Na2O与0.5 mol Na2O2所含Na+总数相同 B、1 mol MnO2与足量浓盐酸充分反应生成氯气22.4 L C、0.15 mol·L−1 NaOH溶液中离子数为0.3NA D、标准状况下,22.4 L乙醇所含分子数为NA
-
9、化学与生产、生活、科技、环境等密切相关。下列说法错误的是( )A、“朝坛雾卷,曙岭烟沉”,其中的“雾”是一种胶体,能产生丁达尔效应 B、绚烂的烟花是某些金属或它们的化合物在燃烧时火焰呈现出的特征颜色 C、“凡石灰经火焚炼为用”,其中涉及的化学反应为氧化还原反应 D、维生素C有较强的还原性,补血剂琥珀酸亚铁缓释片与维生素C同服,可增强该药物的吸收
-
10、以乙炔为原料制备乙酸和聚丙烯酸甲酯(
 )路线如下(部分反应条件已省略):
)路线如下(部分反应条件已省略):
回答下列问题:
(1)、X所含官能团名称是:。(2)、反应②的化学方程式为: , 该反应的类型为。(3)、反应③的化学方程式为: , 该反应的类型为。(4)、乙烯、、三种物质中可与金属钠反应的有 , 反应①②③中原子利用率为100%的是(填序号)。 -
11、资源化利用受到越来越多的关注,它能有效减少碳排放,有效应对全球
的气候变化,并且能充分利用碳资源。二氧化碳催化加氢制甲醇有利于减少温室气体
排放,涉及的反应如下:
Ⅰ.
Ⅱ. kJ⋅mol
Ⅲ. kJ⋅mol
回答下列问题:
(1)、kJ⋅mol。(2)、平衡常数(用、表示)。(3)、为提高反应Ⅲ中的平衡产率,应选择的反应条件为____(填标号)。A、低温、高压 B、高温、低压 C、低温、低压 D、高温、高压(4)、不同压强下,按照投料,发生反应Ⅰ,实验测得的平衡转化率随温度的变化关系如下图所示。
①压强、由大到小的顺序为 , 判断的依据是。
②图中A点对应的甲醇的体积分数是%(计算结果保留1位小数)。
(5)、在恒温恒压(压强为p)的某密闭容器中,充入1 mol 和3 mol , 仅发生反应Ⅰ和Ⅱ,经过一段时间后,反应Ⅰ和Ⅱ达到平衡,此时测得的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[]},则该温度下反应Ⅰ的平衡常数(写出计算式即可,分压=总压×物质的量分数)。 -
12、硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体()。向和混合溶液中通入可制得。实验装置如图所示(省略夹持装置)
 (1)、实验步骤:连接装置, , 按图示加入试剂。(2)、盛放的仪器a名称是。(3)、E装置的作用是。(4)、反应开始时,先打开(填“A”或“C”)中分液漏斗活塞,理由是。(5)、该实验一般控制在碱性环境,否则产品容易发黄,用离子方程式表示其原因。
(1)、实验步骤:连接装置, , 按图示加入试剂。(2)、盛放的仪器a名称是。(3)、E装置的作用是。(4)、反应开始时,先打开(填“A”或“C”)中分液漏斗活塞,理由是。(5)、该实验一般控制在碱性环境,否则产品容易发黄,用离子方程式表示其原因。 -
13、工业上由黄铜矿(主要成分)冶炼铜的主要流程如下:
 (1)、冰铜中的在高温下也能被氧化成和气体A,该反应的化学方程式是。(2)、下列处理气体A的方法,不合理的是。
(1)、冰铜中的在高温下也能被氧化成和气体A,该反应的化学方程式是。(2)、下列处理气体A的方法,不合理的是。a.高空排放 b.用纯碱溶液吸收制备亚硫酸钠
c.用氨水吸收后,再经氧化制备硫酸铵 d.用溶液吸收制备
(3)、用稀浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在(填离子符号)。(4)、由泡铜冶炼粗铜的化学反应方程式为。(5)、利用反应可制备 , 若将该反应设计为原电池,其负极电极反应式为。(6)、取一定量的泡铜,加入1 L 0.6 mol⋅L 溶液恰好完全溶解,同时放出2240 mL NO气体(标准状况),另取等量的泡铜,用足量的还原,得到的铜的质量为g。 -
14、研究化学反应中的能量变化对生产、生活有重要的意义。(1)、某氮肥厂含氮废水中的氮元素多以和形式存在,处理过程中在微生物的作用下经过两步反应被氧化成 , 这两步反应过程中的能量变化如图所示:

1 mol 全部被氧化成热化学方程式为。
使用更高效的催化剂,第二步反应的(填“变大”、“变小”或“不变”)。
(2)、已知 kJ⋅mol , 其他相关数据如下表:物质
键能/kJ·mol
436
200
a
则表中。
(3)、已知:kJ⋅mol
kJ⋅mol
若某反应(反应物与生成物均为气体)的平衡常数表达式为 , 请写出此反应的热化学方程式。
-
15、不同温度下,在某一恒容密闭容器中充入一定量的CO和 , 发生反应 。测得CO的平衡转化率的变化关系如图所示,下列说法正确的是( )
 A、正反应速率: B、平衡常数: C、a点时,再向容器中加入一定量CO,CO的平衡转化率一定增大 D、d点时,移除可使平衡正向移动且加快逆反应速率
A、正反应速率: B、平衡常数: C、a点时,再向容器中加入一定量CO,CO的平衡转化率一定增大 D、d点时,移除可使平衡正向移动且加快逆反应速率 -
16、已知反应的速率方程为(k为速率常数),其反应历程如下:
① 慢
② 快
下列说法正确的是( )
A、其他条件不变,适当升高温度,只可以提高反应①的速率 B、其他条件不变,增大或 , 可减慢总反应的反应速率 C、反应②的活化能高,该反应的快慢主要取决于反应② D、、分别增大相同的倍数,对总反应的反应速率的影响程度不相同 -
17、在一个绝热、体积一定的密闭容器中,充入2 mol 和6 mol , 一定条件下,发生可逆反应: , 下列各项中能说明该反应已经达到平衡状态的是( )A、一定条件下,体系的密度不再改变 B、一定条件下,和转化率相同 C、断裂1 mol 键的同时,也断裂6 mol 键 D、反应消耗的、与生成的的速率
-
18、短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素,Y原子的最外层有2个电子,Z的单质晶体是应用最广泛的半导体材料,W与X位于同一主族。下列说法正确的是( )A、原子半径: B、Z的最高价氧化物对应水化物的酸性比W的弱 C、由X、Z组成的化合物是离子化合物 D、由X、W组成的化合物都能使品红溶液褪色
-
19、微生物燃料电池能将污水中的乙二胺()氧化成环境友好的物质,示意图如图所示,a、b均为石墨电极。下列说法正确的是( )
 A、燃料电池是将化学能转化为热能的装置 B、电池工作时电流方向是b→a→质子交换膜→b C、电池工作时,乙二胺在a电极得到电子 D、b电极的电极反应为
A、燃料电池是将化学能转化为热能的装置 B、电池工作时电流方向是b→a→质子交换膜→b C、电池工作时,乙二胺在a电极得到电子 D、b电极的电极反应为 -
20、室温下,下列各组离子在指定溶液中一定能大量共存的是( )A、0.1 mol⋅L 的溶液:、、、 B、0.1 mol⋅L 的溶液:、、、 C、0.1 mol⋅L 的溶液:、、、 D、0.1 mol⋅L 的溶液:、、、