-
1、生物质X(
 )与Y(
)与Y( )同时反应如下:
)同时反应如下:反应Ⅰ:(
 )
)反应Ⅱ:(
 ) , 反应历程如图,下列说法不正确的是
) , 反应历程如图,下列说法不正确的是 A、 B、相同条件下,反应Ⅰ更快达到平衡 C、降低温度,的平衡物质的量分数增大 D、升高温度,反应Ⅰ、Ⅱ的反应速率都增大
A、 B、相同条件下,反应Ⅰ更快达到平衡 C、降低温度,的平衡物质的量分数增大 D、升高温度,反应Ⅰ、Ⅱ的反应速率都增大 -
2、用如图装置分别进行两个实验:①先注入 , 再打开止水夹;②先打开止水夹 , 再将中水注入烧瓶。下列说法正确的是
 A、实验室可以加热直接制取 B、实验②观察到烧瓶中产生红色的“喷泉” C、实验①先产生白雾,然后观察到喷泉现象 D、实验①后烧瓶中一定存在
A、实验室可以加热直接制取 B、实验②观察到烧瓶中产生红色的“喷泉” C、实验①先产生白雾,然后观察到喷泉现象 D、实验①后烧瓶中一定存在 -
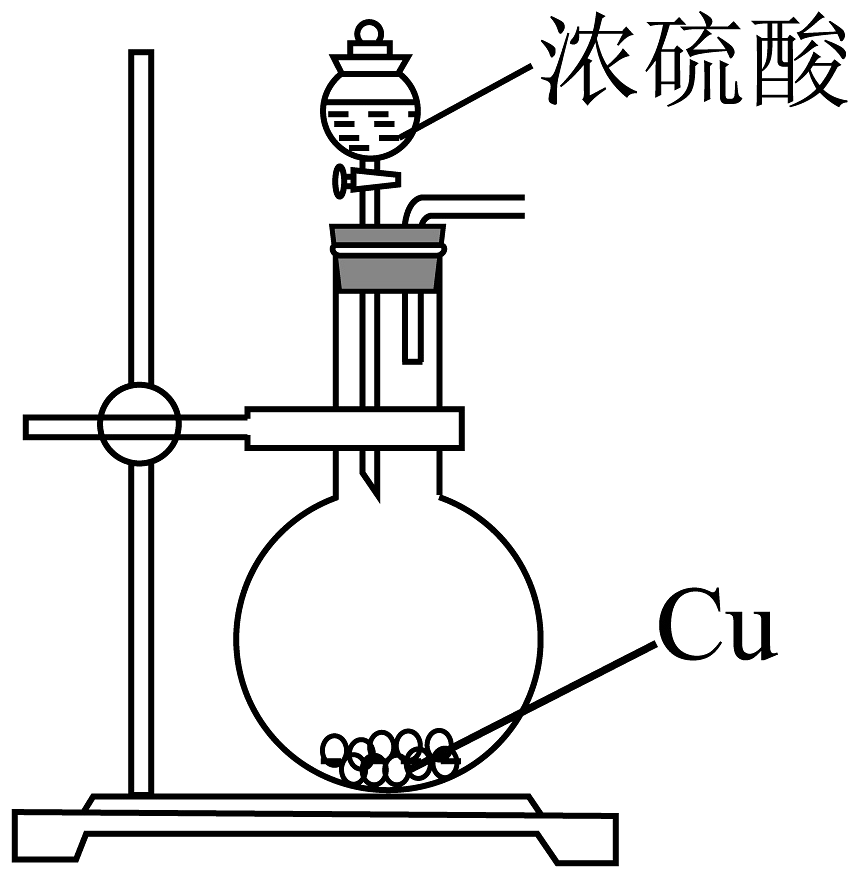
3、探究蔗糖与浓硫酸反应及气体产物的性质,设计如图所示实验,下列说法正确的是
 A、蔗糖变为黑色,说明浓硫酸有强氧化性 B、品红和酸性溶液褪色原理相同 C、石蕊变红,说明气体产物溶于水有酸性 D、澄清石灰水变浑浊,气体产物一定含
A、蔗糖变为黑色,说明浓硫酸有强氧化性 B、品红和酸性溶液褪色原理相同 C、石蕊变红,说明气体产物溶于水有酸性 D、澄清石灰水变浑浊,气体产物一定含 -
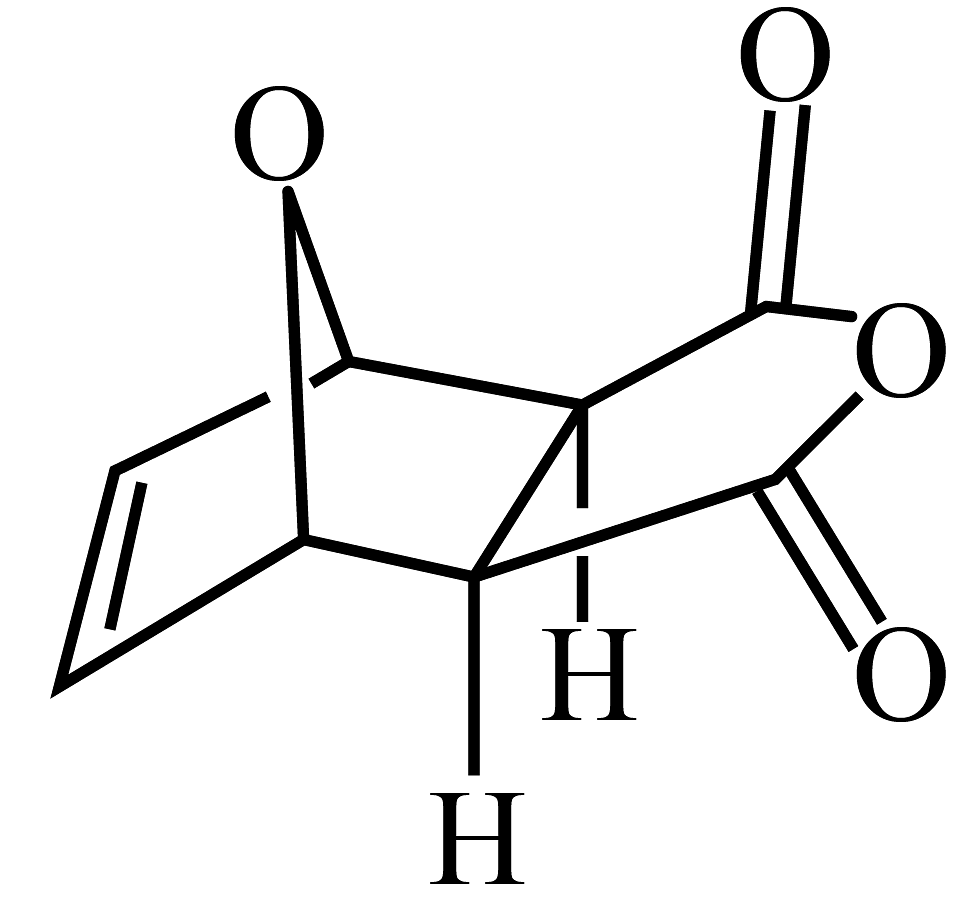
4、MMA结构简式如图所示,可用于合成有机玻璃聚甲基丙烯酸甲酯(PMMA)。有关MMA说法正确的是
 A、是PMMA的链节 B、所有碳原子一定共平面 C、能发生加成、水解和消去反应 D、能使溴水和酸性溶液褪色
A、是PMMA的链节 B、所有碳原子一定共平面 C、能发生加成、水解和消去反应 D、能使溴水和酸性溶液褪色 -
5、2022年我国十大科技突破——海水直接电解制 , 其工作原理如图,防水透气膜只能水分子通过。下列说法正确的是
 A、a为电解池的阴极 B、b的电极反应方程式: C、去除透气膜,a极发生的电极反应不变 D、电解池工作时,海水侧的离子浓度理论上逐渐减小
A、a为电解池的阴极 B、b的电极反应方程式: C、去除透气膜,a极发生的电极反应不变 D、电解池工作时,海水侧的离子浓度理论上逐渐减小 -
6、一种新型离子液体溶剂结构简式如图所示。下列说法正确的是
 A、电负性: B、离子液体中存在离子键 C、的空间构型为平面四边形 D、该离子液体中的所有元素都分布在区
A、电负性: B、离子液体中存在离子键 C、的空间构型为平面四边形 D、该离子液体中的所有元素都分布在区 -
7、下列装置按制备、收集、验证漂白性及尾气处理的顺序进行实验(“→”表示气流方向),能达到实验目的的是A、
 B、
B、 C、
C、 D、
D、
-
8、非物质文化遗产是中华优秀传统文化的重要组成部分。下列广东的非遗项目中涉及的主要物质由硅酸盐材料制成的是




A.粤绣
B.西关打铜
C.石湾陶塑
D.潮州木雕
A、A B、B C、C D、D -
9、环丙叉环丙烷(b)由于其特殊的结构,一直受到结构和理论化学家的注意,根据其转化关系,下列说法正确的是
 A、m的同分异构体中属于芳香族化合物的共有5种 B、p在氢氧化钠的乙醇溶液中加热生成烯烃 C、反应①是加成反应,反应②是消去反应 D、b的所有原子都在同一个平面内
A、m的同分异构体中属于芳香族化合物的共有5种 B、p在氢氧化钠的乙醇溶液中加热生成烯烃 C、反应①是加成反应,反应②是消去反应 D、b的所有原子都在同一个平面内 -
10、电催化氮气制备铵盐和硝酸盐的原理如图所示。下列说法正确的是
 A、a极反应式为N2+12OH--10e-=2NO+6H2O B、电解一段时间,a、b两电极区的pH均减小 C、电解过程中H+从a极通过质子交换膜转移至b极 D、相同时间内,a、b两极消耗N2的物质的量之比为5∶3
A、a极反应式为N2+12OH--10e-=2NO+6H2O B、电解一段时间,a、b两电极区的pH均减小 C、电解过程中H+从a极通过质子交换膜转移至b极 D、相同时间内,a、b两极消耗N2的物质的量之比为5∶3 -
11、标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知和的相对能量为0],下列说法不正确的是
 A、 B、可计算键能为 C、相同条件下,的平衡转化率:历程Ⅱ>历程Ⅰ D、历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
A、 B、可计算键能为 C、相同条件下,的平衡转化率:历程Ⅱ>历程Ⅰ D、历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为: -
12、在澄清透明的溶液中,能够大量共存的离子组是A、、、、 B、、、、 C、、、、 D、、、、
-
13、反应 , 在温度为T1、T2时,平衡体系中的体积分数随压强变化曲线如图所示。下列说法正确的是
 A、A、C两点的反应速率:A>C B、A、C两点气体的颜色:A深,C浅 C、A、C两点气体的平均相对分子质量:A>C D、由状态B到状态A,可以采用升温的方法
A、A、C两点的反应速率:A>C B、A、C两点气体的颜色:A深,C浅 C、A、C两点气体的平均相对分子质量:A>C D、由状态B到状态A,可以采用升温的方法 -
14、下列与实验有关的图标对应不正确的是A、护目镜
 B、用电
B、用电 C、明火
C、明火 D、洗手
D、洗手
-
15、据文献报道,我国学者提出O2氧化HBr生成Br2反应历程如图所示。下列有关该历程的说法错误的是
 A、O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O B、中间体HOOBr和HOBr中Br的化合价相同 C、发生步骤②时,断裂的化学键既有极性键又有非极性键 D、步骤③中,每生成1molBr2转移2mol电子
A、O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O B、中间体HOOBr和HOBr中Br的化合价相同 C、发生步骤②时,断裂的化学键既有极性键又有非极性键 D、步骤③中,每生成1molBr2转移2mol电子 -
16、在化学分析中,以标准溶液滴定溶液中的时,采用为指示剂。一定温度下,AgCl和的沉淀溶解平衡曲线如图所示。下列说法不正确的是
 A、滴定时先产生AgCl沉淀 B、利用与反应生成砖红色沉淀指示滴定终点 C、图中a点条件下既不能生成AgCl沉淀,也不能生成沉淀 D、图中b点时, ,
A、滴定时先产生AgCl沉淀 B、利用与反应生成砖红色沉淀指示滴定终点 C、图中a点条件下既不能生成AgCl沉淀,也不能生成沉淀 D、图中b点时, , -
17、二氯异氰尿酸钠(
 ,简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冷水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。
,简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冷水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。

已知:实验室常用高浓度的NaClO溶液和氰尿酸溶液在10℃时反应制备DCCNa,主要发生反应:
 (氰尿酸)
(氰尿酸) (1)、和中大小:-NH2(填“>”“<”或“=”)。(2)、A装置中盛装X试剂的仪器名称是;D中软导管的作用是。(3)、请选择合适的装置,按气流从左至右方向组装,则导管连接顺序为(填小写字母)。(4)、X试剂为饱和氢氧化钠溶液。当装置A内出现现象时,打开装置A的活塞加入(氰尿酸)溶液,在反应过程中仍不断通入的目的是。(5)、实验过程中A的温度必须保持为7℃~12℃,pH值控制在6.5~8.5的范围,则该实验的控温方式是。若温度过高,pH过低,会生成和等,写出该反应的化学方程式。
(1)、和中大小:-NH2(填“>”“<”或“=”)。(2)、A装置中盛装X试剂的仪器名称是;D中软导管的作用是。(3)、请选择合适的装置,按气流从左至右方向组装,则导管连接顺序为(填小写字母)。(4)、X试剂为饱和氢氧化钠溶液。当装置A内出现现象时,打开装置A的活塞加入(氰尿酸)溶液,在反应过程中仍不断通入的目的是。(5)、实验过程中A的温度必须保持为7℃~12℃,pH值控制在6.5~8.5的范围,则该实验的控温方式是。若温度过高,pH过低,会生成和等,写出该反应的化学方程式。 -
18、下列各组离子中,能在溶液里大量共存的是A、 B、 C、 D、
-
19、下列实验方案不能达到实验目的的是
A.检验乙醇与浓硫酸共热生成乙烯
B.检验1-溴丁烷发生消去反应生成丁烯


C.验证乙酸、碳酸、苯酚的酸性强弱
D.检验电石与水反应生成乙炔

 A、A B、B C、C D、D
A、A B、B C、C D、D -
20、某研究小组以甲苯为起始原料,按下列路线合成有机光电材料中间体K。

已知:①R-BrR-CNR-COOH;
②R-CHO+CH3CHOR-CH=CHCHO。
请回答:
(1)、反应Ⅰ所需试剂和反应条件分别是、。化合物M的结构简式是。(2)、下列说法不正确的是___________。A、化合物D分子中所有原子可能共平面 B、化合物E与苯甲酸互为同系物 C、E→F、G→J的反应类型分别为加成反应、取代反应 D、化合物N可由环戊二烯与乙烯经加成反应制得(3)、反应F→G第①步反应的化学方程式是。(4)、写出同时符合下列条件的化合物E的同分异构体的结构简式。①分子中含有苯环;遇氯化铁溶液显紫色;
②1H−NMR谱表明分子中有5种化学环境不同的氢原子;IR谱显示存在碳氧双键、碳碳双键。
(5)、设计以HCHO、CH3CHO为原料合成的合成 路线(用流程图表示,其它无机试剂任选)。
路线(用流程图表示,其它无机试剂任选)。