-
1、化学与生活密切相关,下列说法不正确的是( )A、单晶硅是一种半导体材料,可用于制造硅电池 B、食品包装袋中常用的干燥剂有生石灰、还原铁粉、硅胶等 C、过氧化钠能与二氧化碳反应,可作潜水艇中的供氧剂 D、84消毒液是以为有效成分的消毒液,与白醋混合可以提升消毒效果
-
2、下列离子在给定条件下能大量共存的是( )A、澄清透明的溶液中: B、无色酚酞试液呈红色的溶液中: C、溶液中: D、含的溶液中:
-
3、下列有关说法不正确的是( )A、溶于水中既破坏了离子键又破坏了共价键 B、溶液都能导电,说明它们都是离子化合物 C、由于冰中水分子间以氢键结合排列成规则的晶体,所以冰的密度比水小 D、分子中各原子都满足8电子稳定结构
-
4、下列说法正确的是( )A、富勒烯与金刚石的物理性质相同 B、在一定条件下发生化学反应生成 C、与互为同素异形体 D、互为同位素
-
5、下列化学用语表示不正确的是( )A、电子式:
 B、中子数为10的氧原子:
C、镁原子的结构示意图:
B、中子数为10的氧原子:
C、镁原子的结构示意图: D、的球棍模型:
D、的球棍模型:
-
6、常温下,关于反应 , 下列说法正确的是( )A、该反应的还原产物是 B、每生成 , 反应共转移电子 C、氧化剂与还原剂的物质的量之比为 D、该反应体现了单质的氧化性
-
7、下列物质对应的化学式不正确的是( )A、漂粉精: B、苏打: C、重晶石: D、金刚砂:C
-
8、磁流体是电子材料的新秀,在一定条件下,将含等物质的量的和的溶液混合,再滴入稍过量的溶液,可得到一种黑色磁流体(其中分散质有 , 分散质粒子大小在之间)。下列说法中不正确的是( )A、用一束光照射该磁流体能产生丁达尔效应,是区分其他分散系的本质原因 B、该过程发生了非氧化还原反应 C、所得的黑色磁流体是混合物 D、黑色磁流体能与盐酸发生反应
-
9、下列物质中,属于电解质且能导电的是( )A、固体 B、溶液 C、熔融 D、
-
10、下列实验仪器的名称不正确的是( )A、
 坩埚
B、
坩埚
B、 分液漏斗
C、
分液漏斗
C、 泥三角
D、
泥三角
D、 球形干燥管
球形干燥管
-
11、下列物质既不属于酸性氧化物,也不属于碱性氧化物的是( )A、 B、 C、 D、
-
12、丙烯是有机化工中的重要原料,可用丙烷直接脱氢工艺和丙烷氧化脱氢工艺制备,其主反应和有关物质的燃烧热数据如下。
Ⅰ.丙烷直接脱氢工艺:
Ⅱ.丙烷氧化脱氢工艺:
物质
燃烧热
-2219.9
-2058.0
-285.8
回答下列问题:
(1)、反应Ⅰ的 , 其自发进行的条件是。丙烷在不同温度下按照一定流速通过铬催化剂反应相同时间,所得混合物中部分物质的体积分数如下表所示,实际控制温度为580℃,原因是。510℃
550℃
580℃
620℃
丙烷(%)
64.82
57.87
37.76
31.91
丙烯(%)
12.33
1585
22.72
23.13
乙烯(%)
0.12
0.19
0.20
0.71
甲烷(%)
1.50
2.78
4.03
7.31
氢气(%)
20.47
18.99
25.45
31.14
(2)、①反应Ⅱ属于自由基反应,其反应历程如下,写出第iv步的反应方程式。i)
ii)
iii)
iv)。
(3)、将、置于某恒温(高于100℃)、恒压(p)的密闭容器中进行反应Ⅱ时,发生了副反应Ⅲ:。达平衡时的体积分数 , , 则的选择性为(的选择性 , 计算结果保留3位有效数字),反应Ⅲ的(用平衡分压代替平衡浓度计算,分压=总压物质的量分数)。(4)、使用惰性电极电解的酸性溶液制丙烯,其装置如下图所示。
①若以铅酸蓄电池作为直流电源,其工作时负极质量(填“增大”“减小”或“不变”)。
②X电极的电极反应式为。
-
13、文拉法辛(化合物G)是一种用于治疗各类抑郁症的药物,其合成路线如下图所示:

回答下列问题:
(1)、A的化学名称是。(2)、C→D的反应类型是。(3)、E中手性碳原子有个。(4)、F中官能团的名称为。(5)、C发生消去反应生成的烯烃被足量酸性溶液氧化后的产物是和(写结构简式)。(6)、B的同分异构体中,同时满足下列条件的共有种。a.能发生银镜反应
b.遇溶液显紫色
(7)、以丙酮、、甲醛和甲酸为含碳原料,合成化合物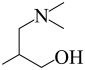 。基于你设计的合成路线,相关步骤涉及到氢气参与反应,其化学方程式为。
。基于你设计的合成路线,相关步骤涉及到氢气参与反应,其化学方程式为。 -
14、乙酰水杨酸(俗称阿司匹林),是常用的解热镇痛药。实验室选择草酸绿色催化剂制备阿司匹林。
【实验原理】
主反应:

副反应:

名词
熔点/℃
溶解性
水杨酸
157~159
溶于水和乙醇
乙酸酐
-73.1
易水解
乙酰水杨酸
135
微溶冷水,可溶热水,易溶于乙醇
【实验流程】

回答下列问题:
(1)、制备过程中采用的合适加热方式是。(2)、“加冷水”后,发生反应的化学方程式为。(3)、“操作2”中加入饱和溶液的目的是。(4)、“操作3”中缓慢加入过量18%的盐酸,充分搅拌直至(填现象变化),再冷却结晶。(5)、为检验所获得的产品中是否含有水杨酸,可选用的试剂为。(6)、为提高产品的产率,下列装置可能会用到的有。 (7)、用分光光度法测定阿司匹林粗产品的纯度。现测得阿司匹林标准溶液的吸光度A与其浓度关系如下图所示。
(7)、用分光光度法测定阿司匹林粗产品的纯度。现测得阿司匹林标准溶液的吸光度A与其浓度关系如下图所示。
准确称取16.0mg实验产品,用乙醇溶解并定容至100mL,测得溶液吸光度 , 则该产品的纯度是(以质量分数表示)。
-
15、某制药厂的废钯催化剂含、、、、和活性炭,提取贵金属的流程如下:

已知:①铂系元素(包括Pt、Pd等六种元素)的单质均为惰性金属;
②性质较稳定,难溶于酸、碱,可溶于王水;
③、。
回答下列问题:
(1)、“焙烧”步骤的主要目的是除去活性炭,通常控制温度600℃、焙烧时间约 , 焙烧温度过高或时间过长均导致钯浸出率降低,原因是。(2)、“浸渣”的成分是少量及。(3)、“浸出”步骤中生成配合物 , 写出该反应的化学方程式。(4)、“氨化”步骤中转化为 , 反应后溶液 , 此时溶液中。(5)、“沉钯”步骤中的离子方程式为。(6)、存在两种平面结构,将其记为A和B。查得25℃时A、B在水中的溶解度分别为0.2577g、0.0366g,A具有广谱的抗癌活性,写出A的结构式(中共价键不必画出)。 -
16、菠萝“扎嘴”的原因之一是菠萝中含有一种难溶于水的草酸钙针晶。常温下,草酸钙在不同下体系中与关系如图所示(代表),已知。下列有关说法正确的是( )
 A、数量级为 B、溶液时, C、时,曲线①呈上升趋势的原因是部分转化为 D、点时,体系中
A、数量级为 B、溶液时, C、时,曲线①呈上升趋势的原因是部分转化为 D、点时,体系中 -
17、为了保护环境、充分利用铅资源,科学家设计了如下的-铅化合物燃料电池实现铅单质的回收。

下列有关说法错误的是( )
A、正极区溶液pH升高,负极区溶液pH降低 B、电子流向:电极b→负载→电极a C、阴极区电极反应式为 D、为了提高的回收率,离子交换膜为阴离子交换膜 -
18、一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示(晶胞边长为apm,晶胞高为cpm,为阿伏加德罗常数的值)。

下列说法正确的是( )
A、该物质的化学式为 B、硼原子间最近距离为 C、的配位数为12 D、该物质的摩尔体积为 -
19、(可表示为)催化剂的催化原理如下图所示(为烃基)。
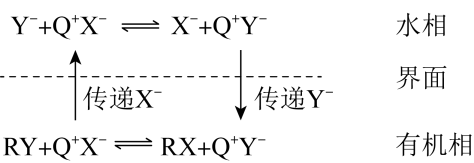
下列说法错误的是( )
A、总反应为: B、易溶于水相而难溶于有机相 C、与、之间的离子键强度要适中 D、PTC催化剂可用作相转移倠化剂 -
20、下列实验方法或操作能达到实验目的的是( )
实验目的
实验方法或操作
A.
在水溶液中存在
向的溶液中加入浓溶液,振荡试管,观察颜色变化
B.
检验中的碳碳双键
取样,加入适量酸性高锰酸钾溶液后观察是否褪色
C.
比较与
常温,测浓度均为的和溶液的
D.
比较Mg和Al的金属性强弱
向浓度均为和溶液中滴加浓氨水至过量
A、A B、B C、C D、D