-
1、组氨酸(
 )能溶于水,在医药上用于治疗胃溃疡、贫血、过敏症等。将组氨酸简写成 , 向组氨酸盐(H3ACl2)溶液中逐滴加入等浓度溶液,溶液的随碱液量有如图所示变化,已知pK=-lgK(K为的电离平衡常数)。下列说法错误的是( )
)能溶于水,在医药上用于治疗胃溃疡、贫血、过敏症等。将组氨酸简写成 , 向组氨酸盐(H3ACl2)溶液中逐滴加入等浓度溶液,溶液的随碱液量有如图所示变化,已知pK=-lgK(K为的电离平衡常数)。下列说法错误的是( ) A、时, B、时, C、 D、组氨酸盐水溶液中:
A、时, B、时, C、 D、组氨酸盐水溶液中: -
2、氯化亚铜(CuCl)难溶于醇和水,在潮湿空气中易水解氧化,广泛应用于冶金工业,以铜为原料生产的流程如下:

下列有关叙述错误的是( )
A、“溶解”时可能发生的反应: B、“还原”反应的氧化产物是或 C、“操作X”是过滤 D、“洗涤”时先用硝酸洗,再用乙醇洗 -
3、某有机物在合成中具有重要作用,其分子结构如下图所示。是核电荷数依次增大的短周期元素。原子序数之和等于Y的原子序数,原子价电子数相同。下列说法错误的是( )
 A、元素的氢化物沸点最高的是Z B、元素电负性最大的是Z C、Q的最高价氧化物是酸性氧化物 D、该有机物具有碱性
A、元素的氢化物沸点最高的是Z B、元素电负性最大的是Z C、Q的最高价氧化物是酸性氧化物 D、该有机物具有碱性 -
4、一种热再生氨基液流电池的工作原理如图所示,下列有关说法错误的是( )
 A、a为阴离子交换膜 B、放电时负极反应为 C、为保证电池的循环使用需不断更换新的负极金属板 D、热解的离子方程式为
A、a为阴离子交换膜 B、放电时负极反应为 C、为保证电池的循环使用需不断更换新的负极金属板 D、热解的离子方程式为 -
5、某实验探究小组设计完成了如图实验,下列有关说法正确的是( )
 A、i中深蓝色溶液中只存在[Cu(NH3)4]2+ B、ii中生成黑色沉淀说明仅Cu2+转化为CuS C、iii中蓝色沉淀为[Cu(NH3)4]SO4·H2O D、iv中反应为[Cu(NH3)4]2++2OH-=Cu(OH)2↓+4NH3↑
A、i中深蓝色溶液中只存在[Cu(NH3)4]2+ B、ii中生成黑色沉淀说明仅Cu2+转化为CuS C、iii中蓝色沉淀为[Cu(NH3)4]SO4·H2O D、iv中反应为[Cu(NH3)4]2++2OH-=Cu(OH)2↓+4NH3↑ -
6、饮用水中的对人类健康会产生危害,为了降低饮用水中的浓度,可以在碱性条件下用铝粉将还原为 , 反应的离子方程式为。设为阿伏加德罗常数的值,下列说法错误的是( )A、消耗 , 反应转移的电子数为 B、消耗时,溶液中增加的数目为 C、标准状况下,中含键数目为 D、液态水中含有的氢键数目少于
-
7、六方硫化锌的结构是S原子作六方最密堆积,其晶胞如图所示,图中A点分数坐标为点分数坐标为;底 , 高。设为阿伏加德罗常数的值。下列说法错误的是( )
 A、晶胞中,填充空隙类型为正四面体空隙 B、图中S原子的配位数为6 C、图中的核间距约为 D、该晶体的化学式为
A、晶胞中,填充空隙类型为正四面体空隙 B、图中S原子的配位数为6 C、图中的核间距约为 D、该晶体的化学式为 -
8、下列离子方程式书写正确的是( )A、用高锰酸钾溶液滴定草酸: B、电解饱和食盐水: C、向溶液中加入足量稀硝酸: D、将足量通入溶液中:
-
9、Knoevenagel反应是指羰基化合物和活泼亚甲基化合物在弱碱性胺催化下缩合制备a,β—不饱和羰基化合物的反应。某Knoevenagel反应如下,有关说法正确的是( )
 A、A具有手性 B、若B的分子量为132,则R表示乙基 C、在一定条件下,C能发生水解反应 D、D的分子式为H2O2
A、A具有手性 B、若B的分子量为132,则R表示乙基 C、在一定条件下,C能发生水解反应 D、D的分子式为H2O2 -
10、用下列装置(夹持与加热装置已略去)进行实验,不能达到实验目的的是( )
A
B
C
D
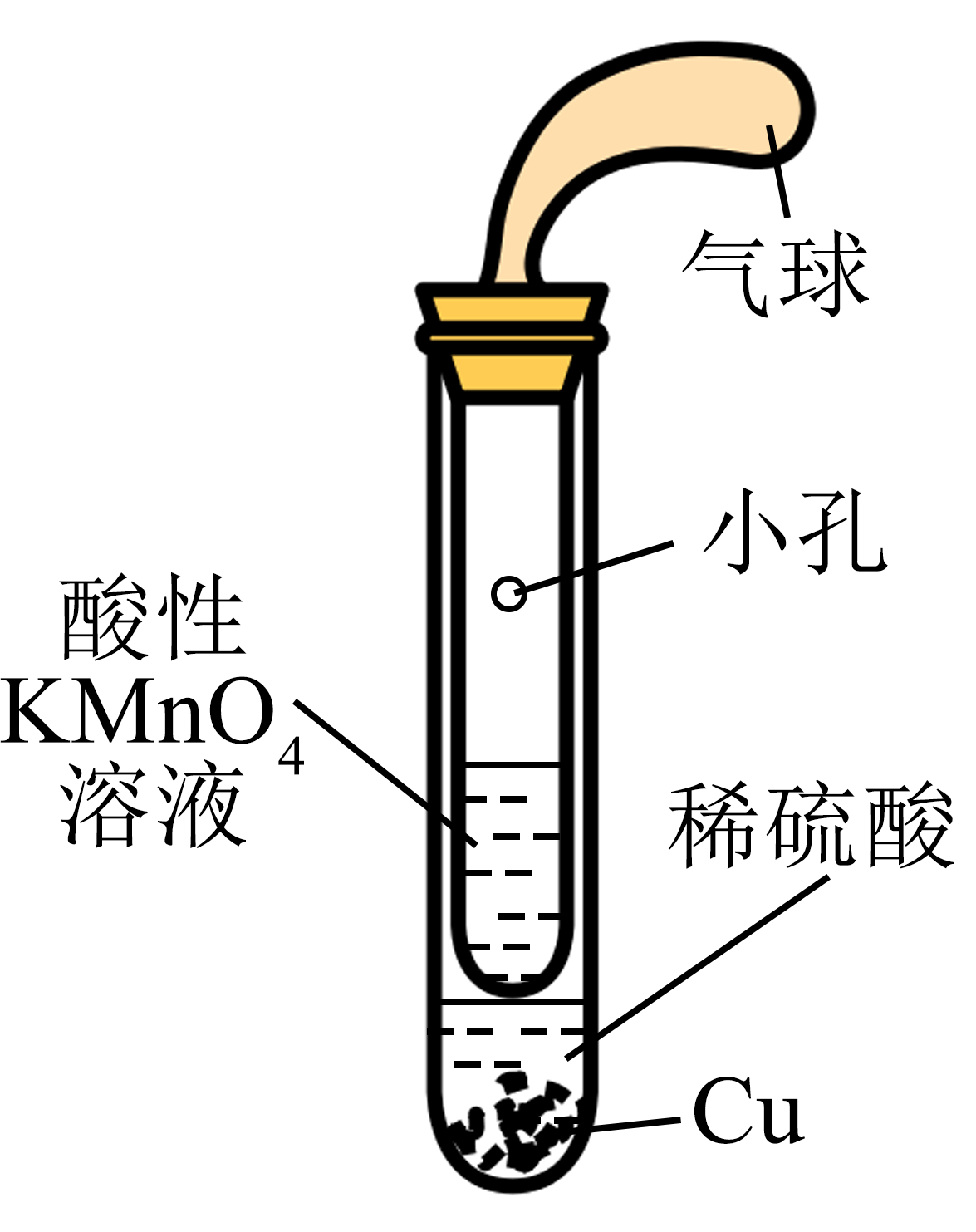



制取SO2 , 并验证其还原性
从茶叶中提取咖啡因
制备Cl2
制备苯甲酸乙酯
A、A B、B C、C D、D -
11、与在一定条件下反应可生成两种单质,在生命活动中也可生成亚硝基硫醇(HSNO)。下列有关说法错误的是( )A、NO为极性分子 B、H2S的VSEPR模型为三角锥形 C、HSNO的结构式为 D、NO与H2S反应生成的两种单质为S、N2
-
12、出土的文物竹简需经历浸泡释污、脱水加固、干燥定形、粘接修复等步骤。文物竹简中的被氧化为后,会与竹材中的木质素(多酚类物质)发生络合反应而变黑,变色竹简需用溶液、乙二胺四乙酸和草酸的混合试剂进行脱色处理,最后再经过蒸馏水清洗,即可恢复原色。下列说法错误的是( )A、纤维素水解的最终产物为果糖 B、还原性较强,起到还原作用 C、脱色过程中,乙二胺四乙酸和草酸主要作配位剂 D、维生素C也可用于竹简脱色
-
13、反应可用于制备火箭推进剂的燃料。下列化学用语表示正确的是( )A、中N为杂化 B、的电子式为
 C、溶液俗称漂白液
D、食盐的分子式为
C、溶液俗称漂白液
D、食盐的分子式为
-
14、2023年诺贝尔化学奖颁发给MoungiG.Bawendi、LouisE.Brus和AlexeyI.Ekimov,以表彰他们在发现和合成量子点方面的贡献。量子点是非常微小的纳米粒子,它们的大小决定了其性质。在20世纪80年代初,AlexeyI.Ekimov成功地在有色玻璃中创造出依赖于尺寸的量子效应,玻璃颜色来自氯化铜纳米颗粒。下列有关说法错误的是( )A、普通玻璃属于晶体 B、分散在玻璃中的氯化铜纳米微小颗粒就是量子点 C、纳米颗粒越小,吸附能力越强 D、氯化铜纳米颗粒的大小决定添加该颗粒的玻璃颜色
-
15、高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,同时在化工制备和电池材料等方面具有广泛的应用前景。某实验小组制备高铁酸钾并探究其性质。

资料:K2FeO4可溶于水、微溶于浓KOH溶液,具有强氧化性,在碱性溶液中较稳定;在酸性或中性溶液中快速产生O2。
(1)、 K2FeO4中铁元素的化合价。(2)、装置B中的试剂为 , 作用。(3)、装置C中制备K2FeO4时,发生反应的化学方程式为 , 每得到1mol K2FeO4 , 理论上消耗Cl2的物质的量为mol。(4)、高铁酸钾与水反应其中一种产物为Fe(OH)3 (胶体),则离子方程式为 , 高铁酸钾作为水处理剂起到的作用是。(5)、制备 K2FeO4可以采用干式氧化法,初始反应为 , 该反应中每消耗6molNa2O2时转移电子数为。 -
16、下表列出了九种元素在周期表中的位置:
周期
族
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
2
a
b
3
c
d
e
f
g
h
4
i
请回答下列问题:
(1)、i元素与h元素形成化合物的电子式是 , 高温灼烧该化合物时,火焰呈色。(2)、b、c、g三种元素的简单离子半径由大到小的顺序是(填离子符号);b、f、g三种元素对应简单氢化物的热稳定性由强到弱的顺序是(填化学式)。(3)、元素的单质与氢氧化钠溶液反应的离子方程式为。(4)、c元素氢化物与发生反应的化学方程式为 , 所得溶液的7.(5)、由a、h组成的一种化合物,分子中a、h原子最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,该化合物的结构式为。 -
17、我国科学家侯德榜发明了联合制碱法。以氯化钠、氨及二氧化碳为原料,同时生产纯碱和氯化铵两种产品,又称“侯氏制碱法”,对世界制碱工业作出了卓越贡献。根据要求回答下列问题:(1)、I、用纯净的碳酸钠固体配制溶液。
用托盘天平称取固体的质量是(2)、本实验中需要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和。(3)、下列说法中,正确的是____(填字母)。A、定容时仰视刻度线,会导致配制的溶液浓度偏小 B、定容时如果加水超过刻度线,要用滴管吸出 C、摇匀后发现凹液面下降,再加水至刻度线 D、转移时溶液倒出容量瓶外,要重新配制溶液(4)、II、生成纯碱的流程如下:
工业生成纯碱的第一步是除去饱和食盐水中的、、 , 依次加入的试剂是 、 、 、过滤、 。备用的除杂试剂有:①足量溶液;②足量溶液;③适量稀盐酸;④足量的溶液。则正确的试剂添加顺序(填字母)。
A、①②③④ B、②①④③ C、②④①③ D、④②①③(5)、已知:溶解度(20℃)
36.0
21.7
9.6
37.2
写出装置I中反应的化学方程式:。
(6)、制出的纯碱中只含有杂质 , 下列实验方案中,不能测定出混合物中质量分数的是____(填字母)。A、取混合物充分加热,质量减少 B、取混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到固体 C、取混合物与足量溶液充分反应,沉淀经过滤、洗涤、干燥得到固体 D、取混合物与足量稀盐酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加(7)、将碳酸钠和碳酸氢钠的混合物 , 加热到质量不再变化时,剩余物质的质量 , 则混合物中碳酸钠的质量分数(精确到0.1)。 -
18、掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质,是了解电解质的性质、研究离子反应的前提。
有以下十种物质:①Cl2②C2H5OH ③Fe(OH)3胶体 ④盐酸 ⑤FeSO4 ⑥K2Cr2O7 ⑦Ca(HCO3)2⑧NaOH ⑨CO2 ⑩Na2CO3。请按要求填空。
(1)、属于电解质的是 , 属于非电解质的是(填序号)。(2)、制备③的化学方程式。(3)、向⑤溶液中滴入⑧溶液的实验现象为。(4)、向④中滴入少量⑩溶液的离子方程式为。(5)、⑦的溶液中加入过量的NaOH溶液的离子方程式为。 -
19、有一质量为11.76g的Fe、CuO、Fe2O3混合固体,完全溶解在200mL2mol/L稀盐酸中,然后向溶液中加铁粉,剩余固体质量与加入铁粉质量的关系如图所示。下列说法正确的是( )
 A、0~m1阶段发生反应为Fe+2H+=Fe2++H2↑ B、混合固体中的质量为0.01mol C、5.04~m2阶段发生反应为2Fe3++Fe=3Fe2+ D、图中m2=5.6
A、0~m1阶段发生反应为Fe+2H+=Fe2++H2↑ B、混合固体中的质量为0.01mol C、5.04~m2阶段发生反应为2Fe3++Fe=3Fe2+ D、图中m2=5.6 -
20、A、B、C、X均为中学常见的物质,它们之间有如下转化关系(其它产物已略去):。下列说法错误的是( )A、若是 , 则可能是 B、若是 , 则可能是 C、若是金属单质,则、中的化合价可能是 D、若是 , 则与可能反应生成