相关试卷
-
1、下图是某药厂生产补钙剂的商品标签图。
XXX儿童咀嚼片(60片装)
【主要成分】:碳酸钙、维生素
【功效】:补钙
【功效】:2.0g/片、每片中含:碳酸钙1g、维生素D:100IU
【食用方法】:嚼食、每日一片
碳酸钙的化学式为CaCO3 , 请你根据以上标标签信息完成下列计算:
(1)、补钙剂中的钙指的是(填“原子”或“元素”)。(2)、碳酸钙的相对分子质量为。(3)、每片药剂中含钙元素的质量为多少。(写出计算过程)。 -
2、“糖醋鲤鱼”是一道传统名菜,其亨饪过程中用到了黄酒食醋。黄酒中的乙醇与食醋中的乙酸发生反应生成乙酸乙酯(C4H8O2),使亨饪出的菜品别具香味。(1)、乙酸乙酯由种元素组成。(2)、乙酸乙酯中H、O两种元素的质量比为(填最简整数比)。
-
3、
空气是一种宝贵的资源,其中含有多种气体。某化学兴趣小组的同学对此产生了浓厚的兴趣,他们对空气的组成成分及其用途、制取保护等展开了探究。
【任务一】空气的组成分及用途
(1)空气成分中含量最高且常用作保护气的是。
【任务二】空气中氧气含量的测定
实验课上,老师利用传感器技术完成了空气中氧气含量测定的实验,并实时测定了实验装置(如图1)内的压强、温度和氧气浓度三条曲线变化趋势如图2所示。

(2)红磷燃烧的符号表达式为 , 该实验中红磷必须足量的目的是;解释该实验的测定原理是。
(3)如图2所示Y曲线表示的是(填“温度”或“氧气浓度”)。
(4)实验中测得的数据如下:
测量项目
实验前
实验后
烧杯中水的体积
烧杯中剩余水的体积
瓶中剩余气体的体积
体积/mL
80.0
61.0
81.0
根据实验数据计算:测得的空气中氧气的体积分数为。
【拓展延伸】
最志衣的殚公会
“温控保鲜”和“气调保鲜”是两类食品保鲜技术。它们通过降低温度和改变气体成分,达到抑制储藏物细胞呼吸的目的。如图所示是工业上用膜分离技术实现“气调保鲜”的流程。

(5)冰箱中常用的是“气调保鲜”,在空气分离后。进入冰箱保鲜室内的气体是(填“富氧空气”或“富氮空气)。
-
4、根据下图所示,按要求回答问题:
 (1)、写出图中带有标号仪器的名称:a , b。(2)、图G实验的目的 , 手握试管一段时间后,导管口有气泡产生的主要原因是。
(1)、写出图中带有标号仪器的名称:a , b。(2)、图G实验的目的 , 手握试管一段时间后,导管口有气泡产生的主要原因是。A.分子间隔变大 B.分子体积变大 C.分子个数变多
(3)、若用高锰酸钾制氧气制取氧气,选择的发生装置(填序号),该反应的符号表达式为 , 检验氧气的方法是;选择装置D收集氧气,因为氧气具有的物理性质是。(4)、实验室用过氧化氢溶液分解制氧气,可选择的发生装置是(填序号),反应的符号表达式是;该反应的基本类型为。(5)、实验室加热高锰酸钾制取氧气的主要步骤如下,正确的顺序是。①装入药品,开始加热 ②停止加热 ③收集气体 ④组装仪器,检查气密性
-
5、
航天员在太空生活需要氧气和水。氧气和水的相互转化,体现了“合”与“分”的思想。兴趣小组追寻科学家的足迹,对水进行探究。
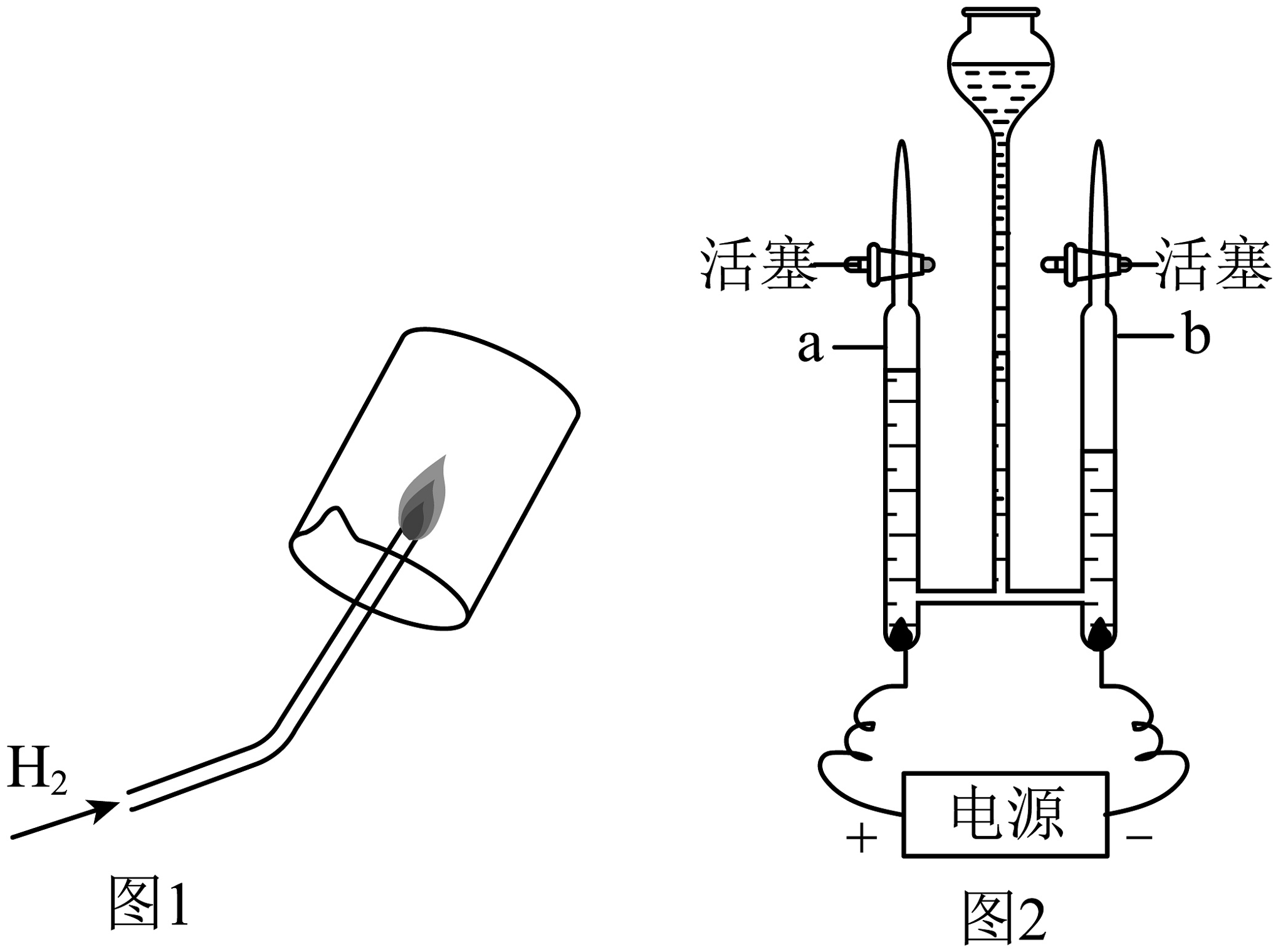
【宏观辨识】根据实验探究水的组成
(1)“合”的思想:液氢和液氧反应产生的能量可为返回舱返回提供动力,该反应的符号表达式为;从安全角度考虑,如图1在点燃氢气前,一定要检验氢气的。
(2)“分”的思想:航天员在空间站生沽所需氧气主要通过电解水获得,该反应的符号表达式为。图2中管b中的气体是 , 电解水实验中,不变的粒子是
(3)“合”与“分”的思想
通过以上事实,证明了水是由组成,获得此结论的理论依据是。
【证据推理】结合实验现象推算水分子中氢、氧原子个数比。
(4)方法一:根据相同条件下气体的体积比等于其分子的个数比,得出电解水的产物中氢、氧原子个数比为 ,
方法二:已知电解水实验中氢气和氧气的体积比和正、负极产生气体的 , 可计算出水中各元素质量比,结合氢、氧原子的相对原子质量,可进一步推算出结果。
【模型构建】
(5)以分子构成的物质为例,图中“▲”表示的是。

-
6、我国正在筹建月球科考站。针对“月球上是否存在大气”,查阅资料:
资料1 当天体中气体的分子运动平均速率大于分子脱离速率的20%时,该气体会脱离天体逸散到宇宙中。月球表面气体分子的脱离速率均为2.4km·s-1.
资料2 使用质谱仪测定在月球黑暗处发现有极微量的气体生成,其主要成分是氢气、氦气、氖气和氩气等。日出时,月球表面有极微量的甲烷和氨气产生。
(1)、氖的原子结构示意图和氩在元素周期表中的部分信息分别如图所示。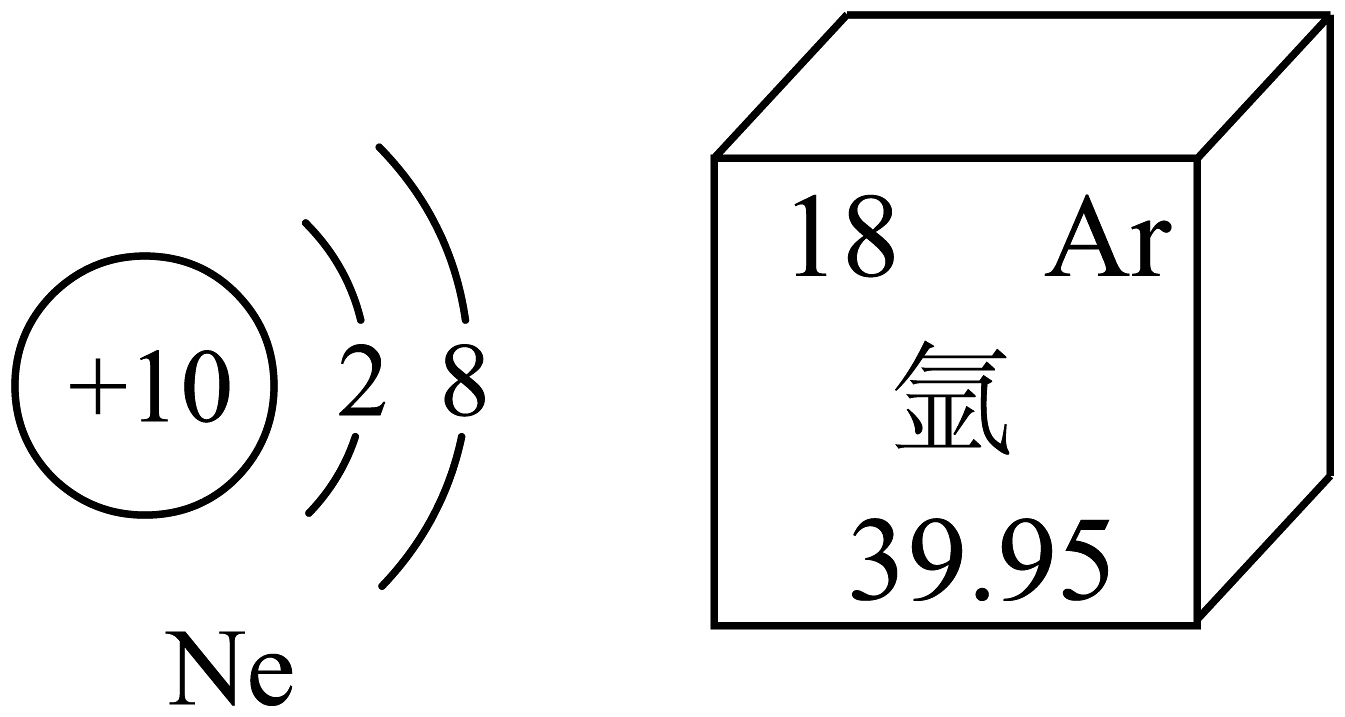
①氖原子的最外电子数为8,属于(填“相对稳定”或“不稳定”),决定原子化学性质的是。
②氩的相对原子质量为。
(2)、0℃时,氢气、氦气和氮气的分子运动示意图分别如下所示。
①由上图分析,分子运动平均速率与有关。
②已知月球表面最高温度超过100℃。月球表面因不能留住氢气、氦气等气体分子,所以不存在稳定大气,结合资料信息说明其原因。
-
7、实验是化学探究的重要途径,下面是有关氧气性质的探究实验,请完成相应问题。
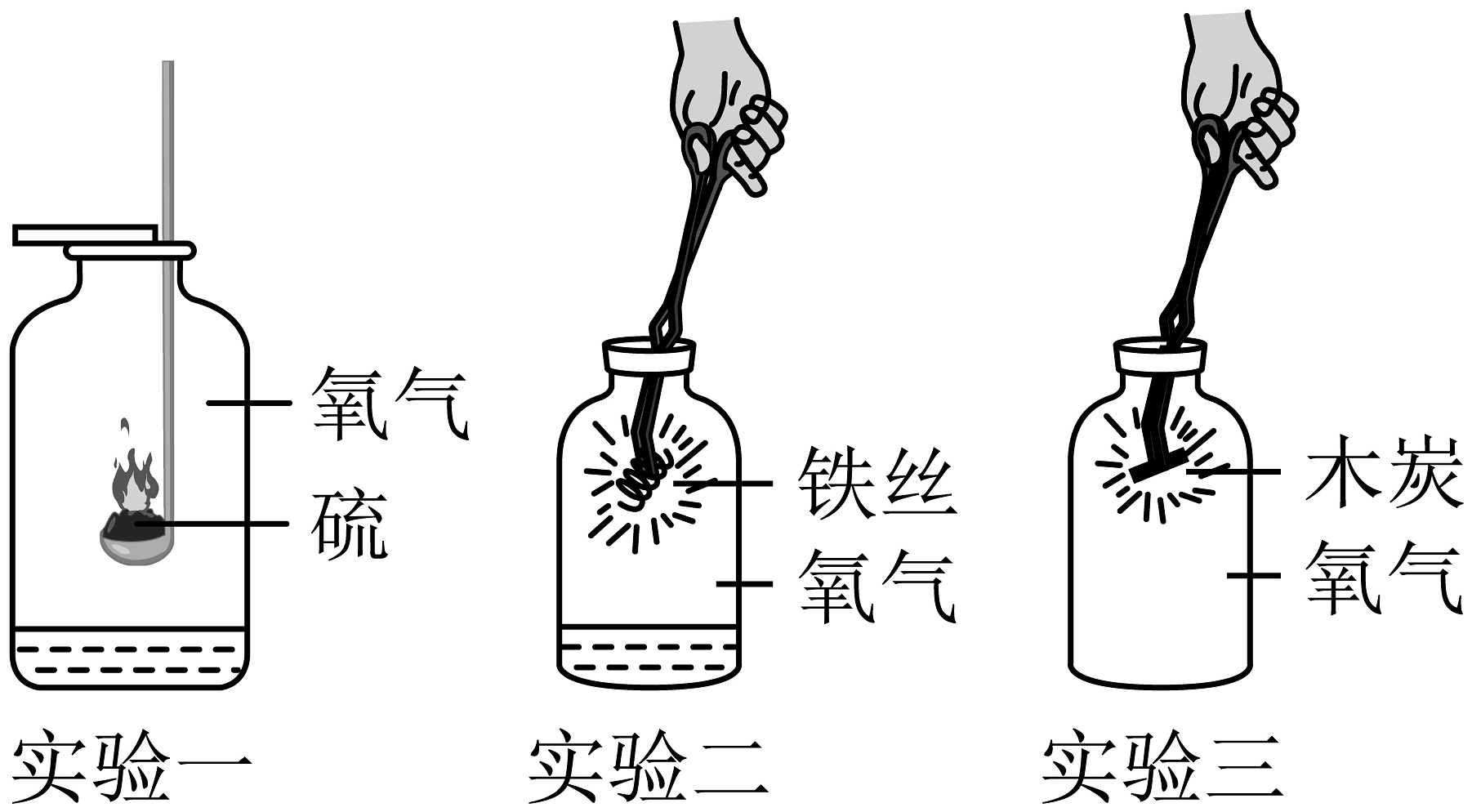 (1)、实验一:硫在氧气中燃烧,产生蓝紫色火焰,放出热量,生成一种有气味的气体,该反应的符号表达式是为。(2)、实验二:铁丝在氧气中剧烈燃烧的符号表达式是;集气瓶内水的作用是。(3)、实验三:木炭在氧气中燃烧,产生一种使澄清石灰水变浑浊的气体,说明木炭在空气中燃烧的生成物为。(4)、以上三个反应的基本类型为。
(1)、实验一:硫在氧气中燃烧,产生蓝紫色火焰,放出热量,生成一种有气味的气体,该反应的符号表达式是为。(2)、实验二:铁丝在氧气中剧烈燃烧的符号表达式是;集气瓶内水的作用是。(3)、实验三:木炭在氧气中燃烧,产生一种使澄清石灰水变浑浊的气体,说明木炭在空气中燃烧的生成物为。(4)、以上三个反应的基本类型为。 -
8、在宏观、微观和符号之间建立联系是化学学科的特点。(1)、物质的组成及构成关系如图1所示图中②表示的是。
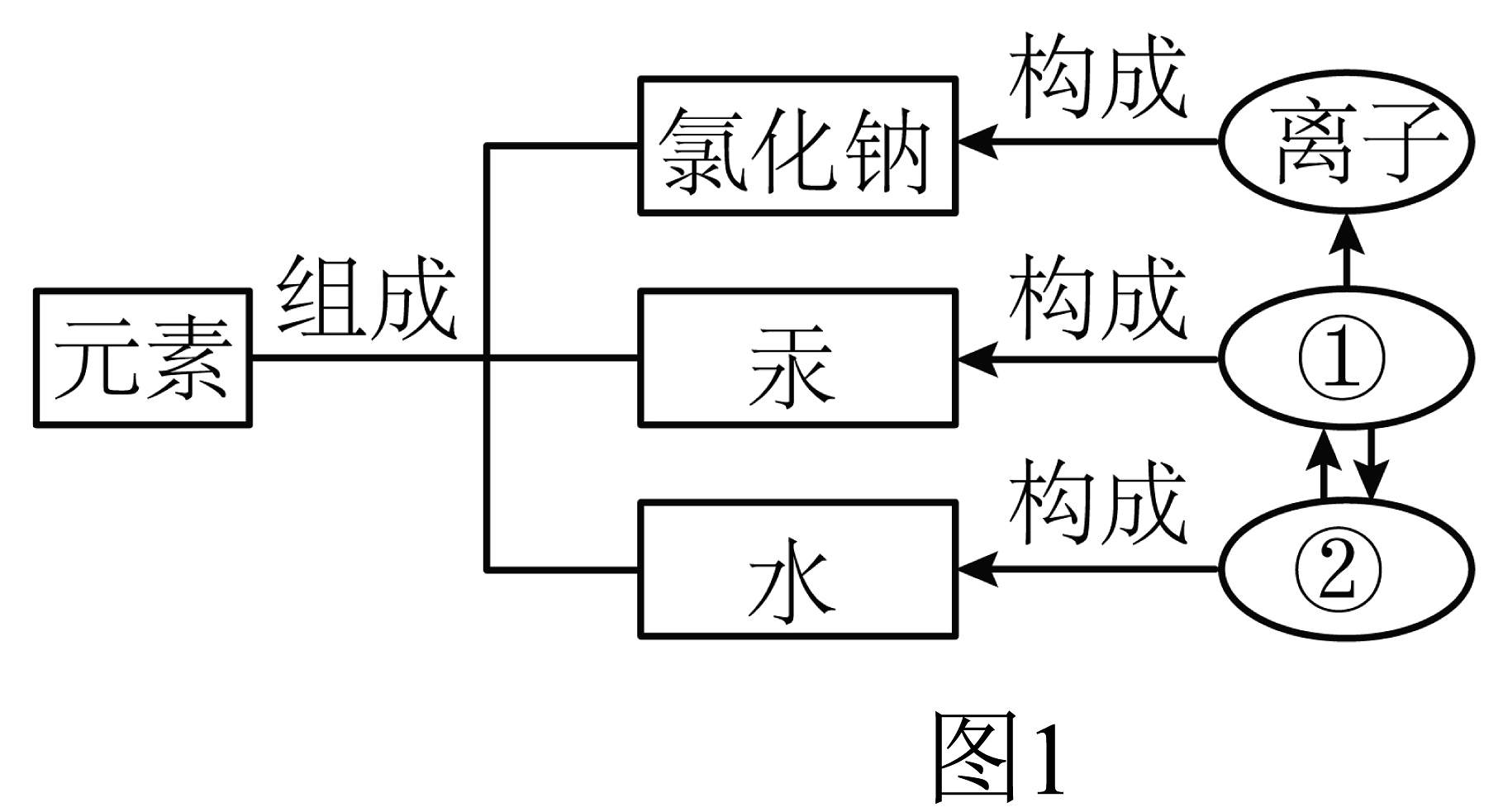 (2)、氯化钠是由组成的,构成氯化钠的粒子是(填符号);(3)、汞是由构成的。(4)、下列说法正确的是___________(填字母)。A、二氧化碳是由二氧化碳分子构成的 B、二氧化碳是由碳和氧气组成的 C、二氧化碳是由一个碳原子和两个氧原子构成的 D、二氧化碳是由一个碳元素和两个氧元素组成的
(2)、氯化钠是由组成的,构成氯化钠的粒子是(填符号);(3)、汞是由构成的。(4)、下列说法正确的是___________(填字母)。A、二氧化碳是由二氧化碳分子构成的 B、二氧化碳是由碳和氧气组成的 C、二氧化碳是由一个碳原子和两个氧原子构成的 D、二氧化碳是由一个碳元素和两个氧元素组成的 -
9、用化学用语填空(1)、4个硅原子。(2)、氢氧根离子。(3)、保持氢气化学性质的粒子是。(4)、两个氧分子。(5)、地壳中含量最多的金属元素和非金属元素形成的化合物的化学式。
-
10、化学课程培养核心素养,体现对学生发展的重要价值。下列相关说法错误的是
A
化学观念
化学变化的本质是分子分裂成原子,原子重新结合成新分子
B
科学思维
催化剂能改变化学反应速率,则要改变化学反应速率必须添加催化剂
C
科学探究与实践
通过蜡烛及其燃烧实验,探究蜡烛的性质
D
科学态度与责任
要保护大气环境,防止空气污染
A、A B、B C、C D、D -
11、对下列事实的解释错误的是
选项
事实
解释
A
用扫描隧道显微镜获得的某种有机物分子图像
分子很小、分子是真实存在的
B
H2O和H2O2的化学性质不同
分子的构成不同
C
用水银体温计测量体温,水银柱上升
温度升高,分子变大
D
冰水混合物属于纯净物
都含有同一种分子
A、A B、B C、C D、D -
12、某化学符号的意义如下:①表示一种物质;②表示该物质由两种元素组成;③表示1个分子;④表示1个分子由3个原子构成。下列选项中符合上述描述的是A、Cl2 B、KCl C、ClO2 D、HClO
-
13、元素观微粒观是化学的重要观念,下列有关元素和微粒的说法不正确的是A、相对原子质量越大的原子质量越大 B、同种原子可以构成不同种分子 C、繁多复杂的物质世界是由种类有限的元素组成的 D、原子核都由质子和中子构成
-
14、分类是化学学习和研究的重要方法之一,下列分类正确的是A、物理性质包括:溶解性、挥发性、可燃性 B、混合物:空气、海水、稀有气体 C、黑色固体:木炭、二氧化锰、氧化汞 D、可在酒精灯上加热的仪器:燃烧匙、量筒、集气瓶
-
15、下图是实验室制取气体的常用装置,请回答下列问题。
 (1)、仪器①的名称为。(2)、实验室常用B装置制取氧气,反应的化学方程式是;若想收集到纯净的氧气应选择的收集装置是;(3)、若用F装置利用排空气法收集氧气,氧气应从端(填“a”或“b”)进入。(4)、图G是利用制得的氧气验证氧气性质的实验,图G中装少量水的作用是 , 该反应的化学方程式是。(5)、甲烷是一种无色、无味的气体,密度比空气小且极难溶于水,是天然气的主要成分。实验室制取甲烷气体常用无水醋酸钠(固体)和碱石灰(固体)加热制得。则实验室制取甲烷可选用以上的发生装置是(填序号)。(6)、实验室用加热高锰酸钾的方法制取氧气,若要制取0.8g氧气,理论上需要高锰酸钾的质量是多少?(写出计算过程)。
(1)、仪器①的名称为。(2)、实验室常用B装置制取氧气,反应的化学方程式是;若想收集到纯净的氧气应选择的收集装置是;(3)、若用F装置利用排空气法收集氧气,氧气应从端(填“a”或“b”)进入。(4)、图G是利用制得的氧气验证氧气性质的实验,图G中装少量水的作用是 , 该反应的化学方程式是。(5)、甲烷是一种无色、无味的气体,密度比空气小且极难溶于水,是天然气的主要成分。实验室制取甲烷气体常用无水醋酸钠(固体)和碱石灰(固体)加热制得。则实验室制取甲烷可选用以上的发生装置是(填序号)。(6)、实验室用加热高锰酸钾的方法制取氧气,若要制取0.8g氧气,理论上需要高锰酸钾的质量是多少?(写出计算过程)。 -
16、如图分别是水的净化、水的合成、水的分解实验,请回答:
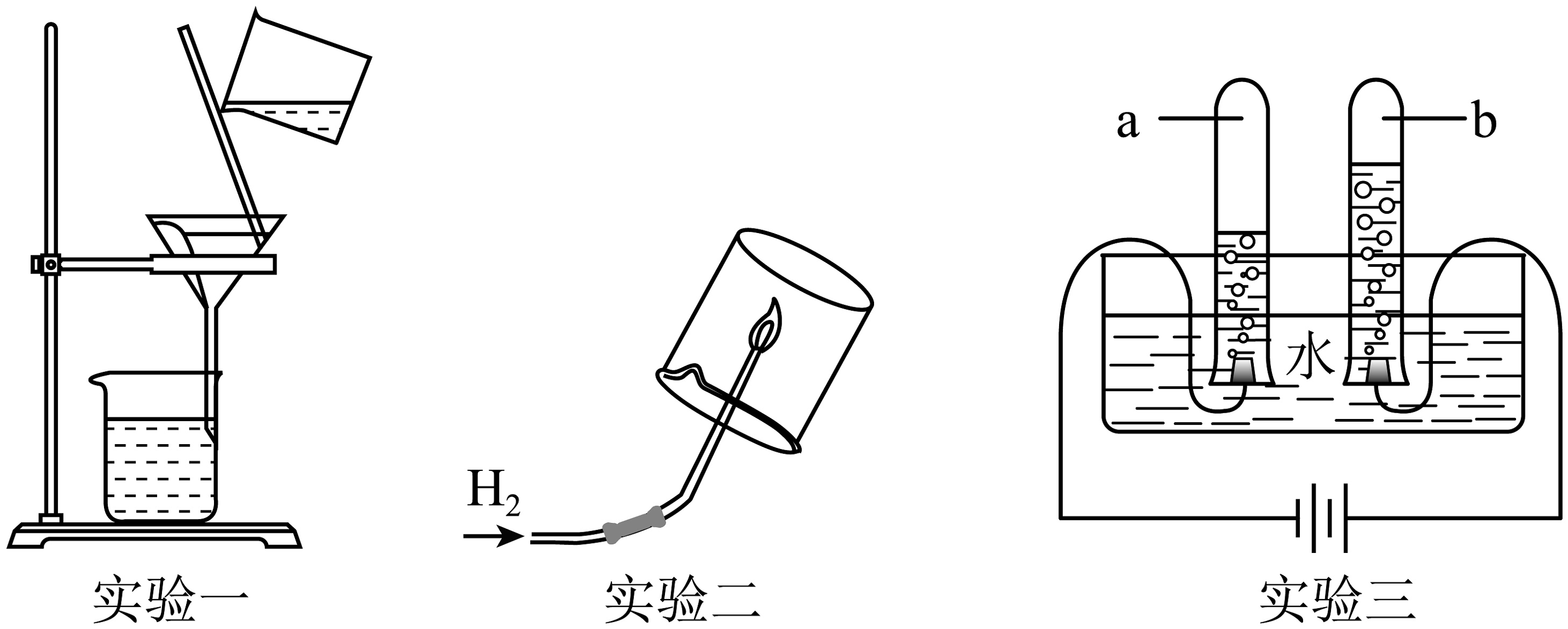 (1)、实验一中是净化水的一种方法,其中玻璃棒的作用是;净化水程度最高的方法是。(2)、实验二中,点燃氢气前必须进行的操作是;该反应的化学方程式是。(3)、实验三中,b管产生的气体是。
(1)、实验一中是净化水的一种方法,其中玻璃棒的作用是;净化水程度最高的方法是。(2)、实验二中,点燃氢气前必须进行的操作是;该反应的化学方程式是。(3)、实验三中,b管产生的气体是。 -
17、“宏观-微观-符号”之间建立联系是化学学习的重要思维方式。请根据示意图回答下列问题:
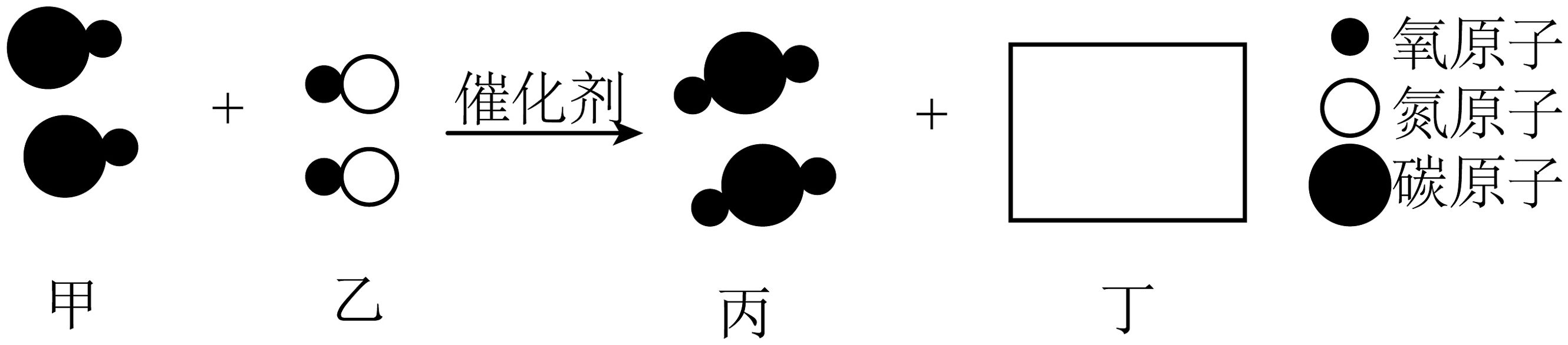 (1)、请在框中画出丁分子的模型。(2)、该反应的化学方程式为。(3)、生成物丙与丁的质量之比。
(1)、请在框中画出丁分子的模型。(2)、该反应的化学方程式为。(3)、生成物丙与丁的质量之比。 -
18、某化学兴趣小组的同学设计了如图实验装置(天平略)验证质量守恒定律。
 (1)、上述四个实验装置中,能直接用于验证质量守恒定律的是。(2)、C装置和D装置不能验证质量守恒定律的理由是。(3)、通过上述实验,同学们得出结论:当有气体参加或生成的反应,验证质量守恒定律必须在装置中进行。(4)、从微观角度分析,在化学反应前后,下列五项中一定不变的是(填数字序号)。
(1)、上述四个实验装置中,能直接用于验证质量守恒定律的是。(2)、C装置和D装置不能验证质量守恒定律的理由是。(3)、通过上述实验,同学们得出结论:当有气体参加或生成的反应,验证质量守恒定律必须在装置中进行。(4)、从微观角度分析,在化学反应前后,下列五项中一定不变的是(填数字序号)。①原子种类 ②分子种类 ③原子数目 ④分子数目 ⑤原子质量
-
19、甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,丙是单质:乙通常为液体,在一定条件下可分解生成丙。它们之间转化关系如图所示(部分物质和反应条件已略去)。
 (1)、甲的化学式为;(2)、乙转化为丙的化学方程式为;(3)、甲反应类型是。
(1)、甲的化学式为;(2)、乙转化为丙的化学方程式为;(3)、甲反应类型是。 -
20、建立“宏观—微观”之间的联系,是化学学习的重要方法。根据图示回答下列问题:
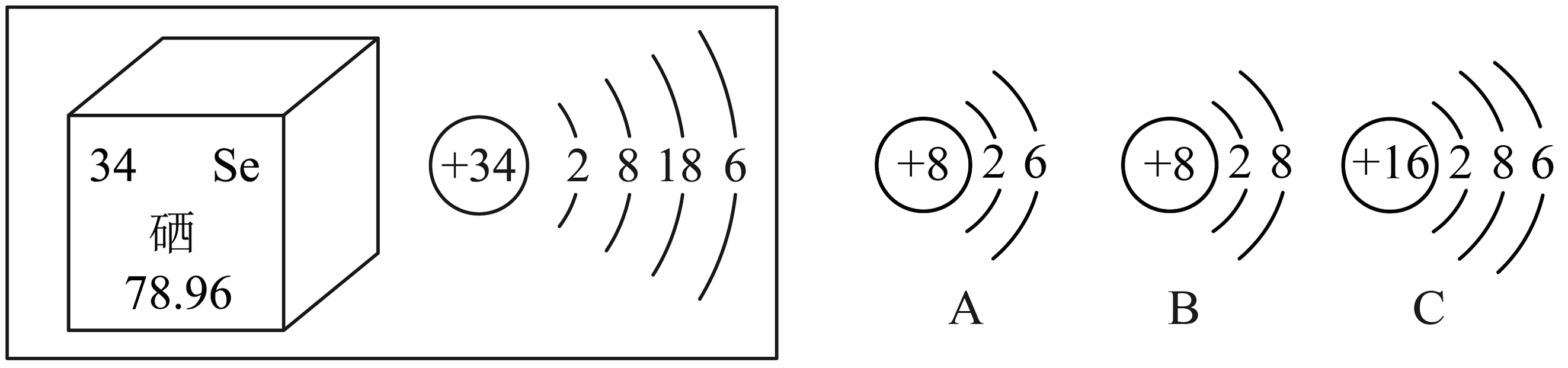 (1)、硒元素被科学家称为“抗癌之王”,科学界研究发现血硒水平的高低与癌的发生息息相关。如图:硒的相对原子质量是;硒元素位于第周期。(2)、A、B、C中共有种元素;表示的阴离子是(写离子符号)。
(1)、硒元素被科学家称为“抗癌之王”,科学界研究发现血硒水平的高低与癌的发生息息相关。如图:硒的相对原子质量是;硒元素位于第周期。(2)、A、B、C中共有种元素;表示的阴离子是(写离子符号)。