-
1、化学用语是国际通用的化学语言,下列有关说法不正确的是A、:“”表示一个镁离子带2个单位正电荷 B、:“4”表示四个钠元素 C、“”表示氧化铜中铜元素的化合价为价 D、:“3”表示3个水分子
-
2、人体吸入的空气中有转化为活性氧,它会加速人体衰老。科学家尝试用亚硒酸钠()清除人体内的活性氧,下列有关亚硒酸钠的说法正确的是A、亚硒酸钠属于氧化物 B、亚硒酸钠由2个钠原子、1个硒原子和3个氧原子构成 C、亚硒酸钠由三种元素组成 D、亚硒酸钠中含有臭氧分子
-
3、我国研究人员将应用到光电催化分解水实验。铋元素在元素周期表中的信息如图所示。下列关于铋元素的说法正确的是
 A、属于非金属元素 B、铋的相对原子质量为 C、中子数为83 D、铋原子的核外电子数为83
A、属于非金属元素 B、铋的相对原子质量为 C、中子数为83 D、铋原子的核外电子数为83 -
4、人类的生存离不开空气,下列关于空气及其成分说法正确的是A、氮气化学性质不活泼,可用于食品防腐 B、新鲜空气中不含二氧化碳 C、氧气的化学性质很活泼,常温下能与所有物质发生化学反应 D、空气中既含有单质也含有化合物,其组成是固定不变的
-
5、2024年世界环境日的中国主题是“全面推进美丽中国建设”。下列做法符合此主题的是A、就地丢弃废旧塑料 B、分类回收生活垃圾 C、生活污水排入河道 D、乱采矿产资源
-
6、物质的性质决定物质的用途。下列物质的用途主要应用其化学性质的是A、活性炭作冰箱除味剂 B、稀有气体用于制作霓虹灯 C、铜丝作导线 D、双氧水用于消毒
-
7、备基本的实验技能是进行科学探究的保证,下列实验操作正确的是A、过滤黄河水
 B、点燃酒精灯
B、点燃酒精灯 C、氧气的验满
C、氧气的验满 D、倾倒液体
D、倾倒液体
-
8、化学课上,同学们看老师做镁条与稀盐酸反应的实验,观察到反应非常剧烈,产生大量气泡。于是就提出“铜片能不能与稀盐酸反应呢”,这一过程属于科学探究中的A、提出问题 B、设计实验 C、进行观察 D、得出结论
-
9、成语是中华民族文明与智慧的结晶,是中华文化的瑰宝。下列成语所描述的情境主要包含化学变化的是A、风吹草动 B、立竿见影 C、火上浇油 D、滴水成冰
-
10、构建知识网络是一种重要的学习方法。如图为兴趣小组绘制的铁的化学性质知识网络图。
 (1)、反应①中另一反应物可以是(填化学式)。(2)、早在西汉时期,我国劳动人民就利用反应②制取铜,称为“湿法炼铜”,该反应的现象是。(3)、为了测定某生铁中铁的含量,该小组利用反应③的原理进行如下实验:将一定质量的生铁样品(杂质不溶于水,也不与稀硫酸反应)放入足量的稀硫酸中,充分反应后,生成0.2g气体;过滤,将所得固体洗涤、干燥后称得其质量为0.2g。计算该生铁中铁的质量分数。(结果精确到0.1%)
(1)、反应①中另一反应物可以是(填化学式)。(2)、早在西汉时期,我国劳动人民就利用反应②制取铜,称为“湿法炼铜”,该反应的现象是。(3)、为了测定某生铁中铁的含量,该小组利用反应③的原理进行如下实验:将一定质量的生铁样品(杂质不溶于水,也不与稀硫酸反应)放入足量的稀硫酸中,充分反应后,生成0.2g气体;过滤,将所得固体洗涤、干燥后称得其质量为0.2g。计算该生铁中铁的质量分数。(结果精确到0.1%) -
11、我国是世界上锌冶炼最早的国家。明代宋应星所著的《天工开物》中有关“火法”炼锌的工艺记载是:“每炉甘石(主要成分是碳酸锌)十斤装载入一泥罐内……然后逐层用煤炭饼(反应后生成一氧化碳)垫盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅(锌)也。”此工艺过程分解模拟如图。(已知:Zn的熔点420℃,沸点为907℃。)请结合图文信息,分析思考,解决问题:
 (1)、炉甘石主要成分属于(多选,填字母)。
(1)、炉甘石主要成分属于(多选,填字母)。a.纯净物 b.化合物 c.混合物 d.氧化物
(2)、装入原料器之前,将炉甘石敲碎的目的是。(3)、煤属于(填“可再生”或“不可再生”)能源。“其底铺薪”中的“薪”的作用是。(4)、高温炉内,碳酸锌(ZnCO3)在高温条件下与煤的主要成分发生反应生成Zn和CO,反应的化学方程式为。ZnCO3中碳元素的化合价为价。(5)、冷凝器通过控制温度除去CO的同时液态锌流出,故温度应控制在。(6)、我国古代冶锌晚于铁和铜,结合已知信息,分析说明其中的原因是。 -
12、
在日常生活中能看到很多精美的金属蚀刻画。兴趣小组利用废弃的金属片进行制作金属蚀刻画的项目活动,请你一起参与下列任务。
任务一:到垃圾回收站筛选金属底板
(1)区分铝片和铁片的物理方法是(写一种)。
任务二:预处理金属底板
用砂纸打磨掉铝片表面的氧化膜,用化学方法除去铁片表面的铁锈。
任务三:选择蚀刻液进行蚀刻
(2)首先将有镂空图案的不干胶保护膜(能隔绝蚀刻液与金属底板接触)分别贴到处理好的铝片和铁片上,然后将铝片浸入足量的甲蚀刻液中,将铁片浸入足量的乙蚀刻液中,一段时间后取出。小组同学看到铝片上有凹陷图案,没有附着物;铁片上出现红色附着物图案。则甲蚀刻液、乙蚀刻液分别是下列中的、(填序号)。
①硫酸铜溶液 ②硝酸银溶液 ③稀盐酸 ④氯化亚铁溶液 ⑤氯化钠溶液
任务四:金属蚀刻画的后处理
(3)将蚀刻好的金属片清洗掉废液,去掉不干胶保护膜,进行装饰。为防止铁片蚀刻画生锈,可采取的措施是(写一种)。
任务五:废液回收利用
(4)铝片蚀刻废液处理,可加入足量铝片,得到溶液,回收保存。
(5)铁片蚀刻废液处理,如图所示:
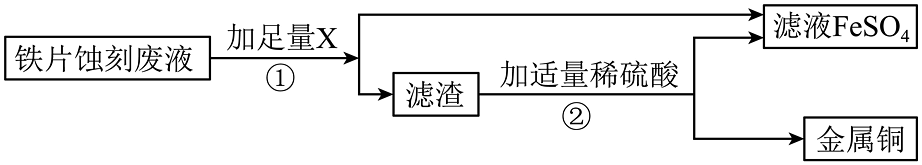
过程①和②都涉及的实验操作是 , 过程①加入的物质X是 , 过程②加入稀硫酸反应的化学方程式是;其基本反应类型是。
-
13、回答下列问题。(1)、实验室制取气体。

①仪器甲的名称是。
②若实验室用高锰酸钾制氧气,应在装置A的试管口 , 以防固体粉末进入导管。
③若实验室用装置BD制取氧气,其反应的化学方程式为。
④装置B、C均可用于实验室制取二氧化碳,两者相比,装置C的优点是 , 不能用装置D收集可推其具有的物理性质是。在装置E中加入用于检验CO2。
(2)、基于特定需求设计和制作简易供氧器。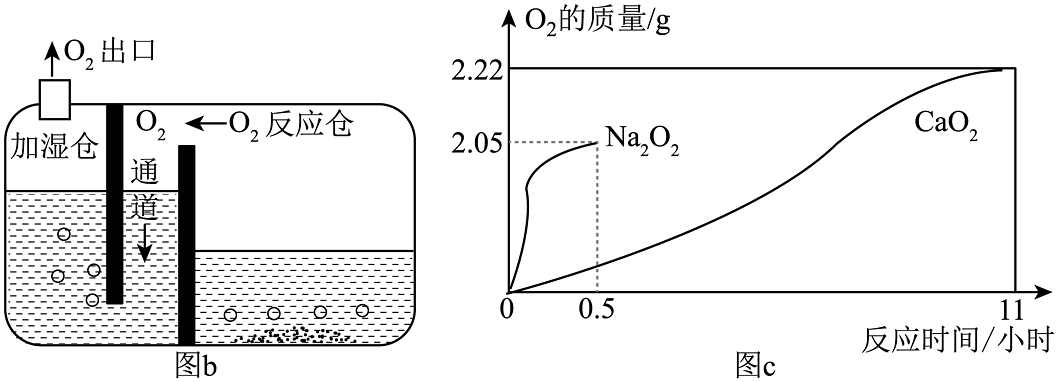
①加湿仓内水的作用是(写一点),图b中“O2通道”相当于图a中E装置的(填“a”或“b”)端导管。
②10gNa2O2和10gCaO2固体与水作用生成氧气的质量与时间的关系如图c所示,若给鱼池增氧,应选的药品为(填化学式)。
-
14、氢能有望在未来能源体系中占据更加重要的位置。制氢(图1)、储氢和用氢(图1)是目前重点关注的问题。
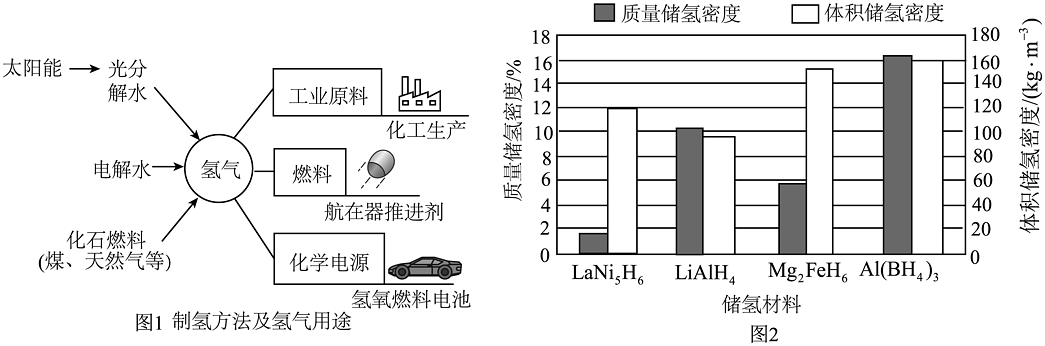
氢气的储存方式主要有金属氢化物储氢、低温液化储氢、高压压缩储氢、碳基材料储氢等。图2为一些储氢材料(以储氢后的化学式表示)的质量储氢密度和体积储氢密度。(已知:质量储氢密度=储氢后氢元素在储氢材料中的质量分数;体积储氢密度=储氢后单位体积的储氢材料中储存氢元素的质量)。
依据上文,回答问题。
(1)、氢能具有的优点是(写一点)。(2)、从节能的角度分析,最理想的制氢的方式是。a.光分解水 b.电解水 c.化石燃料制氢
(3)、从分子的角度解释低温或高压储氢的原理:。(4)、用作碳基储基储氢材料的“碳纳米管”与金刚石都是碳的单质,但物理性质不同原因是。(5)、分析图2,下列储氢材料中最理想的是(填字母)。a.LaNi5H6 b.LiAlH4 c.Mg2FeH6 d.Al(BH4)3
(6)、氢氧燃料电池是将能直接转化为电能的装置。一定条件下,氢氧燃料电池内发生反应的化学方程式为。 -
15、化学源于生活,生活中蕴含着许多化学知识。(1)、某保健食品中含有的“钙、铁、锌”等指的是(填“原子”“分子”或“元素”)。(2)、自来水厂净化过程中利用除去水中色素和异味;长期饮用硬水对人体有害,日常生活中常用的方法降低水的硬度。(3)、古代用墨书写或绘制的字画能够保存至今的原因:。(4)、生石灰(CaO)除湿防潮的原理是(用化学方程式表示),该反应(选填“放出”或“吸收”)热量。
-
16、我国科研人员实现了用高效催化剂将甲烷与氧气在常温下制甲酸。该反应的微观示意图如图,有关说法正确的是
 A、反应前后催化剂的质量和性质不变 B、反应前后原子数目不变 C、参加反应的乙和生成的丁的质量比为16:9 D、参加反应的甲和乙的分子个数比为1:1
A、反应前后催化剂的质量和性质不变 B、反应前后原子数目不变 C、参加反应的乙和生成的丁的质量比为16:9 D、参加反应的甲和乙的分子个数比为1:1 -
17、化学课程要培养核心素养。下列有关化学核心素养的理解正确的是A、化学观念:C60是由碳原子构成的 B、科学思维:化学反应常伴随着能量变化,故有能量变化的一定是化学反应 C、科学探究与实践:利用燃着的木条鉴别氮气和二氧化碳 D、科学态度与责任:实验后的废液集中回收处理,符合绿色化学理念
-
18、据报道,维生素C(C6H8O6)对人体有重要的作用,下列有关叙述不正确的是A、每个维生素C分子由20个原子构成 B、维生素C的相对分子质量计算式为12×6+1×8+16×6 C、维生素C中C、H、O元素的质量比为9:1:12 D、维生素C中氧元素的质量分数的计算公式为:×100%
-
19、明代《天工开物》中绘有许多风箱(如图)。为保持冶炼炉内高温,需要不断拉动风箱,目的是
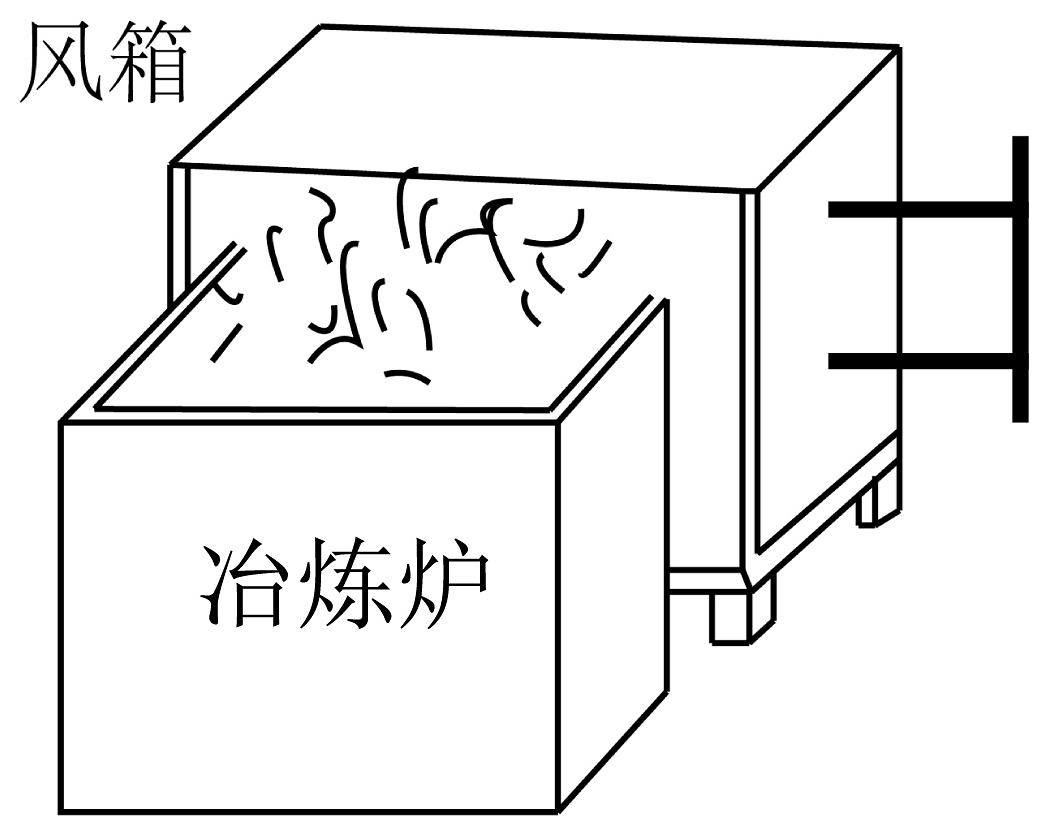 A、降低木材的着火点 B、提供充足的空气 C、增大木材间间隔 D、清除多余的可燃物
A、降低木材的着火点 B、提供充足的空气 C、增大木材间间隔 D、清除多余的可燃物 -
20、下列有关物质用途的说法不正确的是:A、氮气可用于包装食物 B、铜常用于制作导线 C、金刚石可用于切割玻璃 D、铅可用作铅笔芯