-
1、2024年中国环境日的主题为“全面推进美丽中国建设”。下列做法与该主题相符的是A、工业废水未经净化处理直接排放 B、大量燃放烟花爆竹增添节日气氛 C、合理使用农药、化肥,减少水体污染 D、多开私家车,方便出行
-
2、市面上有一种免洗手消毒凝胶,其成分中含有正丙醇(化学式为C3H8O)。请计算:(1)、正丙醇的相对分子质量为。(2)、正丙醇中碳、氢、氧元素的质量比是(填最简整数比)。(3)、正丙醇中碳元素的质量分数为(列出计算过程方可得分)。
-
3、如图是实验室制取气体的常用装置,回答下列问题:
 (1)、写出仪器a的名称。(2)、实验室用高锰酸钾制取氧气的符号表达式为 , 该反应的发生装置为(填字母),该装置有一处不足的地方,请你加以改正。(3)、甲同学要做铁丝在氧气中燃烧的实验,用装置E收集氧气,这样做对该实验的优点是铁丝在氧气中燃烧的符号表达式为。(4)、用装置F进行“排空气法”收集氧气,把图中的F瓶内“导气管”补画完整。
(1)、写出仪器a的名称。(2)、实验室用高锰酸钾制取氧气的符号表达式为 , 该反应的发生装置为(填字母),该装置有一处不足的地方,请你加以改正。(3)、甲同学要做铁丝在氧气中燃烧的实验,用装置E收集氧气,这样做对该实验的优点是铁丝在氧气中燃烧的符号表达式为。(4)、用装置F进行“排空气法”收集氧气,把图中的F瓶内“导气管”补画完整。
-
4、在宏观、微观和符号之间建立联系是化学学科的重要思维方式。(1)、图1为构成物质的粒子之间的关系,字母a代表的是 , 字母b代表的是。
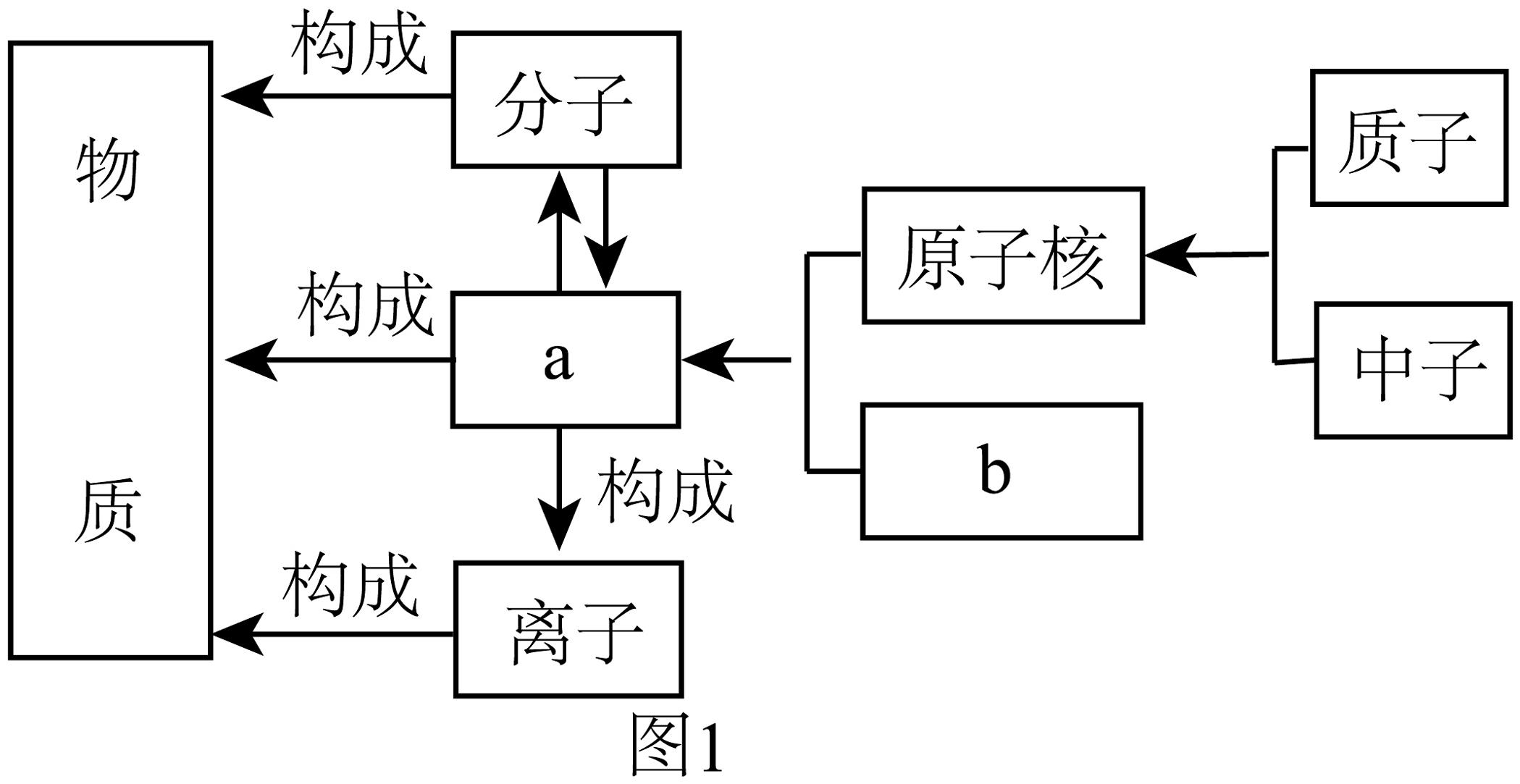 (2)、如图2所示,A、B、C、D、E属于同种元素的是(填序号),C元素位于第周期,E微粒是(填“原子”或“阴离子”或“阳离子”)。
(2)、如图2所示,A、B、C、D、E属于同种元素的是(填序号),C元素位于第周期,E微粒是(填“原子”或“阴离子”或“阳离子”)。 (3)、若D表示某元素的原子,则m= , 该微粒在化学变化中容易(填“得到”或“失去”)电子。(4)、B和D元素原子相互化合时形成的化合物是(填化学式)。
(3)、若D表示某元素的原子,则m= , 该微粒在化学变化中容易(填“得到”或“失去”)电子。(4)、B和D元素原子相互化合时形成的化合物是(填化学式)。 -
5、水是一种重要的资源,人类离不开水。公园、车站等公共场所内设有许多直饮水机,其中水处理的过程如图所示。
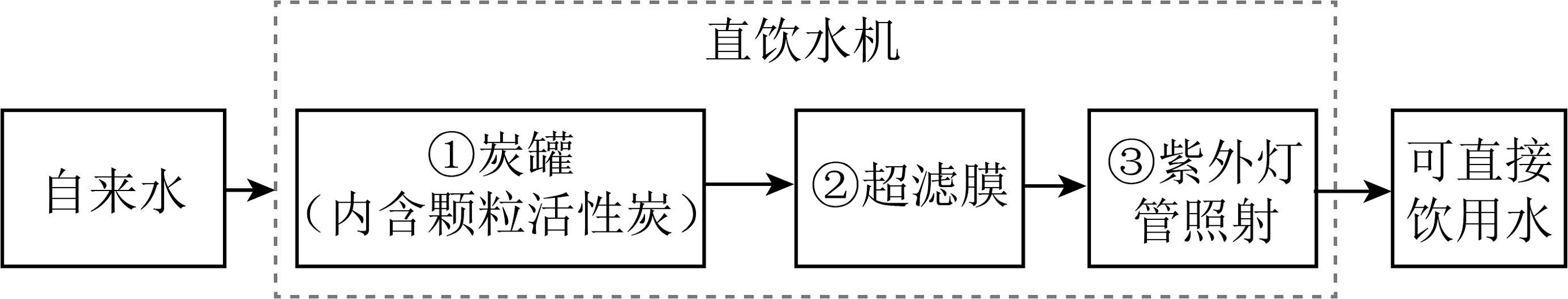 (1)、自来水中含有较多的钙离子、镁离子,则该水为(填“硬水”或“软水”),生活中降低水的硬度,常采用的方法。(2)、炭罐中利用活性炭的性除去水中的色素异味。(3)、步骤②相当于(填操作名称),该操作中用到的玻璃仪器有漏斗、烧杯和。过滤后发现滤液仍然浑浊,可能的原因是(写出一条即可)。(4)、流程③“紫外灯管照射”的过程发生的是变化(填“物理”或“化学”)。(5)、请写出一条生活中节约用水的措施。
(1)、自来水中含有较多的钙离子、镁离子,则该水为(填“硬水”或“软水”),生活中降低水的硬度,常采用的方法。(2)、炭罐中利用活性炭的性除去水中的色素异味。(3)、步骤②相当于(填操作名称),该操作中用到的玻璃仪器有漏斗、烧杯和。过滤后发现滤液仍然浑浊,可能的原因是(写出一条即可)。(4)、流程③“紫外灯管照射”的过程发生的是变化(填“物理”或“化学”)。(5)、请写出一条生活中节约用水的措施。 -
6、水是一种重要的自然资源,爱护水资源,人人有责。(1)、如图是水的电解实验装置图,请回答下列问题:
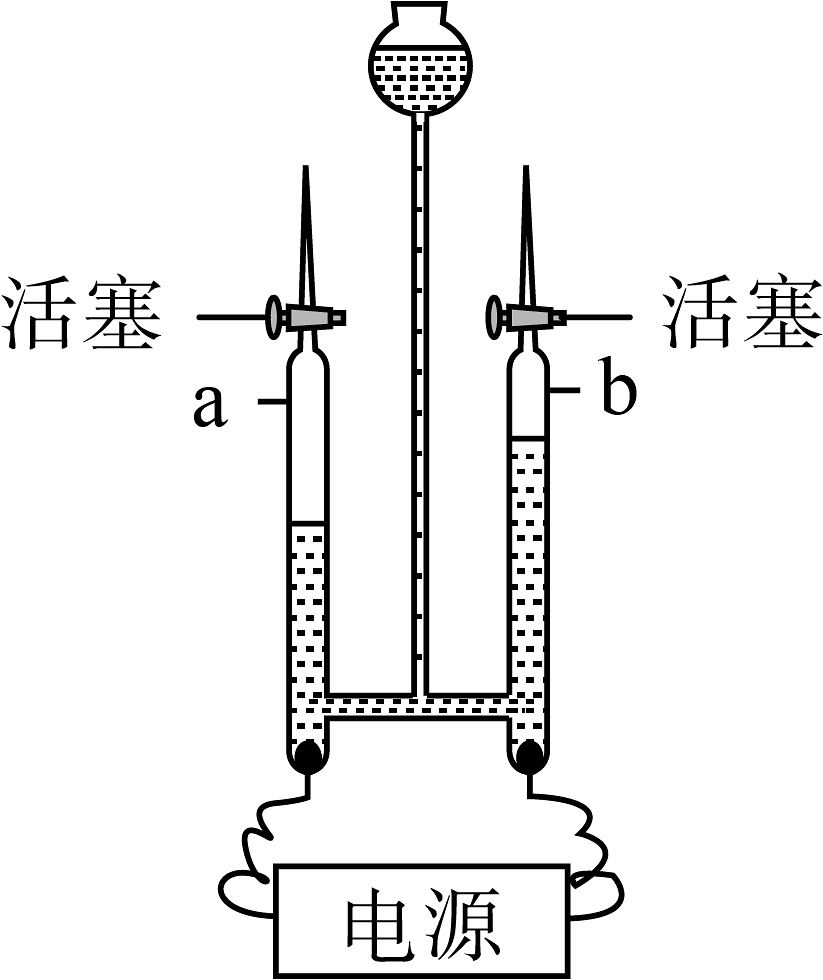
①与b管相连的是电源的(填“正”或“负”)极;a管产生的气体是。
②若a管收集到8mL气体,则在相同条件下b管应收集到的气体是mL。
(2)、从微观上分析:下列说法正确的是_______(填字母序号)。A、水是由氢气和氧气组成的 B、水是由氢元素和氧元素组成的 C、每个水分子是由2个氢原子和1个氧原子构成的(3)、写出电解水反应的符号表达式。 -
7、空气是一种宝贵的资源,对人类的生产、生活有重要作用。(1)、从分类角度:洁净的空气属于(填“纯净物”或“混合物”)。(2)、从含量角度:航天员翟志刚、王亚平、叶光富在中国“天和号”空间站进行“天宫课堂”第一课。水球光学实验中打入的“人造空气”与我们身边的空气成分含量基本相同,“人造空气”中氧气含量约为_______。A、0.03% B、0.94% C、21% D、78%(3)、从环保角度:随着工业的发展,排放到空气中的有害气体和烟尘对空气造成了污染,下列物质中,不属于空气污染物的是_______。A、二氧化硫 B、二氧化碳 C、一氧化碳 D、二氧化氮(4)、从应用角度:工业上用分离液态空气的方法制取氧气。从微观角度解释,在空气液化过程中,主要改变的是(填“分子的间隔”或“分子大小”)。(5)、如图为实验室里测定空气中氧气含量的实验。

红磷燃烧时,产生大量的(填“白烟”或“白雾”),其反应的符号表达式为。
-
8、用化学用语填空。(1)、1个氢离子。(2)、1个氧分子。(3)、4个硫原子。(4)、磷元素。(5)、CO2中碳元素的化合价。(6)、氧化铝。
-
9、NaClO中Cl的化合价为A、+5 B、+3 C、0 D、+1
-
10、柠檬酸(C6H8O7)是一种常用于制汽水、果冻的添加剂,关于柠檬酸的说法正确的是A、柠檬酸属于氧化物 B、柠檬酸是由碳、氢、氧三种元素组成的 C、柠檬酸是由碳、氢、氧三种原子构成的 D、柠檬酸中氢元素的质量分数最大
-
11、下列实验现象的描述正确的是A、硫在氧气中燃烧发出蓝紫色火焰,有刺激性气味 B、红磷在空气中燃烧产生大量的白雾 C、木炭在氧气中燃烧发出红光 D、铁在氧气中燃烧,生成四氧化三铁
-
12、将一段去除氧化镁的镁条放入一定量的盐酸中,有气泡产生,充分反应后静置,发现试管中有白色沉淀产生。为探究白色沉淀的成分,九(1)班兴趣小组同学在老师的指导下进行如下实验:
试管(盛有等体积等浓度的盐酸)
①
②
③
④
镁条质量(g)
1
1.5
2
2.5
实验现象
快速反应,试管发热,镁条全部消失
白色沉淀量(恢复至20℃)
无
少量
较多
很多
(1) 4支试管中盛有等体积等浓度的盐酸的原因。
[得出结论]
(2)镁条与盐酸反应产生白色沉淀的量与有关。
[提出问题]
白色沉淀是什么物质?
[查阅资料]
在氯化镁溶液中,镁能与水常温下反应生成氢氧化镁和氢气。
[猜想与假设]
甲:白色沉淀可能是碳酸镁
乙:白色沉淀可能是生成的氯化镁增多析出的晶体
丙:白色沉淀可能是剩余的镁
丁:白色沉淀可能是氢氧化镁
(3)其他同学认为甲的猜想是错误的,原因是。
[实验验证]
序号
操作步骤
实验现象
结论
1
取第一份白色不溶物于试管中,加入蒸馏水,振荡
(4)沉淀溶解(选填会或不会)
乙同学猜想不成立
2
取第二份白色不溶物于试管中,加入稀盐酸
(5)
丙同学猜想不成立
3
①取第三份白色不溶物于试管中,加入稀硝酸
②向所得溶液加入几滴硝酸银溶液
①白色沉淀不溶解
②出现大量白色沉淀
①丁同学猜想不成立
②白色不溶物定含
(6)元素
[实验结论]
在老师的帮助下,同学们得出白色沉淀物是Mg2(OH)2Cl2 , 反应的化学方程式为2Mg+2HCl+2H2O=Mg2(OH)2Cl2+2H2。
-
13、在“空气中氧气含量的测定”实验探究中,小明进行了如下实验,将红磷盛放在燃烧匙内,点燃后立即插入集气瓶内并塞上胶塞.
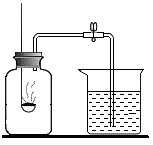
(1)实验原理:由于红磷燃烧消耗空气中的氧气,生成固体,使瓶内减小,烧杯中水倒吸到集气瓶.由此可以得出氧气约占空气体积的;
(2)集气瓶中红磷燃烧的现象是:;写出相关的化学表达式 .
(3)红磷燃烧一段时间后自动熄灭了,你认为原因是;
(4)冷却后,松开止水夹,你观察到的现象为 ,
(5)结果发现测定氧气的体积分数低于21%,造成此结果的可能原因主要有(写出一点即可)
(6)为获得较为准确的实验数据,下列做法不正确的是 .
A 检查装置的气密性
B 燃烧匙中的红磷足量
C 点燃红磷后缓慢将燃烧匙插入瓶中,塞紧瓶塞
D 红磷熄灭,集气瓶冷却后打开弹簧夹
-
14、水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任。解答下列问题:(1)、海水含有大量氯化钠,氯化钠中阳离子的符号是(填微粒符号);(2)、①除去水中异味和色素的试剂常用(填物质名称),该物质起作用。
②进入用户的自来水,在饮用之前要将其 , 目的是除去可溶性离子和杀菌消毒。
③净水盐高铁酸钠的化学式为Na2FeO4 , 铁元素的化合价为 , 此物质中质量分数最大的元素是(铁的相对原子质量为56)。
④除去不溶性杂质时,下列操作规范的是(填字母)。
A.用玻璃棒引流
B.将滤纸湿润,使其紧贴漏斗内壁
C.漏斗下端紧靠烧杯内壁
D.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(3)、①如图是电解水的实验,请写出该反应的符号表达式 , 通电一段时间后,玻璃管a中收集到的气体是 , a管和b管产生气体的体积比为。②关于电解水实验,下列说法正确的是。

A.水分子发生了改变
B.氢原子和氧原子没有发生变化
C.该实验说明水是由氢元素和氧元素组成的
D.该变化中水分子是化学变化中最小的微粒
-
15、下表是元素周期表的一部分:
族
周期
IA
0
一
1 H
1.008
ⅡA
ⅢA
ⅣA
V A
ⅥA
ⅦA
2
4.003
二
3 Li
6.941
4 Be
9.012
5 B
10.8l
6 C
12.01
7 N
14.0l
8 O
16.00
9 F
19.00
10 Ne
20.18
三
11 Na
22.99
12 Mg
24.31
13 Al
26.98
14 Si
28.09
15 P
30.97
16 S
32.06
17 Cl
35.45
18 Ar
39.95
(1)Be元素的相对原子质量为;
(2)相对原子质量为22.99的元素属(填“金属”或“非金属”);Ne的化学性质比较(填“稳定”或“不稳定”);F元素最外层电子数为;
(3)下图为某元素的原子结构示意图,该元素位于周期表中第周期。

-
16、图①、②是碳元素、氯元素在元素周期表中的信息,A、B、C是三种原子的结构示意图。请回答:
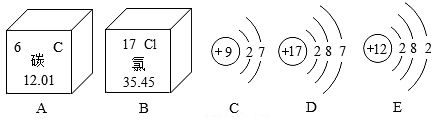 (1)、碳原子的原子序数是 , 碳元素位于元素周期表中第周期,表示氯原子的结构示意图的是;(2)、D元素与E所代表的元素可形成一种化合物,其化学式为;(3)、C的原子化学反应中易(填得到或失去)电子,理由是。
(1)、碳原子的原子序数是 , 碳元素位于元素周期表中第周期,表示氯原子的结构示意图的是;(2)、D元素与E所代表的元素可形成一种化合物,其化学式为;(3)、C的原子化学反应中易(填得到或失去)电子,理由是。 -
17、空气是人类宝贵的自然资源。下列说法正确的是A、空气中氮气的质量分数约占78%,氧气的质量分数约占21% B、红热的细铁丝在空气中剧烈燃烧,火星四射,产生黑色固体 C、利用红磷可以测量出空气中氧气含量,体积约占空气总体积的五分之一 D、造成空气污染的主要气体有CO、CO2、SO2、NO2
-
18、手机使用的锂电池是新型的高能电池,以质量轻、电容量大而受到重视。其中锂电池的总反应可表示为Li+MnO2=LiMnO2。锂元素(Li)在化合物中显+1价,下列说法中不正确的是A、锂电池是化学能转化为电能的装置 B、发生的化学反应属于化合反应 C、反应前后Mn的化合价从+4降低为+3 D、LiMnO2为锂、锰的氧化物
-
19、硒元素具有抗衰老、抑制癌细胞生长的功能,其原子结构示意图及在元素周期表中的信息如图,下列说法错误的是
 A、硒原子核内有34个质子 B、硒元素位于元素周期表中第五周期 C、硒元素的相对原子质量是78.96 D、硒元素在某些化合物中可显-2价
A、硒原子核内有34个质子 B、硒元素位于元素周期表中第五周期 C、硒元素的相对原子质量是78.96 D、硒元素在某些化合物中可显-2价 -
20、糖类是人类食物的重要成分,在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成CO2和H2O,同时放出能量(已知葡萄糖放出约16kJ的能量)。请回答:(1)、葡萄糖是由(填数字)种元素组成的,其相对分子质量为。(2)、葡萄糖分子中碳、氢、氧原子数目比为(填最简整数比)。(3)、葡萄糖中碳、氢、氧三种元素的质量比为(填最简整数比)。(4)、一般人每行走1km,大约需消耗170kJ的能量。假设这些能量全部来自葡萄糖。小明同学步行5km,大约需消耗(取整数)g葡萄糖。