-
1、实验室制取气体。(1)、ⅰ.仪器a的名称是 , 用A装置制取气体,试管口略向下倾斜的原因。
ⅱ.用B装置制取二氧化碳,发生反应的化学方程式 , 该装置的特点是。
 (2)、探究酸的化学性质。
(2)、探究酸的化学性质。操作
现象
结论

实验观察到(填字母)。
a.甲中铁锈溶解,有少量气泡冒出
b.乙中冒出大量气泡
c.反应后溶液都为无色
酸能与某些金属氧化物;某些活泼金属如钾、钙、钠、铁、(填一种)等;某些盐发生反应。
(3)、微型空气质量“检测站”。ⅰ.如图是“检测站”测到某城区5月4日的空气质量情况,当天(填“非常适合”、“不适合”)户外运动,其首要污染物是。

ⅱ.若要获得天气的其他情况,“检测站”还需选择(答一种)等气象传感器。
-
2、综合利用海水资源是工农业发展的需要。海水晒盐是世界上最早利用海水资源的产业,渗析海水浓缩制盐是最常见的制盐技术,其工作原理如图所示。

浓缩海水的主要成分为氯化钠、氯化镁、溴化钠等。液态溴单质通过酸化氧化的方法得到,因其沸点低,可用热空气法吹出溴气()。剩余的浓海水和石灰乳可制备氢氧化镁阻燃剂。海洋中还含有丰富的生物资源如海带,海带的利用已实现产业化。依据上文,回答下列问题。
(1)、海水中的钠、溴、镁以(填“单质”或“化合物”)形式存在。(2)、溴化钠中溴元素的化合价为-1价,溴化钠的化学式是。(3)、热空气法吹出溴气,利用了溴的(填“物理”或“化学”)性质。(4)、将氯化钠和氯化镁的混合溶液通入如图所示装置中,通过AEM-阴离子交换膜,和(填化学符号)通过CEM-阳离子交换膜,得到淡化液和浓缩海水。(5)、利用浓海水中的氯化镁与石灰乳[主要成分为]反应,可制备固体氢氧化镁阻燃剂,并生成氯化钙,其反应的化学方程式为 , 该反应属于反应(填基本反应类型)。(6)、从人体健康角度分析,海带利用产业化的意义是。 -
3、明代宋应星编著的《天工开物》记载:“凡升水银,或用嫩白次砂,……,其下炭质亦用三十斤。凡升汞,上盖一釜,釜当中留一小孔,釜傍盐泥涂固……。煅火之时,曲溜一头插入釜中通气,……,釜中之气在达于罐中之水而止。”
 (1)、用水银体温计测体温时汞柱升高原因(从微观角度分析)。(2)、“炭质”燃烧常用风箱鼓风辅助,目的是。(3)、“涂固”的目的是保障容器 , 以防汞蒸气泄露;“罐中之水”的作用是液封“空管”和。(4)、“升炼水银”与实验室中(填序号)原理类似。
(1)、用水银体温计测体温时汞柱升高原因(从微观角度分析)。(2)、“炭质”燃烧常用风箱鼓风辅助,目的是。(3)、“涂固”的目的是保障容器 , 以防汞蒸气泄露;“罐中之水”的作用是液封“空管”和。(4)、“升炼水银”与实验室中(填序号)原理类似。a.蒸发 b.蒸馏 c.过滤 d.结晶
(5)、“白次砂”主要含HgS,受热分解生成汞单质和硫磺,其反应的化学方程式为。 -
4、下列实验设计不能达到实验目的的是
实验目的
验证烧碱有吸水性
探究Fe、Cu、Ag的金属活动性强弱
测定空气中氧气的含量
验证质量守恒定律
实验设计




选项
A
B
C
D
A、A B、B C、C D、D -
5、“劳动是一切幸福的源泉”。下列劳动实践与化学知识没有直接关联的是
选项
劳动实践
化学知识
A
利用活性炭自制净水器
活性炭具有杀菌消毒作用
B
菜刀使用后要洗净擦干
铁制品在潮湿的环境中容易生锈
C
种植绿植施用
属于复合肥
D
用碳纤维复合材料制作龙舟桨
碳纤维复合材料密度小、强度高
A、A B、B C、C D、D -
6、可用作钾肥,对大豆的生长具有重要的作用。的溶解度随温度变化的曲线如图所示,下列说法正确的是
 A、将硝酸钾饱和溶液从10℃升温至40℃,仍是饱和溶液 B、40℃时,硝酸钾饱和溶液的溶质质量分数为64% C、30℃,硝酸钾的溶解度为64g D、70℃时,将65g加入到50g水中,形成不饱和溶液
A、将硝酸钾饱和溶液从10℃升温至40℃,仍是饱和溶液 B、40℃时,硝酸钾饱和溶液的溶质质量分数为64% C、30℃,硝酸钾的溶解度为64g D、70℃时,将65g加入到50g水中,形成不饱和溶液 -
7、我国科学家成功研制出可用于外太空核反应堆的钼合金。钼在元素周期表中的部分信息如图所示,下列有关说法正确的是
 A、钼的原子序数为42 B、钼的元素符号为MO C、钼是非金属元素 D、钼原子的质量是95.96g
A、钼的原子序数为42 B、钼的元素符号为MO C、钼是非金属元素 D、钼原子的质量是95.96g -
8、化学源于生活,服务于生活。下列说法中,错误的是A、衣:可用抽丝灼烧的方法鉴别天然纤维和合成纤维 B、食:水果蔬菜中含丰富的维C,适量食用可以预防坏血病 C、住:铝制门窗耐腐蚀,是因为铝的化学性质不活泼 D、行:氢能源车投入使用,即能节约石油资源,又能保护环境
-
9、生产航天服的原料之一是二苯甲烷二异氰酸酯(),关于二苯甲烷二异氰酸酯的说法正确的是A、碳元素的质量分数为: B、碳、氢原子个数比为12∶1 C、含有29个原子 D、由四种元素组成
-
10、液态二氧化氮()能与燃料(如偏二甲肼)反应产生高能推力,用于火箭和导弹发动机,则中氮元素的化合价为A、+4 B、+2 C、+1 D、+3
-
11、下列关于实验室制取气体的常见操作,不合理的是




A.制的试剂
B.制的发生装置
C.检查气密性
D.收集
A、A B、B C、C D、D -
12、化学的发展离不开化学家的贡献。下列说法错误的是A、徐光宪—研究稀土分离技术 B、闵恩泽—研究石油化工催化剂 C、侯德榜—发现抗疟疾药物青蒿素 D、张青莲—测定相对原子质量
-
13、化学用语是学习化学的工具。下列表示3个氧原子的是A、3O B、3 C、 D、
-
14、某饼干包装袋上的部分说明如表,请据此完成下面小题:
商品名称
XX饼干
配料
小麦粉、白砂糖、精炼植物油、鲜鸡蛋、奶油、食盐、膨松剂、碳酸钙、食用香精
储藏方法
存放于阴凉干燥处,避免阳光直射
保质期
270天
(1)、配料表中所含的碳酸钙属于A、酸 B、碱 C、氧化物 D、盐(2)、配料表中富含蛋白质的是A、精炼植物油 B、鲜鸡蛋 C、白砂糖 D、小麦粉 -
15、海昏侯墓出土的青铜蒸馏器(如图)具有极高的历史和文化价值,被视为国宝级文物,该蒸馏器材料属于
 A、合成材料 B、金属材料 C、复合材料 D、天然材料
A、合成材料 B、金属材料 C、复合材料 D、天然材料 -
16、膜蒸馏法是一项具有重大应用前景的海水淡化技术。如图所示,我国科学家研究合成了超高通量纳米多孔石墨烯膜,利用热量驱动水蒸气通过石墨烯膜的纳米级孔隙,实现高效可持续的海水淡化。下列说法不正确的是
 A、石墨烯由碳原子构成 B、光照产生水蒸气的过程中水分子间的间隔变大 C、通过多孔石墨烯膜的过程中水分子体积变小 D、该方法可以缓解淡水资源短缺的问题
A、石墨烯由碳原子构成 B、光照产生水蒸气的过程中水分子间的间隔变大 C、通过多孔石墨烯膜的过程中水分子体积变小 D、该方法可以缓解淡水资源短缺的问题 -
17、2025蛇年除夕,小明一家打算在户外聚餐吃火锅,小明决定自制户外火锅燃料。(1)、选择燃料(表格中所用燃料的质量均相等)
木柴
木炭
固体酒精
点燃难易
中
难
易
燃烧持续性
短
较长
长
燃烧产物
、、
、
、
综上信息,选择作为户外燃料较好。
(2)、自制固体酒精并使用燃料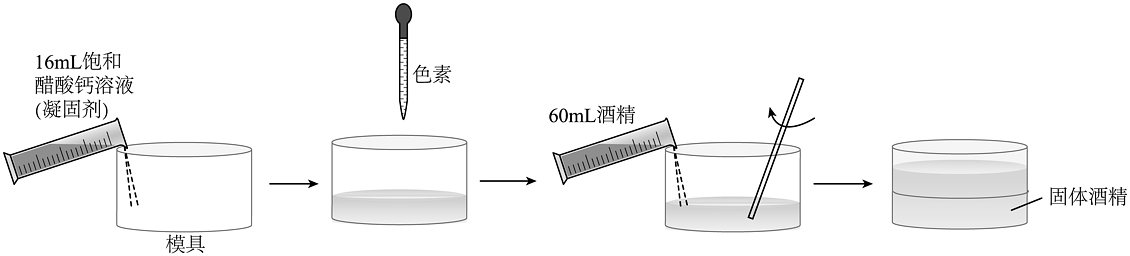
ⅰ.加色素的目的是。
ⅱ.固体酒精属于(填“混合”或“纯净”)物。
ⅲ.使用固体酒精代替液体酒精的优点有(写一条)。
ⅳ.假设小明自制的固体酒精中酒精含量为50%,46g固体酒精中酒精完全燃烧理论上能产生二氧化碳的质量(写出计算过程)。
(3)、将一定质量的酒精与8.8g氧气混合于密闭容器内,在一定条件下反应物完全耗尽,生成一氧化碳和二氧化碳混合气8g,同时生成水。则密闭容器中一氧化碳全部转化为二氧化碳,还需要g氧气。 -
18、一种利用赤泥(主要含)和煤矸石(主要含、及C)协同还原焙烧回收Fe、Al等元素的工艺环节如图所示。
 (1)、赤泥和煤矸石焙烧前进行粉碎的原因是。(2)、“高温焙烧”中,C还原生成Fe的反应,该反应属于(填基本反应类型)。通的目的是。(3)、“磁选分离”属于(填“物理”或“化学”)变化。(4)、赤泥-煤矸石质量比对还原焙烧产物中铁精矿产率以及铁品位值的影响如图所示。若煤矸石比例过高(如质量比2∶8),铁品位小幅下降,但铁精矿产率显著下降,可能的原因是。
(1)、赤泥和煤矸石焙烧前进行粉碎的原因是。(2)、“高温焙烧”中,C还原生成Fe的反应,该反应属于(填基本反应类型)。通的目的是。(3)、“磁选分离”属于(填“物理”或“化学”)变化。(4)、赤泥-煤矸石质量比对还原焙烧产物中铁精矿产率以及铁品位值的影响如图所示。若煤矸石比例过高(如质量比2∶8),铁品位小幅下降,但铁精矿产率显著下降,可能的原因是。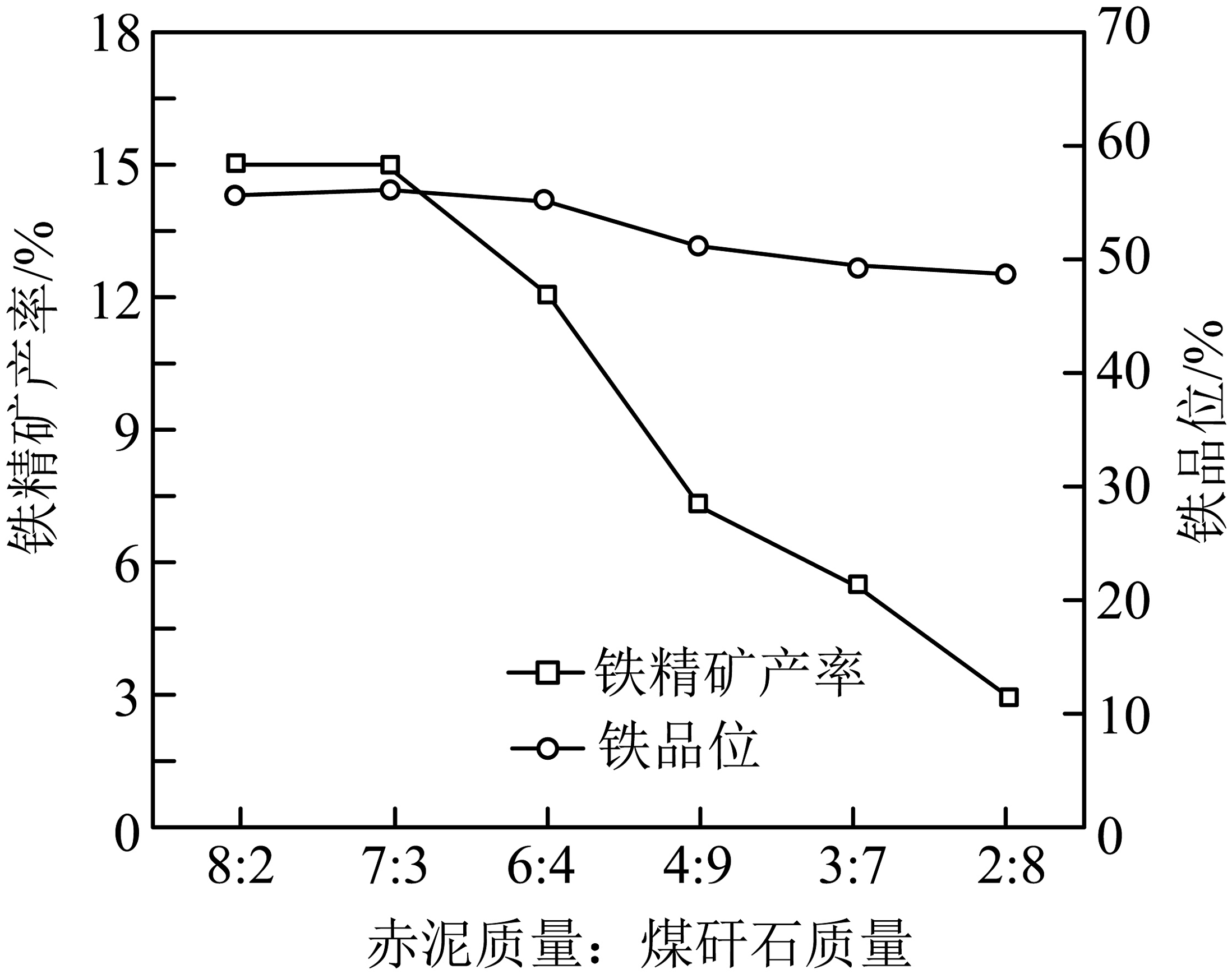 (5)、“酸浸室”中的化学方程式为。“操作1”的名称为。(6)、该工艺的优点有(写一点)。
(5)、“酸浸室”中的化学方程式为。“操作1”的名称为。(6)、该工艺的优点有(写一点)。 -
19、“盐光互补”是一种将光伏发电与盐业生产相结合的新型复合产业模式。兴趣小组开展了与“盐光互补”模式相关的探究活动。(1)、原理:在盐池区域上架设光伏板如图所示,卤水在的照射下反射光线至组件背面,可额外提高发电效益,光伏组件的热效应能显著提高盐池温度,加快卤水蒸发,实现发电与制盐的共赢。
 (2)、产盐:光伏组件的热效应,使产盐过程无需经过蒸发池,大大提高了产盐效率,结晶池中剩余溶液是氯化钠的(填“饱和”或“不饱和”)溶液。(3)、探究:某盐池的主要成分是NaCl,还可能有、中的一种或两种。教师提供模拟结晶池中的晶体。
(2)、产盐:光伏组件的热效应,使产盐过程无需经过蒸发池,大大提高了产盐效率,结晶池中剩余溶液是氯化钠的(填“饱和”或“不饱和”)溶液。(3)、探究:某盐池的主要成分是NaCl,还可能有、中的一种或两种。教师提供模拟结晶池中的晶体。【提出问题】晶体中的成分还有什么?
【作出猜想】想1: 猜想2: 猜想3:
【实验探究】取少量样品分别加入试管A、B中:
实验序号
操作
现象
结论
1
向A中加入适量水溶解,加入过量稀硫酸
含
2
向B中加入适量水溶解,滴加足量的溶液
产生白色沉淀
含
【分析评价】有同学认为实验2结论不够严谨,理由是(用化学方程式解释)
【补充实验】
实验序号
操作
现象
结论
3
向实验2反应后的B试管中滴加足量的
猜想3成立
(4)、交流:与单一产业相比,“盐光互补”产业模式的优点有(多选,填字母)。a.卤水液面反射的太阳辐射,提高了光伏发电量
b.增加盐池吸收的太阳辐射,提高产盐量
c.改变土地利用类型,改善生态环境
d.提高土地利用率,增加经济效益
-
20、2024年4月,我国首次在神舟十八号问天舱以斑马鱼和金鱼藻为研究对象,在轨建立稳定运行的空间自循环水生生态系统:藻类光合作用产生的供鱼呼吸,鱼呼出的二氧化碳供藻类进行光合作用。
(1)的制取及性质
ⅰ.制取
小华欲制备氧气,实验桌上有下列仪器和胶皮管、棉花、火柴以及实验所需药品。
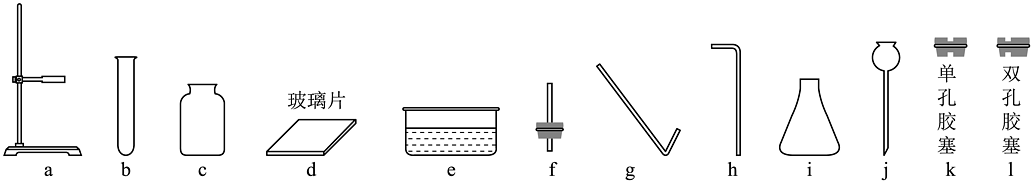
若用高锰酸钾固体制取氧气,还缺少一种仪器(填仪器名称):补全仪器后,小华要制取并收集一瓶纯净的氧气,可选择的仪器a、b、c、d、、k(填标号)。
ⅱ.收集一瓶并进行性质检验
操作
现象
结论

铁丝在氧气中燃烧时,(填字母)
a.剧烈燃烧
b.生成黑色固体
c.火星四射
物质燃烧剧烈程度与有关
(2)化学助力太空养鱼
太空鱼缸水环境的二氧化碳相对匮乏不利金鱼藻生长和光合作用,小华为太空鱼缸设计了二氧化碳补给器。
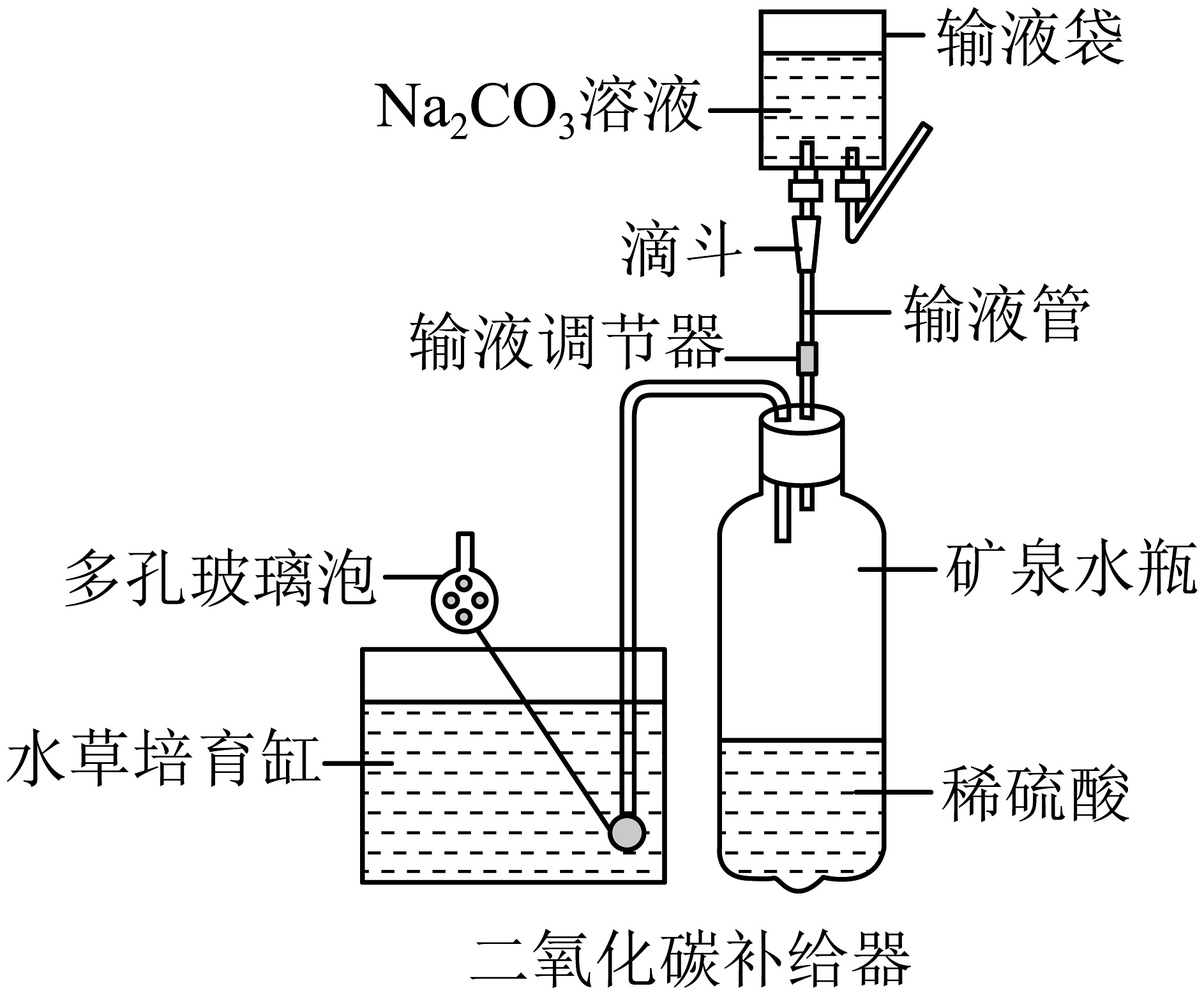
ⅰ.二氧化碳补给器采用溶液和稀硫酸反应,通过观察确定气体的流速,反应化学方程式为。
ⅱ.小华测得鱼缸内溶液酸性增强(pH下降),原因是。
ⅲ.下表是设计评价量表
评价等级
优秀
合格
待改进
评价指标
反应安全,可控,气体能直接排出
气体能直接排出,但不可控制气流速率
气体无法排出,存在较大安全隐患
根据设计评价量表,你对小华设计的二氧化碳补给器评价是。