-
1、将一定浓度且足量的稀盐酸、稀硫酸分别加入装有等质量粉末的容器中,相同条件下测得两者产生的体积(V)与反应时间(t)的关系如图所示。下列判断错误的是( )
 A、反应I、II最终测得的CO2的体积应相同 B、0~100s内,反应I、II生成CO2的速率均先慢后快 C、反应Ⅱ中,0~100s内产生的CO2体积比100~200s内的少5amL D、实验室可以用一定浓度的稀硫酸与CaCO3粉末反应制备CO2
A、反应I、II最终测得的CO2的体积应相同 B、0~100s内,反应I、II生成CO2的速率均先慢后快 C、反应Ⅱ中,0~100s内产生的CO2体积比100~200s内的少5amL D、实验室可以用一定浓度的稀硫酸与CaCO3粉末反应制备CO2 -
2、如图是以铁为核心的物质间的转化关系(部分物质和反应条件已省略),下列说法错误的是( )
 A、转化①②均可通过化合反应来实现 B、转化③不能通过铁丝燃烧实现 C、转化④是高炉炼铁的主要原理 D、转化⑤⑥一定会有气泡产生
A、转化①②均可通过化合反应来实现 B、转化③不能通过铁丝燃烧实现 C、转化④是高炉炼铁的主要原理 D、转化⑤⑥一定会有气泡产生 -
3、物质的分离、鉴别和除杂是重要的实验技能。下列能达到实验目的的是( )
选项
实验目的
实验方法
A
除去CO2中的CO
点燃
B
分离木炭粉和铁粉
加入足量稀盐酸,过滤
C
除去CaO中少量的CaCO3
高温煅烧
D
鉴别CH4和H2
分别点燃,观察火焰颜色
A、A B、B C、C D、D -
4、下列实验方案不能达到相应目的是( )
A
B
C
D




过滤将硬水软化
探究可燃物燃烧的条件
排水法收集二氧化碳
探究铁生锈的条件和空气中氧气的含量
A、A B、B C、C D、D -
5、使用风力、水力及光伏发电电解水制氢是实现氢能全过程清洁化的研究方向。电解水的过程中某电极上发生的微观变化如下图。下列说法正确的是( )
 A、该电极是正极 B、阶段一“●”表示的可能是OH- C、电解水的化学方程式为: D、阶段一到阶段二气泡变大是因为分子的体积变大
A、该电极是正极 B、阶段一“●”表示的可能是OH- C、电解水的化学方程式为: D、阶段一到阶段二气泡变大是因为分子的体积变大 -
6、第十五届全运会由粤港澳三地联合举办,在绿色环保、科技创新、文化融合、全民参与等方面呈现诸多亮点。回答下面小3~5题。(1)、吉祥物“喜洋洋”与“乐融融”铸件全部采用环保再生铜材。铜元素在元素周期表中的信息和原子结构示意图如图所示,下列说法正确的是( )
 A、铜原子中的中子数为29 B、铜属于金属元素 C、铜的原子质量为63.55 D、图中x的数值是2(2)、场馆内的场地标线、赛事标识的印刷,使用的是环保型油墨,它的核心成分之一是乙酸乙酯关于CH3COOC2H5的说法正确的是( )A、乙酸乙酯由碳、氢、氧三个元素组成 B、乙酸乙酯中碳、氢、氧元素的质量比为4:8:2 C、乙酸乙酯分子由4个碳原子、8个氢原子和2个氧原子构成 D、乙酸乙酯的相对分子质量为88(3)、下列有关全运会实践行为的化学知识错误的是( )
A、铜原子中的中子数为29 B、铜属于金属元素 C、铜的原子质量为63.55 D、图中x的数值是2(2)、场馆内的场地标线、赛事标识的印刷,使用的是环保型油墨,它的核心成分之一是乙酸乙酯关于CH3COOC2H5的说法正确的是( )A、乙酸乙酯由碳、氢、氧三个元素组成 B、乙酸乙酯中碳、氢、氧元素的质量比为4:8:2 C、乙酸乙酯分子由4个碳原子、8个氢原子和2个氧原子构成 D、乙酸乙酯的相对分子质量为88(3)、下列有关全运会实践行为的化学知识错误的是( )选项
实践行为
涉及到的化学知识
A
机器人“夸父”以铝合金材质为主体
铝合金硬度大、耐腐蚀、密度小
B
火炬“绽放”以丙烷C3H8为燃料
丙烷具有可燃性
C
游泳场馆用二氧化氯ClO2消毒
发生的是物理变化
D
空气质量检测仪监测PM2.5的含量
PM2.5是大气污染物
A、A B、B C、C D、D -
7、下列化学用语表达正确的是( )A、氯化铁:FeCl2 B、两个氧原子:O2 C、四个硫酸根离子:4SO32- D、锌离子:Zn2+
-
8、“美丽中国我先行”是我国倡导的环保理念之一。下列做法与该理念不相符的是( )A、生活中推广使用一次性筷 B、工业上合理开采矿物 C、农业上合理使用农药和化肥 D、实验室废水需要回收处理
-
9、
回答下列问题:
(1)加热氯酸钾和二氧化锰的混合物可制备氧气,该反应的化学方程式为。
但实验中发现有刺激性气味的气体产生。请你一起参与探究:
【提出问题】刺激性气味的气体是什么呢?
【猜想假设】猜想一:臭氧(化学式为O3) 猜想二:HCl 猜想三:Cl2
(2)同学们认为不需实验验证就可以判断猜想是错误的,理由为。
【查阅资料】①臭氧在MnO2存在情况下极易分解成氧气。
② , AgCl是一种白色沉淀。
【实验探究】
(3)查阅资料后大家认为猜想一是错误的,理由为。
(4)他们进一步又做了如下实验:取氯酸钾和二氧化锰的混合物放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管口(见下图),看到的现象是 , 再将湿润的蓝色石蕊试纸悬于试管口,试纸变色,最终证明猜想三正确。

【反思拓展】
(5)欲证明二氧化锰是氯酸钾分解的催化剂,需证明二氧化锰的在反应前后不变。
(6)自来水厂常用氯气来杀菌消毒,氯气和水反应后会产生H+、Cl-和ClO- , 而野外常用漂白粉[主要成分化学式为Ca(ClO)2.你认为在水中起杀菌消毒作用的离子是。
(7)工业上常采用电解食盐水的方法制取氯气,两电极上分别产生氯气和氢气,同时得到一种重要的碱。请写出该反应的化学方程式:。
-
10、请根据下列实验装置图,回答有关问题。
 (1)、图甲是实验室加热高锰酸钾制取氧气的发生装置,实验时应在试管口塞一团棉花,其作用是。试管中发生反应的化学方程式为。(2)、图乙中标号仪器①的名称是 , 利用图乙进行下列实验:
(1)、图甲是实验室加热高锰酸钾制取氧气的发生装置,实验时应在试管口塞一团棉花,其作用是。试管中发生反应的化学方程式为。(2)、图乙中标号仪器①的名称是 , 利用图乙进行下列实验:Ⅰ:开始先关闭K2 , 打开K1 , 片刻后观察到烧杯中蜡烛燃烧更剧烈,A中发生反应的化学方程式为 , 其中二氧化锰的作用是。
Ⅱ:然后关闭K1 , 打开K2 , 观察到烧杯中蜡烛燃烧不旺直至熄灭,B中发生反应的化学方程式为 , 蜡烛逐渐熄灭说明二氧化碳具有的化学性质是。
(3)、下列三种气体能选用图乙中A作为发生装置的是:(填序号)。气体
药品
条件
①氢气
锌粒和稀硫酸
常温
②氯气
二氧化锰和浓盐酸
加热
③硫化氢
硫化亚铁固体和稀硫酸
常温
-
11、铁黄()是一种颜料,以某硫铁矿废渣(主要成分 , 含有少量的 , 其余成分不考虑)为原料,制取铁黄,以下是制取工艺流程。
注:铁黄不与水反应,不与水和反应
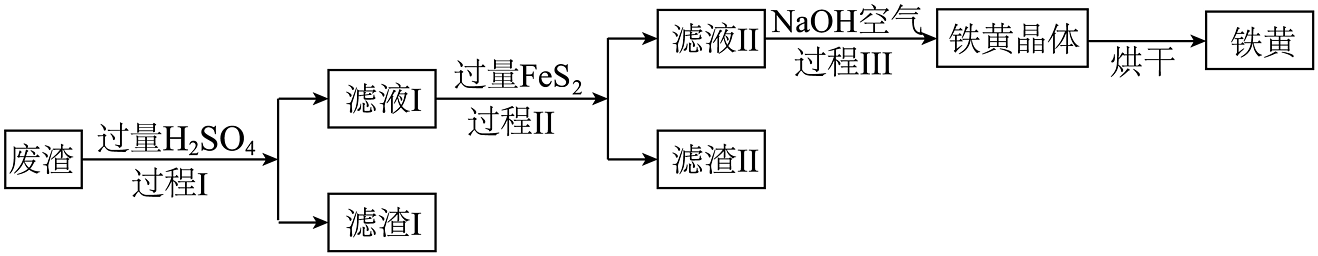 (1)、滤渣I中的物质有(填化学式);(2)、过程Ⅱ的操作名称为;(3)、①随着温度的升高,可以加热分解成和一种常见的溶剂,写出其反应的化学方程式;
(1)、滤渣I中的物质有(填化学式);(2)、过程Ⅱ的操作名称为;(3)、①随着温度的升高,可以加热分解成和一种常见的溶剂,写出其反应的化学方程式;②温度不同时,生成的颜色如下表:
温度/℃
400
700
750
800
颜色
橘红
鲜红
鲜红
暗红
如果想获得鲜红的 , 应把温度控制在。
(4)、用含1.6吨氧化铁的废渣为原料,经过过程I后得到的滤液I中硫酸铁的质量最多为吨。(2分,不需要写出计算过程) -
12、化学存在于我们生活的各个角落,厨房中的化学精彩纷呈。(1)、下列调味品加入水中,能形成溶液的是________(填序号)。A、香油 B、胡椒粉 C、味精(2)、自制汽水时有气泡产生,主要是因为碳酸氢钠和柠檬酸反应生成了气体;摇匀后打开瓶盖,汽水会自动喷出,说明压强 , 气体的溶解度。(3)、小柯和家人在家吃火锅时,发现火锅越吃越咸,原因是随着时间的推移,。(4)、小宇用白糖自制了一杯糖水,为加快白糖的溶解速率,可采取的措施是(写一条)。从微观角度分析,溶液中的白糖以(填“分子”或“离子”)的形式均匀地分散到水中。(5)、生理盐水密封放置一段时间出现浑浊现象,可以立即判断这是不合格产品,这是因为溶液具有性。
-
13、下图是某品牌矿泉水标签的部分说明。
 (1)、水(填“是”或“否”)食品中的营养素。(2)、配料表中硫酸镁的化学式为。(3)、一瓶该矿泉水含钾离子的质量最多为mg。(4)、偏硅酸(H2SiO3)中硅元素的化合价是。
(1)、水(填“是”或“否”)食品中的营养素。(2)、配料表中硫酸镁的化学式为。(3)、一瓶该矿泉水含钾离子的质量最多为mg。(4)、偏硅酸(H2SiO3)中硅元素的化合价是。 -
14、现有乙烯()、乙醛()和乙酸()三种蒸气的混合物共20g,其中碳元素的质量是12g,则混合物中氧元素的质量是( )A、4g B、6g C、7g D、7g~8g之间
-
15、在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的量如下表所示。下列有关说法不正确的是( )
物质
M
N
P
Q
反应前的质量/g
16
24
15
20
反应后的质量/g
x
y
0
10
A、参加反应的P与Q的质量比为3∶2 B、x+y=65 C、当x≤16时,该反应一定是化合反应 D、y的最大值为75 -
16、下列实验方案不能达到实验目的的是A、用Na2CO3溶液鉴别稀盐酸和稀硫酸 B、用带火星的木条检验O2 C、用酚酞试液鉴别蒸馏水和氨水 D、用点燃氢气的方法证明水的组成
-
17、以下是某同学记录的实验现象,其中不符合事实的是A、镁带在空气中燃烧发出耀眼的白光,生成白色固体 B、向鸡蛋清中加入饱和硫酸铵溶液,出现黄色沉淀 C、在氢氧化钠溶液中滴加硫酸铜溶液,产生蓝色沉淀 D、向盛有饱和食盐水的试管中加入少量硝酸钾,振荡后硝酸钾消失
-
18、化学符号是学习化学的重要工具。下列叙述正确的是A、2N表示2个氮原子或2个氮元素 B、食盐水中含有钠离子的符号为Na+ C、居里夫人发现的镭元素符号为Ra2 D、碳酸氢钠的化学式是Na2HCO3
-
19、甲、乙、丙三种固体物质的溶解度曲线如图所示,从中获取的信息正确的是
 A、t1℃时,甲物质中加入50g水,充分溶解后得到60g溶液 B、t2℃时,甲、乙两种溶液所含溶质的质量一定相同 C、t1℃时,甲、丙两种溶液的溶质质量分数均为16.7% D、t2℃时,甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为乙>甲=丙
A、t1℃时,甲物质中加入50g水,充分溶解后得到60g溶液 B、t2℃时,甲、乙两种溶液所含溶质的质量一定相同 C、t1℃时,甲、丙两种溶液的溶质质量分数均为16.7% D、t2℃时,甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为乙>甲=丙 -
20、同种元素形成的不同单质互称同素异形体,下列两种物质属于同素异形体的是A、CO和CO2 B、冰和干冰 C、白磷和红磷 D、汞和水银