-
1、某兴趣小组用硫铁矿烧渣(主要成分为 , 还含少量FeO、、CuO等)制备纯净的溶液(不溶于水和硫酸)。流程如图:
 (1)、稀硫酸与烧渣混合,发生反应的化学方程式为(写出任意一个),该反应属于(填基本反应类型)。(2)、加入溶液将滤液1中的转化为 , 溶液温度不宜过高,原因是在加热条件下容易分解,用化学方程式表示为 , 在该过程中铁元素的化合价(填“升高”、“降低”或“不变”)(3)、加入氨水调节溶液的pH,使、在不同pH条件下沉淀,固体2中物质的化学式为。(4)、化学反应速率受多种因素的影响。下列说法正确的是______。A、将烧渣预先粉碎再加入稀硫酸,可加快反应 B、稀硫酸与烧渣混合后进行搅拌,可加快反应 C、适当提高各反应物的浓度,可加快反应(5)、向中加入稀盐酸,反应的实验现象。
(1)、稀硫酸与烧渣混合,发生反应的化学方程式为(写出任意一个),该反应属于(填基本反应类型)。(2)、加入溶液将滤液1中的转化为 , 溶液温度不宜过高,原因是在加热条件下容易分解,用化学方程式表示为 , 在该过程中铁元素的化合价(填“升高”、“降低”或“不变”)(3)、加入氨水调节溶液的pH,使、在不同pH条件下沉淀,固体2中物质的化学式为。(4)、化学反应速率受多种因素的影响。下列说法正确的是______。A、将烧渣预先粉碎再加入稀硫酸,可加快反应 B、稀硫酸与烧渣混合后进行搅拌,可加快反应 C、适当提高各反应物的浓度,可加快反应(5)、向中加入稀盐酸,反应的实验现象。 -
2、
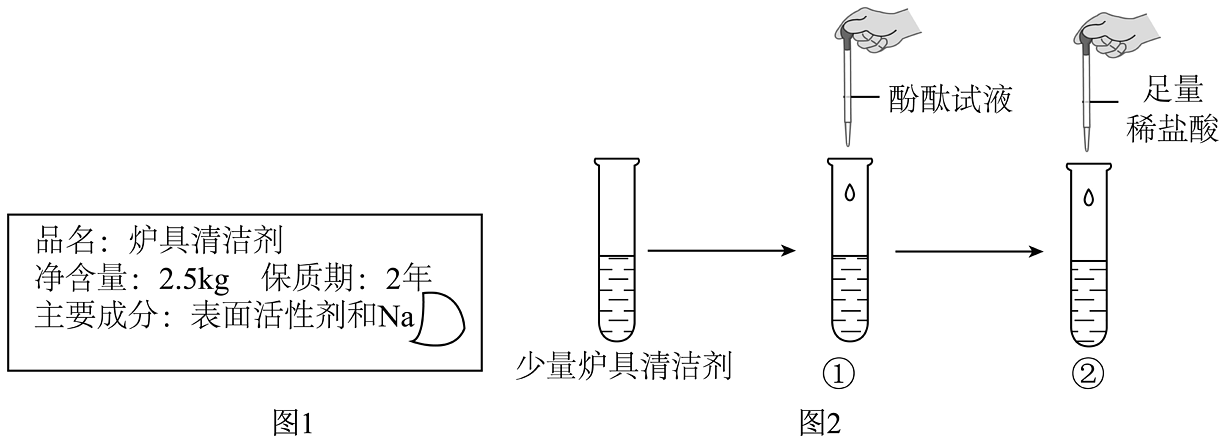
小西家里有一瓶久置的炉具清洁剂。他对该清洁剂的除油污原理、成分及使用方法产生了浓厚兴趣,于是在老师指导下,开启了项目化学习活动。
项目一:了解炉具清洁剂除油污原理
【查阅资料】
表面活性剂属于有机物,常作为家用洗涤剂的有效成分。
【交流讨论】
(1)洗涤剂除油污发生的作用是________(填“乳化”或“溶解”)。
项目二:探究炉具清洁剂的无机物成分
【作出猜想】
根据标签猜测炉具清洁剂的无机物成分为NaOH、或NaCl。
【实验探究】
小西进行了如图2实验:
【实验分析】
(2)观察到①中溶液变红,证明炉具清洁剂的成分不是NaCl。
观察到②中________,证明炉具清洁剂的成分是。
【讨论质疑】
(3)同学们经讨论,认为小西的结论不严谨,原因是如果炉具清洁剂的成分是NaOH,会发生反应________(填化学方程式)而变质,也会产生。
【继续探究】
(4)为了进一步确定该炉具清洁剂的成分,小西进行以下实验。
实验操作
实验现象
实验结论
Ⅰ、取少量炉具清洁剂于试管中,向其中滴加足量的溶液,振荡,静置
a.________
该炉具清洁剂的成分是NaOH,且部分变质
Ⅱ、________
b.________
【实验拓展】
(5)要除去部分变质的NaOH溶液中的杂质,可选择适量的______(填字母)。
A. 溶液 B. 溶液 C. 溶液 项目三:交流炉具清洁剂的使用方法
【反思交流】
(6)根据其主要成分,同学们提出使用炉具清洁剂时要注意的事项:________。
-
3、非物质文化遗产是文化历史的“活化石”。(1)、集烟制墨。松烟墨以松树在密闭燃炉中烧制的烟灰制作,利用了松木的(填“完全”或“不完全”)燃烧;墨加工成的碳素墨水(主要成分为碳)可书写档案并长久保存,由此,你对碳化学性质的认识是。(2)、米酒酿造。高粱研碎、热水浸润后蒸料,加酒曲酶发酵,蒸馏提纯可得米酒。蒸馏过程可用天然气(主要成分为)为燃料,其完全燃烧的化学方程式为。蒸馏是指将液体加热变成蒸汽,再使蒸汽冷凝成液体,除去其中所含杂质,该过程利用酒精与其它成分的不同进行,使酒精先提纯。(3)、烧制陶器。制陶的胚料中若铁粉未被除去,烧制的陶器会出现黑点,这是因为陶土中含有少量的硫,铁粉会与硫在加热条件下化合成硫化亚铁,用化学方程式表示为。氮化物陶瓷中四氮化三硅陶瓷具有较好的抗化学腐蚀性,常用作特殊的机械、介电或导热材料,写出四氮化三硅的化学式。(4)、手工红糖。红糖的主要成分是蔗糖,其中含有钙、铁等多种元素,其中钙是人体所需的(选填“常量”或“微量”)元素。
-
4、实验小组借助传感器对NaOH溶液与稀盐酸的反应进行研究。烧杯中盛放溶液X,向其中匀速滴加另一种溶液,并用磁力搅拌器不断搅拌,实验装置和测定结果如下图所示。下列说法中正确的是
 A、溶液X能使无色酚酞溶液变红 B、0~40s时,溶液中H+数目不断增加 C、M点时两者恰好完全反应,pH=7 D、60s时,溶液中的微观粒子有Na+、Cl-和H2O
A、溶液X能使无色酚酞溶液变红 B、0~40s时,溶液中H+数目不断增加 C、M点时两者恰好完全反应,pH=7 D、60s时,溶液中的微观粒子有Na+、Cl-和H2O -
5、下列有关物品的提纯或鉴别中,所选用的两种方法均正确的是
选项
实验目的
方法和所加试剂
方法一
方法二
A
鉴别羊毛织品和尼龙织品
观察外观
取样,灼烧闻气味
B
鉴别黄金和黄铜(Cu-Zn合金)
浸入硝酸银溶液中
灼烧
C
除去氧化钙中少量碳酸钙
加足量的水,过滤
加适量稀盐酸
D
除去中的少量HCl
通过盛有NaOH的洗气瓶
通过盛有的洗气瓶
A、A B、B C、C D、D -
6、我国科学家研究出碳化钼负载金原子的高效催化体系(钼的元素符号为Mo),使水煤气中的CO和在120℃下发生反应,为获得氢能提供新思路,反应微观模型如图所示。下列说法正确的是
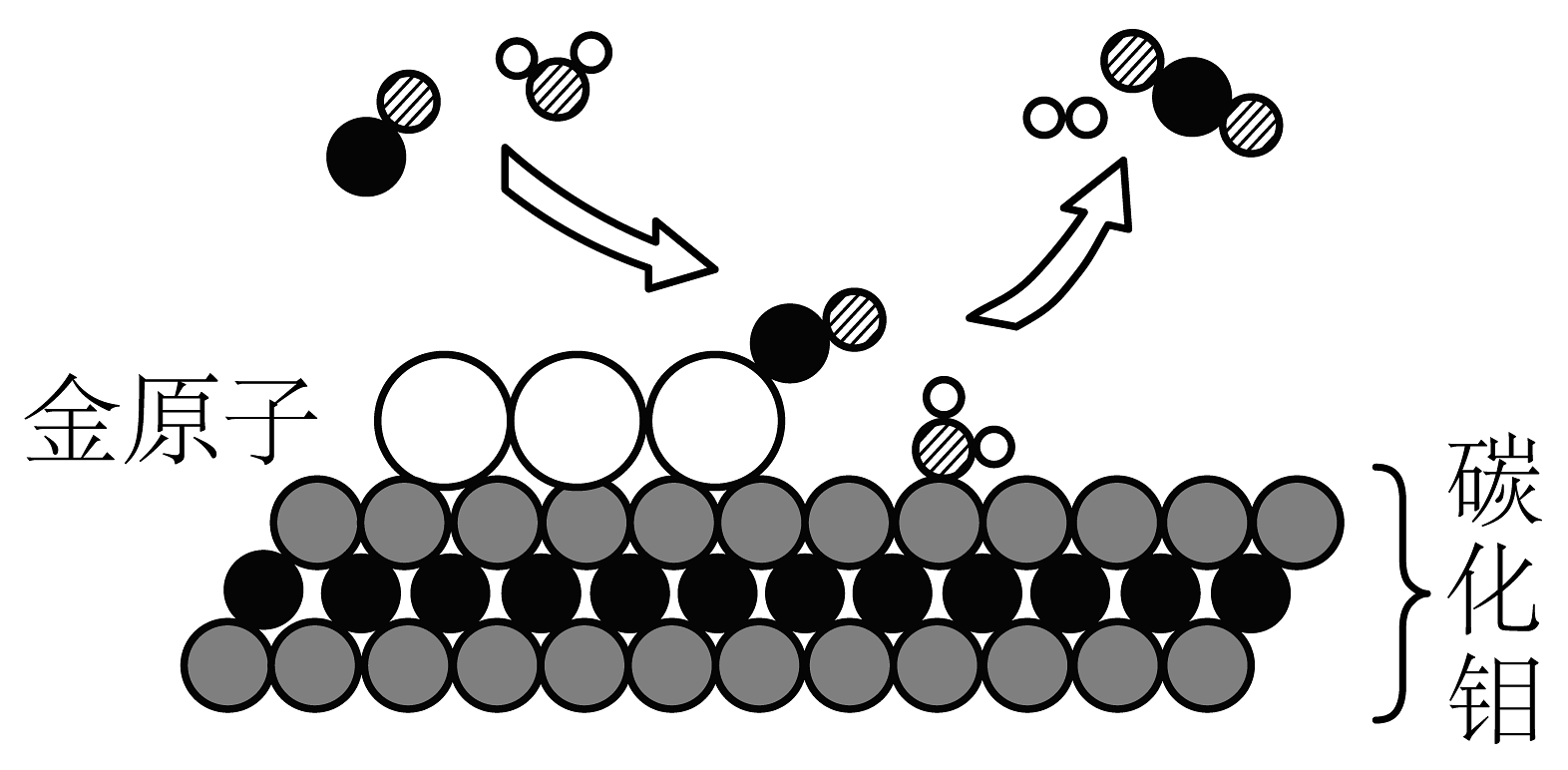 A、该反应属于置换反应 B、从上图可知,碳化钼的化学式为 C、参加反应的CO与质量比为1:1 D、反应中金原子吸附水分子并催化反应
A、该反应属于置换反应 B、从上图可知,碳化钼的化学式为 C、参加反应的CO与质量比为1:1 D、反应中金原子吸附水分子并催化反应 -
7、据《Science》杂志报道,科学家合成了一种环状物质 , 这种物质具有广泛的应用前景。下列有关说法正确的是A、属于有机物 B、环状碳分子间不存在间隔 C、是由18个碳原子构成的 D、和都是由分子构成的单质
-
8、铜在电气工业中有非常重要的用途。结合图中信息,下列叙述正确的是
 A、黄铜片的硬度比纯铜片小 B、铜元素位于元素周期表中第四周期 C、铜的原子序数为29,其相对原子质量为63.55g D、铜原子的最外层只有1个电子,所以它在化合物中只能显+1价
A、黄铜片的硬度比纯铜片小 B、铜元素位于元素周期表中第四周期 C、铜的原子序数为29,其相对原子质量为63.55g D、铜原子的最外层只有1个电子,所以它在化合物中只能显+1价 -
9、下列化学用语正确的是A、高锰酸钾 B、硫酸根离子 C、3Pb表示3个铅元素 D、氧化铁FeO
-
10、下列不属于合成材料的是A、顺丁橡胶 B、蚕丝 C、聚氯乙烯 D、涤纶
-
11、化学是能源科学、环境科学、航空航天工程等现代科学技术的基础。(1)、社会发展离不开优质能源开发。下列属于可再生能源的是(填字母)。
a. 煤
b.石油
c. 氢气
d. 天然气
(2)、能源转型是人类进步的驱动力,家用燃料的变迁承载了社会文明发展的需求。某兴趣小组通过调查家用燃料的变迁与合理使用,绘制了下图所示的家用燃料变迁图。请完成下列问题。

①点燃煤时常用柴草引燃,说明可燃物燃烧需要的条件之一是
②天然气主要成分是甲烷。甲烷完全燃烧的化学方程式为
③天然气作为一种比较清洁的燃料,已经走进城乡居民生活。与燃煤相比,使用天然气可以减少的空气污染物是(填一种即可)。
(3)、CO2捕集是实现低碳目标的一种有效手段,某捕集CO2工艺流程如下图所示。
①捕捉室中采用“喷淋”方式加入NaOH溶液,请叙述“喷淋”方式的优点。
②写出反应分离室中生成NaOH的化学方程式。
③以上工艺流程中不涉及的化学反应基本类型是
(4)、新能源在我国航天科技领域有着广泛的应用,火箭发射卫星时常用液氢和液氧作推进剂。要将卫星送达预定轨道,某型火箭至少需要燃烧220kg的液氢才能提供足够的能量。理论上该火箭需要携带液氧的质量是多少? -
12、实验室制取气体的常用装置如下图所示,请回答下列问题。
 (1)、制取O2 , 和CO2可选用相同的发生和收集装置,该套装置为(填字母)。(2)、写出实验室用装置B制取O2的化学方程式。(3)、若用虚线框内装置干燥CO2气体,请将该装置图补画完整。
(1)、制取O2 , 和CO2可选用相同的发生和收集装置,该套装置为(填字母)。(2)、写出实验室用装置B制取O2的化学方程式。(3)、若用虚线框内装置干燥CO2气体,请将该装置图补画完整。 -
13、某同学设计下图所示装置进行实验(夹持仪器略去,K1、K2均关闭)。打开K1),待液体全部流下,关闭K,观察到烧杯中的溶液变浑浊;充分反应后,打开K1、K2使液体全部流人锥形瓶,瓶中无明显现象。
 (1)、用化学方程式说明烧杯中的溶液变浑浊的原因。(2)、充分反应后,取锥形瓶中的溶液,测得pH=4。写出该溶液中溶质的成分。
(1)、用化学方程式说明烧杯中的溶液变浑浊的原因。(2)、充分反应后,取锥形瓶中的溶液,测得pH=4。写出该溶液中溶质的成分。 -
14、为探究金属活动性,某同学利用下图所示装置进行实验。将足量常见金属M加入到Y形试管右管中,观察到溶液逐渐变蓝;充分反应后,倾斜Y形试管,使右管中溶液进人左管,观察到溶液蓝色变浅直至消失。
 (1)、判断M可能是什么金属。(2)、用化学方程式说明左管中溶液蓝色消失的原因。(3)、根据实验判断锌、银、M的金属活动性由强到弱的顺序。
(1)、判断M可能是什么金属。(2)、用化学方程式说明左管中溶液蓝色消失的原因。(3)、根据实验判断锌、银、M的金属活动性由强到弱的顺序。 -
15、古代经典诗词、书画精品是中华民族传统文化的瑰宝。(1)、从分子的角度解释唐代诗句“山城斜路杏花香”所描述的现象。(2)、元代著名水墨画《富春山居图》保存至今不变色的原因是什么?
-
16、郑州古荣镇发现的汉代冶铁遗址,证实中原炼铁历史悠久。炼铁高炉内主要物质间转化关系如下图所示(“一”表示物质间能反应,“→”表示反应一步实现,部分物质和反应条件已略去)。已知B为固体燃料,C为赤铁矿的主要成分。
写出物质A在生产、生活中的一种用途:;A转化为D的化学方程式为;C与D反应的化学方程式为

-
17、常温下,铝与氧气反应的化学方程式为;取6.2g部分被氧化的铝粉,加入150g19.6%的稀硫酸,恰好完全反应,则被氧化的铝的质量为g。
-
18、人们常从海水中获得粗盐,早期多采用“天日曝晒,自然结晶,集工采捞”的卤水制盐
方式。结合右图所示的溶解度曲线,回答下列问题。
(1)、通过“曝晒”析出粗盐的原理是结晶;从卤水中“采捞”粗盐与实验操作中的原理类似。(2)、得到的粗盐中含有少量可溶性杂质,可用NaCl饱和溶液反复冲洗除去,选用NaCl饱和溶液的原因是(3)、20℃时,NaCl饱和溶液中溶质质量分数为(只写计算式)。 -
19、某反应微观示意图如右图所示。甲中氮、氢元素质量比为;反应中有种单质;生成丙、丁的分子个数比为

-
20、电解水的实验装置如右图所示。电解一段时间后,可以观察到管a中液面(填“高于”或“低于”)管中液面;关闭电源,将燃着的木条放在管b尖嘴口,打开活塞,可观察到的实验现象是
