-
1、气体的实验室制备是学生必备的实验技能,以下是实验室用于制取气体的部分装置,回答下列问题。
 (1)、仪器①的名称为。(2)、实验室用于制取二氧化碳的药品是 , 反应的化学方程式为。用装置B制取 , 连接装置B、F(竖直放置),当装置B中发生反应一段时间后观察到(填“甲”或“乙”)处燃着的火柴先熄灭。(3)、能用装置C收集氧气,是因为。当观察到时,再把导管口伸入装置C的集气瓶中开始收集氧气。(4)、实验室制取下列气体,可以用图A作为发生装置的有______(填字母序号)。A、电石(固体)和水在常温下反应制乙炔气体 B、氯化铵(固体)和熟石灰共热制氨气 C、浓盐酸(液体)和二氧化锰共热制氯气
(1)、仪器①的名称为。(2)、实验室用于制取二氧化碳的药品是 , 反应的化学方程式为。用装置B制取 , 连接装置B、F(竖直放置),当装置B中发生反应一段时间后观察到(填“甲”或“乙”)处燃着的火柴先熄灭。(3)、能用装置C收集氧气,是因为。当观察到时,再把导管口伸入装置C的集气瓶中开始收集氧气。(4)、实验室制取下列气体,可以用图A作为发生装置的有______(填字母序号)。A、电石(固体)和水在常温下反应制乙炔气体 B、氯化铵(固体)和熟石灰共热制氨气 C、浓盐酸(液体)和二氧化锰共热制氯气 -
2、
柠檬酸亚铁是一种补血剂,易溶于水,难溶于乙醇。某科研小组在实验室研究制备柠檬酸亚铁。
Ⅰ.制碳酸亚铁
用预处理后的硫铁矿烧渣(主要成分 , 含少量不溶性杂质)制备碳酸亚铁的流程如图:

已知:a.;b.在碱性条件下生成沉淀。
(1)“酸浸”时发生的化学反应方程式为。
(2)“操作X”是为了除去过量铁粉和不溶性杂质。“操作X”是(填操作名称),该过程中玻璃棒的作用是。
(3)“沉铁”时,反应原理为。
①实验时需将溶液滴入溶液中,而不能反向滴加,其原因是。
②待完全反应后,过滤,洗涤。洗涤前,沉淀表面吸附的主要杂质是(填化学式)。
Ⅱ.制柠檬酸亚铁
(4)用如图所示装置制备柠檬酸亚铁:
步骤1:在三颈烧瓶中加入一定质量固体、少量铁粉及足量柠檬酸溶液,控制温度约 , 搅拌,充分反应;
步骤2:将所得混合溶液加热浓缩,加入适量无水乙醇,静置,过滤,洗涤,干燥,得到柠檬酸亚铁晶体。

①制备原理为 , 物质X是(填化学式)。
②实验所得柠檬酸亚铁的质量大于根据原理计算所得的质量,原因是。
-
3、Ⅰ.金属材料在生产生活中有广泛的用途,人类的生产生活离不开金属。
为验证铁、铜、银的金属活动性顺序,用如图所示装置进行实验,待Y型管左端充分反应后,缓慢倾斜Y型管,使左侧溶液全部倒入右侧。
 (1)、B中Y型管左端可观察到的现象为。(2)、能达到实验目的的是(填字母),该实验倾斜Y型管后发生反应的化学方程式为。(3)、将一定量的锌粉加入到硝酸银、硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸无气泡产生,则下列叙述中完全正确的组合是。
(1)、B中Y型管左端可观察到的现象为。(2)、能达到实验目的的是(填字母),该实验倾斜Y型管后发生反应的化学方程式为。(3)、将一定量的锌粉加入到硝酸银、硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸无气泡产生,则下列叙述中完全正确的组合是。①滤渣中一定含有银,一定不含有铜
②滤液中的溶质一定含有硝酸锌,一定不含有硝酸银
③若滤液为蓝色,则滤液中的溶质一定含有硝酸铜和硝酸锌
④若滤液为无色,则滤渣中一定含有银和铜,滤液中的溶质一定只含有硝酸锌
A.①② B.②③ C.③④ D.①④
-
4、
我国承诺于2030年前实现“碳达峰”,2060年前实现“碳中和”,体现了大国责任与担当。
任务一:了解二氧化碳排放
(1)空气中的主要来自于化石燃料的燃烧等,大气中过多会导致的加剧。
任务二:学习二氧化碳捕集技术
【捕集技术一】加氢制甲醇双金属纳米催化剂及工艺:

(2)电解水时,若与电源极相连的电极上产生氢气,理论上同时能得到L氧气。写出电解水的化学方程式。
(3)与在一定条件下反生成甲醇和水,该反应的化学方程式是。
【捕集技术二】与转化为
与在一定条件下转化为(反应过程如图,虚线处部分中间产物略去),可实现的再利用。

(4)该反应中,除外的另一种生成物是(填物质名称)。
(5)理论上该反应过程中(填“需要”或“不需要”)不断补充。
任务三:研制低碳行动方案
(6)低碳行动涵盖国际合作、国家工程和个人行为三个层面。请从“个人行为”层面践行“低碳行动”,写出你的一个行动打算:。
-
5、中国传统五色代表物有桃红、凝脂、缃叶、群青、沉香。(1)、群青:取自青金石(主要含Na、Al、Si、O、Ca等元素),各种元素最本质的区别是不同。(2)、桃红:古代的桃红胭脂由红花汁(内有红花素)制成,下列说法正确的有______。A、红花素属于含氧化合物 B、红花素由15个原子、12个氢原子、6个氧原子构成 C、红花素中碳元素与氧元素质量比为(3)、凝脂:从青瓷变为白瓷(降低原料中含铁氧化物的含量)。如图为铁元素的价类二维图,c物质名称为。
 (4)、缃叶:本身指淡黄色的叶子,是桑叶初生的色泽。桑蚕丝织锦的过程中,发生的是变化。(填“物理”或“化学”)(5)、沉香:代表黑色。灰黑色石墨与无色透明金刚石物理性质有差异的原因。
(4)、缃叶:本身指淡黄色的叶子,是桑叶初生的色泽。桑蚕丝织锦的过程中,发生的是变化。(填“物理”或“化学”)(5)、沉香:代表黑色。灰黑色石墨与无色透明金刚石物理性质有差异的原因。 -
6、坐标曲线在多个学科中都有广泛的应用,它能形象直观地反应物理量之间的规律和关系。下列坐标图像能正确反映其对应关系的是
 A、①表示将一定量的60℃硝酸钾饱和溶液冷却至室温 B、②表示在盛有空气的密闭容器(体积不变)中点燃足量红磷 C、③表示向加的试管和未加的试管分别加入等质量等浓度的溶液 D、④表示向一定量的硫酸亚铁溶液中加入锌粉
A、①表示将一定量的60℃硝酸钾饱和溶液冷却至室温 B、②表示在盛有空气的密闭容器(体积不变)中点燃足量红磷 C、③表示向加的试管和未加的试管分别加入等质量等浓度的溶液 D、④表示向一定量的硫酸亚铁溶液中加入锌粉 -
7、下列实验操作中,能达到实验目的的是
选项
物质
实验操作或方法
A
检验某固体是否为碳酸盐
取样,滴加足量稀盐酸,观察是否有气泡
B
除去溶液中少量的HCl
加入过量的碳酸钙,过滤
C
鉴别一氧化碳和二氧化碳
闻气味
D
分离铁粉和硫酸铜粉末
溶解、过滤,滤渣洗涤干燥;滤液蒸发结晶
A、A B、B C、C D、D -
8、证据推理是学习化学的重要方法,下列推理正确的是A、化学反应前后物质总质量不变,则5g碳和5g氧气反应生成10g二氧化碳 B、合金中一定含有金属元素,氧化铜中也含有金属元素,则氧化铜是一种合金 C、碱溶液的pH大于7,则pH大于7的溶液一定是碱性溶液 D、由金属阳离子和酸根阴离子构成的化合物属于盐,则盐一定含有金属元素
-
9、甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是
 A、图中P点表示10℃时丙的饱和溶液 B、10℃时,甲、乙、丙三者的溶液,丙溶液的溶质质量分数最大 C、20℃时,甲、乙、丙饱和溶液降温至10℃,甲溶液中析出固体最多 D、20℃时,向130g乙的饱和溶液加入20g水,所得溶液溶质质量分数变为20%
A、图中P点表示10℃时丙的饱和溶液 B、10℃时,甲、乙、丙三者的溶液,丙溶液的溶质质量分数最大 C、20℃时,甲、乙、丙饱和溶液降温至10℃,甲溶液中析出固体最多 D、20℃时,向130g乙的饱和溶液加入20g水,所得溶液溶质质量分数变为20% -
10、在抗战时期,中国军民用含有硝酸钠和硝酸钙的硝土和草木灰(主要成分)制出硝酸钾后,掺入硫粉和木炭,造出大量土地雷,有效的打击了敌人。该过程涉及的物质中,属于化合物的有A、硝酸钠 B、草木灰 C、硫粉 D、木炭
-
11、电动汽车使用的锂离子电池中含有 , 其中锂元素和铁元素的化合价分别为+1和+2,则磷元素的化合价为A、-1 B、-2 C、+5 D、+6
-
12、如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息。下列说法正确的是
 A、硫原子的相对原子质量为32.06g B、氧原子核外有6个电子 C、氧原子在化学反应中易失去2个电子 D、硫、氧均属于非金属元素
A、硫原子的相对原子质量为32.06g B、氧原子核外有6个电子 C、氧原子在化学反应中易失去2个电子 D、硫、氧均属于非金属元素 -
13、实验室用溶质质量分数为6%的NaCl溶液(密度为)稀释得到50g溶质质量分数为3%的NaCl溶液。下列说法中正确的是A、实验的主要步骤为计算、称量、溶解 B、所需玻璃仪器主要有烧杯、漏斗、玻璃棒、量筒 C、量取浓溶液时俯视量筒读数会导致所配溶液中溶质质量分数偏小 D、往烧杯中加水时有水洒出会导致所配溶液中溶质质量分数偏小
-
14、“爆竹声中一岁除,春风送暖入屠苏”描绘了春节喜庆祥和的气氛。爆竹火药成分中能燃烧产生气体的物质是A、硫粉 B、镁粉 C、红磷 D、铁粉
-
15、人类的日常生活和工农业生产离不开水。下列关于水的叙述不正确的是A、海水淡化是解决水资源危机的途径之一 B、自来水的生产过程包括蒸馏 C、天然水经系列处理后得到的自来水是混合物 D、工业污水要经过净化处理达标后再排放
-
16、下列有关氧气的说法正确的是A、氧气具有可燃性 B、氧气的化学性质很不活泼 C、液氧与氧气化学性质相同 D、过氧化氢中含有氧分子
-
17、化学研究的是物质,下列物质或物质的主要成分对应的化学式不正确的是A、食盐——NaCl B、小苏打——NaHCO3 C、铁锈——Fe3O4 D、干冰——CO2
-
18、下列图标中,表示“严禁烟火”的是A、
 B、
B、 C、
C、 D、
D、
-
19、清洗瓜果、蔬菜表面残留的农药、细菌等关系人体健康。小东利用鸡蛋壳和食盐自制天然果蔬清洗粉,制作过程如图所示。
 (1)、从物质分类角度看,自制天然果蔬清洗粉属于(填“纯净物”或“混合物”)。(2)、已知鸡蛋壳含碳酸钙 90%,求 100g 鸡蛋壳完全煅烧生成蛋壳煅烧粉的质量(写出计算过程)。(3)、自制果蔬清洗粉加入水中会热量(填“放出”或“吸收”)。小东探究成分比例不同的果蔬清洗粉除去甲胺磷和氧化乐果两种杀虫剂的效果,实验数据如图乙所示,则食盐和蛋壳煅烧粉的最佳用量比例为。(4)、甲胺磷和氧化乐果两种杀虫剂呈酸性,自制果蔬清洗粉能高效去除这两种杀虫剂的原因可能是(写一种)。
(1)、从物质分类角度看,自制天然果蔬清洗粉属于(填“纯净物”或“混合物”)。(2)、已知鸡蛋壳含碳酸钙 90%,求 100g 鸡蛋壳完全煅烧生成蛋壳煅烧粉的质量(写出计算过程)。(3)、自制果蔬清洗粉加入水中会热量(填“放出”或“吸收”)。小东探究成分比例不同的果蔬清洗粉除去甲胺磷和氧化乐果两种杀虫剂的效果,实验数据如图乙所示,则食盐和蛋壳煅烧粉的最佳用量比例为。(4)、甲胺磷和氧化乐果两种杀虫剂呈酸性,自制果蔬清洗粉能高效去除这两种杀虫剂的原因可能是(写一种)。 -
20、赤泥(主要含Fe2O3)和煤矸石 [主要含 Al2Si2O5(OH)4] 是典型的矿业固体废物,采用协同还原焙烧有助于实现其所含 Fe、Al 等元素的回收。工艺流程如图1所示。
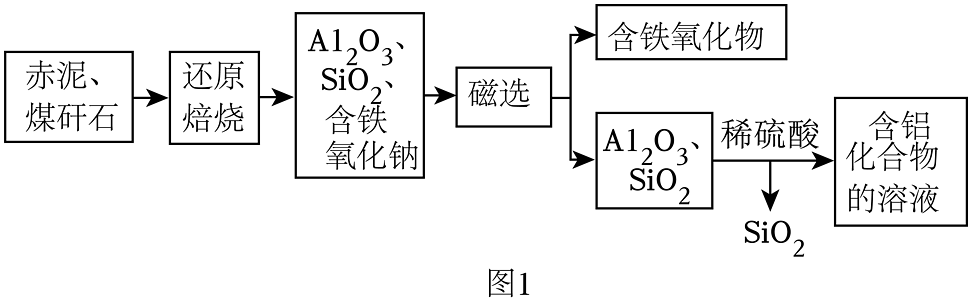
【查阅资料】①磁选是利用不同物质对磁场的反应不同,对物质进行分选;②Fe、Fe3O4能被磁铁吸引,FeO、Fe2O3不能被磁铁吸引。
(1)、赤泥和煤矸石焙烧前进行粉碎的目的是。(2)、Al2Si2O5(OH)4中Si、O原子的个数比为 , 其焙烧过程中会生成3种氧化物Al2O3、SiO2和。从上述流程中可得出 SiO2的一条化学性质为。(3)、加入稀硫酸反应的化学方程式为。(4)、Fe2O3进行还原焙烧时固体中铁元素质量分数随温度变化情况如图2所示。
ⅰ.m、n 点物质分别为、。
ⅱ.为了使含铁氧化物满足磁选需求,焙烧温度 T 应选择的范围是(填序号)。
A.100℃<T<400℃
B.400℃≤T<670℃
C.670℃≤T≤800℃