相关试卷
- 广东省清远市2016-2017学年九年级化学一模考试试卷
- 广西钦州港经济开发区2015-2016学年九年级上学期化学期末考试试卷
- 广西北海市合浦县教育局教研室2013-2014学年九年级上学期化学期末考试试卷
- 广西北海市合浦县2012-2013学年九年级上学期化学期末考试试卷
- 广东省肇庆市鼎湖中学2017-2018学年九年级上学期化学期中考试试卷
- 2016年广西钦州市中考化学试题
- 2015年广西钦州市中考化学试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西钦州地区2016-2017学年九年级化学中考模拟考试试卷
-
1、湖南是美食之乡,下列美食制作过程中,主要发生化学变化的是A、长沙臭豆腐发酵 B、永州东安鸡切配 C、湘西腊肉切片 D、衡阳鱼丸子捏制
-
2、古籍《天工开物》曾记载炼锡(Sn)的原理:。若要炼制11.9t的锡,计算理论上需要的质量(写出计算过程)。
-
3、市面上有一种名为“炸包”的整蛊玩具,由于其能产生一定的“爆炸”效果,从而深得中小学生喜爱。某校化学小组的同学对该玩具产生了浓厚的兴趣,在老师的指导下,他们对炸包展开了一系列探究。(1)、任务一:炸包爆炸的原因分析
在炸包内,隐藏着一个小塑料袋,用手捏破塑料袋后,炸包会迅速膨胀,产生“爆炸”效果。结合教材学过的实验原理分析炸包在其有限的塑料包装内引发爆炸的原因是。
(2)、任务二:探究炸包的成分同学们在实验室经老师指导拆解了一枚炸包玩具,发现里面是一包白色固体和一包无色透明液体。
【查阅资料】碳酸氢钠固体受热易分解,生成碳酸钠、二氧化碳和水,碳酸钠受热不分解。
【猜想假设】根据爆炸原理和拆包现象,同学们对炸包的成分做了如下整理和推测:
猜测一
猜测二
猜测三
白色固体
碳酸盐或碳酸氢盐
无色透明液体
酸
【进行实验】取少量无色透明液体于试管中,滴加 , 溶液变为红色,猜测三正确。
【实验反思】同学们结合所学知识分析,若使用猜测一或猜测二的试剂可能会造成安全事故,其原因是。
【实验探究】在老师的指导下,同学们推测出白色固体的成分可能是、、中的一种,并设计了如下实验进行验证:
实验操作
实验现象
实验结论
①取适量白色固体于烧杯中,加足量蒸馏水充分搅拌后静置
白色固体成分中不含
②取少量①中溶液于试管中,滴加足量
有气泡冒出
白色固体的成分为或
同学们用炸包内的白色固体又设计了如下实验进一步探究,观察到澄清石灰水变浑浊。

【实验结论】由此可得出炸包内的白色固体为碳酸氢钠,图中右侧试管中发生反应的化学方程式为。
(3)、任务三:分析炸包选用磷酸氢钠的原因【信息检索】
①钠盐与酸反应速率比钙盐与酸反应速率快;
②小组同学在老师的帮助下,从相关厂家获取了部分碳酸盐和碳酸氢盐的价格,如下表:
盐的种类
价格(元/吨)
1800
700
1700
7500
【交流讨论】
①从原料成本、反应速率角度分析炸包玩具选用碳酸氢钠的原因是。
②有同学了解到,炸包玩具使用的酸为柠檬酸,柠檬酸是天然的防腐剂和食品添加剂,但部分炸包玩具商家为了压低成本,使用了具有腐蚀性和挥发性毒气的工业废酸,容易导致呼吸道强酸中毒,接触后易腐蚀皮肤。同时,市面上还有数量可观的“危险玩具”具有非常大的安全隐患。这对青少年及家长选购或使用玩具引发的启示有。
-
4、铜是人类最早冶炼与使用的金属。(1)、下表记录了《考工记·六齐》的部分配料比及对应配料比的青铜器的硬度。
《考工记》配料比
含铜量
含锡量
硬度(HB)
钟鼎之齐:六分其金而锡居一
85.71
14.29
140~150
斧斤之齐:五分其金而锡居一
83.33
16.67
150~170
戈戟之齐:四分其金而锡居一
80
20
190~210
①据表分析,青铜器中锡的含量越高,制成器物的硬度就越 , 某铜锡合金中含铜80%、含锡20%,最适合制造的器具是。
②为降低熔炼的温度,青铜在冶炼过程中熔入锡的原理是。
(2)、黄铜是锌铜合金,某化学兴趣小组为探究铁、锌、铜三种金属的活动性强弱,设计了如图1所示实验:能证明锌的金属活动性比铜强的依据是;为达到实验目的,请在图1中补充试管C中所需试剂。 (3)、古法炼铜以孔雀石和木炭为原料,流程如图2所示。
(3)、古法炼铜以孔雀石和木炭为原料,流程如图2所示。①孔雀石的主要成分为碱式碳酸铜 , 加热可分解为三种氧化物,请写出该反应的化学方程式:。
②球形容器封盖后保留细小通气孔的目的是。
③上述流程中,木炭的作用有两个:、直接与氧化铜反应生成铜。
(4)、“乌铜走银”是我国特有的铜制工艺技术,迄今已有300余年的历史。该工艺的废料经初步处理后可得到硝酸银和硝酸铜的混合溶液,向其中加入一定量的金属锌,充分反应后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,有气泡产生,则滤液中含有的溶质为(填化学式)。 -
5、溶液与人类的生产生活关系紧密。(1)、图1是利用海水提取粗盐的过程。

①图1中I是(选填“蒸发”或“冷却”)池,其中质量逐渐减少的物质是(填化学式)。
②析出晶体后的“母液”是对应温度下氯化钠的(选填“饱和”或“不饱和”)溶液。
(2)、若配制溶质质量分数为的溶液,需要水的体积为(水的密度以计)。(3)、如图2为“联合制碱法”涉及的部分物质的溶解度曲线。
①20℃时,的溶解度(选填“大于”或“小于”)NaCl的溶解度。
②50℃时,将等质量和的饱和溶液分别降温到 , 析出晶体质量较多的是(选填“”或“NaCl”)。
③40℃时,将100g溶质质量分数为20%的溶液变为该温度下的饱和溶液,至少应向溶液中再加入固体。
-
6、
古代哲学家认为,气乃万物之源。了解常见气体的发现历程、制备原理,可以更好地为人类服务。
【气体的发现】
(1)早在唐代人们就发现加热火硝能产生“阴气”(即),该“阴气”所属的物质类别是。
【实验室制气】实验室制取气体的装置如图1所示。

(2)仪器a的名称是。
(3)实验室用过氧化氢溶液分解制取氧气,应选择的发生装置是(填字母序号),反应的化学方程式为;相较于装置,用装置收集气体的优点是。
【工业制气】
(4)工业上一般用除尘净化后的空气制取氧气,工业上制取氧气以空气为原料的主要优点是。
【家庭制气】
(5)家用小型制氧机利用分子筛可将氧分子从空气中“筛”出来,从而获得高浓度的氧气,其原理示意图如图2,该方法相当于化学实验中的操作。

-
7、阅读下列材料,分析并回答问题:
氢能是一种绿色低碳、应用广泛的二次能源,与化石能源不同,其难以直接从自然界获取。目前,按照制取方式,制氢的过程可分为三种,通过化石能源燃烧产生氢气,在生产过程中会有二氧化碳的排放,叫作灰氢;利用化石能源制氢,在产生温室气体的同时,会使用碳捕捉、碳封存等技术,从而实现低碳排放生产,是蓝氧;通过核能、太阳能、风能等发电进行电解水制氢,完全没有碳排放,叫作绿氢,绿氢成本较高。分解水法制氢的能量转化如图1,2022年全球制氢路线占比如图2,预测我国2050年氢气来源分布如图3。
 (1)、化石能源主要包括。(2)、材料中涉及的电解水产生绿氢用到的能源有(至少写两种);绿氢相比于灰氢的优点是。(3)、图1中光分解水制氢过程中太阳能转化为能,该反应的化学方程式为。(4)、根据图2和图3,可以得到的信息是(写一条)。
(1)、化石能源主要包括。(2)、材料中涉及的电解水产生绿氢用到的能源有(至少写两种);绿氢相比于灰氢的优点是。(3)、图1中光分解水制氢过程中太阳能转化为能,该反应的化学方程式为。(4)、根据图2和图3,可以得到的信息是(写一条)。 -
8、化学与我们的衣、食、住、行息息相关。(1)、衣:某西服面料成分为羊毛80%、涤纶20%,其中属于合成材料的是(选填“羊毛”或“涤纶”)。(2)、食:贵州常见农家菜有“辣子鸡”“黑木耳炒肉”等。鸡肉中富含的营养物质是;黑木耳中含有钙元素和铁元素,常吃黑木耳可有效预防(填字母序号)疾病的发生。
A.甲状腺肿大 B.发育迟缓 C.骨质疏松 D.贫血
(3)、住:建造房屋使用的大理石的主要成分是碳酸钙,如图为钙元素在元素周期表中的信息,钙的原子序数为。 (4)、行:石墨可用于制作高铁列车的受电弓滑板,其利用的石墨的性质有(填一条)。
(4)、行:石墨可用于制作高铁列车的受电弓滑板,其利用的石墨的性质有(填一条)。 -
9、小明同学在整理实验室试剂柜时发现一瓶敞口放置的氢氧化钠溶液,为了探究其是否变质及变质程度,他取少量该氢氧化钠溶液于烧杯中,逐滴加入稀氯化钙溶液,实验过程中生成沉淀的质量随加入稀氯化钙溶液的体积变化如图所示,下列说法中不正确的是
 A、a点时溶液的 B、b点时溶液中一定含有和 C、该瓶氢氧化钠溶液已经完全变质 D、纵坐标也可表示生成NaCl的质量
A、a点时溶液的 B、b点时溶液中一定含有和 C、该瓶氢氧化钠溶液已经完全变质 D、纵坐标也可表示生成NaCl的质量 -
10、下列实验方案设计不合理的是
选项
实验目的
实验方案
A
鉴别木炭粉和铁粉
分别加入稀硫酸、观察现象
B
鉴别酒精和白醋
闻气味
C
除去溶液中混有的
加入适量 , 溶液,过滤
D
检验某气体是否为一氧化碳
点燃,观察火焰颜色
A、A B、B C、C D、D -
11、某种无人机配有高性能锂电池,放电时会产生。中锂元素的化合价为+1,则锰元素的化合价为A、+2 B、+3 C、+4 D、+5
-
12、下列事实中,不能用分子在不断运动解释的是A、蔗糖溶解 B、湿衣晾干 C、柳絮飞扬 D、花香四溢
-
13、下列实验操作规范的是A、检查气密性
 B、称量试剂
B、称量试剂 C、熄灭酒精灯
C、熄灭酒精灯 D、移走蒸发皿
D、移走蒸发皿
-
14、“推动绿色发展,促进人与自然和谐共生”。下列做法与此理念不相符的是A、积极植树造林 B、适度开采地下水 C、发展清洁能源 D、加高废气烟囱
-
15、实践小组为测定某品牌纯破样品中Na2CO3)的质量分数,进行了如图实验(杂质不参与反应)。
 (1)、实验室取用纯碱粉末需用到的仪器为 , 加入稀盐酸观察到的现象是(2)、充分反应后生成气体的质量是g.(3)、计算样品中Na2CO3的质量分数。(写出计算过程,结果精确到0.1%)(4)、由于二氧化碳能溶于水,该实验测得样品中NACO,的质量分数会(选填“偏大”“偏小”或“不变”)。
(1)、实验室取用纯碱粉末需用到的仪器为 , 加入稀盐酸观察到的现象是(2)、充分反应后生成气体的质量是g.(3)、计算样品中Na2CO3的质量分数。(写出计算过程,结果精确到0.1%)(4)、由于二氧化碳能溶于水,该实验测得样品中NACO,的质量分数会(选填“偏大”“偏小”或“不变”)。 -
16、化学社团探究金属的化学性质时进行了如图实验。(1)、用砂纸打磨铁片的目的是(2)、铁与硝酸银溶液发生置换反应的化学方程式为证明铁的金属活动性比银(3)、【查阅资料】室温下,氯化银是难溶于水的白色固体:粉木状的银为黑色
【提出问题】在水中,铁能与溶于水的硝酸银反应,是否也能与难溶于水的氯化银反应?
【作出猜想】猜想!:能反应
猜想ⅡI:不能反应
【实验预测】若猪想1正确,则可观察到反应后溶液的颜色为
(4)、【进行实验】取少量氮化银于烧杯中,加入蒸馏水,再加入过量的铁粉,充分搅拌,静置后液体颜色无明显变化。甲同学据此认为猜想1I正确,乙同学认为影响液体颜色变化的因素很多,液体颜色无明显变化不能说明反应没有发生,于是他们将烧杯中的物质过滤,继续实验。请完成表格中①~③处填空。实验操作
实验现象
实验分析与结论
a.取少量滤液于试管中,滴加硝酸银溶液
①
滤液中含有氣化亚铁,滤渣的成分为②猜想ㄧ正确
b.取滤渣于另一支试管中,向共中加入足量③
产生气泡,烧杯内有黑色固体剩余
【反思提升】科学探究中,我们要敢丁质疑、收集证据、修正错误观点,提高科学思维能力。
-
17、根据下图回答问题。
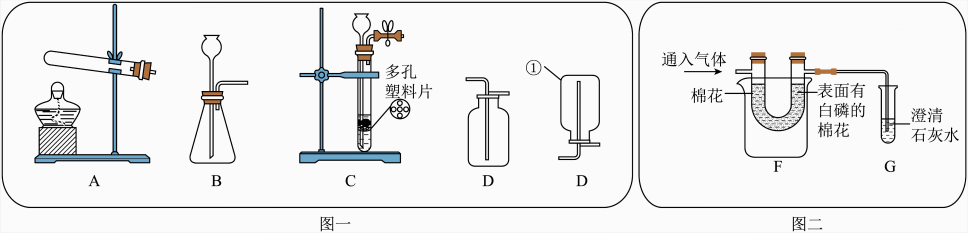 (1)、仪器①的名称是(2)、实验室用高锰酸钾制取氣气的化学方程式为收集氧气可选择的装置是(填序号).(3)、与装置B相比,实验室用装置C制取二氧化碳的优点是(4)、将制得的气体用于图二所示实验:
(1)、仪器①的名称是(2)、实验室用高锰酸钾制取氣气的化学方程式为收集氧气可选择的装置是(填序号).(3)、与装置B相比,实验室用装置C制取二氧化碳的优点是(4)、将制得的气体用于图二所示实验:通入足量的二氧化碳,然后往烧杯中倒入80C的热水:
I.再通入氧气,U形管左边的棉花不燃烧,右边的白磷先燃烧,棉花后燃烧:
I.最后通入二氧化碳,燃着的白磷和棉花都熄灭。
关于该实验的说法正确的是(填序号,双选)。
a.步骤1:可观察到G中澄清石灰水变浑浊
b.步骤Ⅱ:对比U形管两边棉花的燃烧情况,说明燃烧需要氧气
c.步骤1Ⅱ:右边的白磷比棉花先燃烧,说明白磷的着火点比棉花低
d.步骤Ⅲ:燃着的白磷和棉花都熄灭,说明二氧化碳的密度比空气大
-
18、碳酸镁是重要的化工原料。实验室以工业废渣(含MgCO3、MgO、SiO2)为原料制备MgCO3的主要实验过程如下:

已知:MgCO3能与酸反应:SiO2不溶于水且流程中不参与反应
(1)、滤渣的成分是(2)、工业废渣中的氣化镁与稀硫酸反应生成碗酸镁和水,该反应的化学方程式为(3)、操作1和操作2的名称都是不能省去操作1的理由是 -
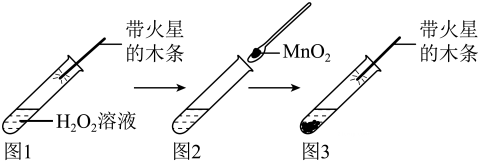
19、兴趣小组为了解调控化学反应的方法,进行了下列实验。(1)、实验一:在空气中点燃木炭,再伸入充满氣气的集气瓶中,木炭燃烧更剧烈,说明会影响化学反应速率。(2)、实验二:图1木条不复燃,图3中的现象为由此可知MnO2可加快H2O2分解的速半。若反应前后MnO2的和化学性质不变,则MnO2是H2O分解的催化剂。为寻找该反应的新催化剂,兴趣小组分别用5mL10%HO2溶液和不同催化剂进行实验,数据如表。分析表中数据,催化效果最好的物质是
试验编号
催化剂
收集气体体积
收集气体所用时间
①
2g氧化铁
7.0 mL
560 s
②
2g土豆
7.0 mL
180 s
③
2g生姜
5.1 mL
180 s
(3)、调控化学反应的方法还有很多,下列事例中调控方法相同的是____(序号)。A、食品在冰箱中保存不易变质 B、燃煤发电时,把煤块粉碎 C、汽车发动机把汽油喷成雾状进行燃烧 -
20、奔赴星辰大海,化学赋能未来。
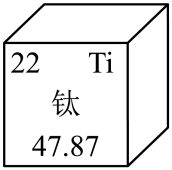 (1)、“天和”驻空:天和核心舱内“人造空气”中能供给呼吸的气体是。航天员的食物有牛肉、蔬菜、米饭等,其中富含蛋白质的是(2)、“奋斗者”探海:“奋斗者”号使用了钛合金和锂电池,钛元素在元素周期表中的信息如图,钛原子的质子数是:工业上制锂的一种方法是:2Al+3Li2O6Li+X,X 的化学式是(3)、“梦想”号入地:“梦想”号的钻探能力堪称全球顶尖。碳化硅(SiC)钻头可用于深海钻探,SiC中碳元素为-4价,则硅的化合价是价。
(1)、“天和”驻空:天和核心舱内“人造空气”中能供给呼吸的气体是。航天员的食物有牛肉、蔬菜、米饭等,其中富含蛋白质的是(2)、“奋斗者”探海:“奋斗者”号使用了钛合金和锂电池,钛元素在元素周期表中的信息如图,钛原子的质子数是:工业上制锂的一种方法是:2Al+3Li2O6Li+X,X 的化学式是(3)、“梦想”号入地:“梦想”号的钻探能力堪称全球顶尖。碳化硅(SiC)钻头可用于深海钻探,SiC中碳元素为-4价,则硅的化合价是价。