相关试卷
- 广东省清远市2016-2017学年九年级化学一模考试试卷
- 广西钦州港经济开发区2015-2016学年九年级上学期化学期末考试试卷
- 广西北海市合浦县教育局教研室2013-2014学年九年级上学期化学期末考试试卷
- 广西北海市合浦县2012-2013学年九年级上学期化学期末考试试卷
- 广东省肇庆市鼎湖中学2017-2018学年九年级上学期化学期中考试试卷
- 2016年广西钦州市中考化学试题
- 2015年广西钦州市中考化学试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西钦州地区2016-2017学年九年级化学中考模拟考试试卷
-
1、
在学习了“酸碱中和反应”后,同学们开展了实验探究。
实验一:小亮在做“稀盐酸中和氢氧化钠溶液”实验时,滴加稀盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行了探究。
【提出猜想】所得溶液可能呈酸性。
【实验验证】
(1)
实验操作
实验现象
实验结论
取少量反应后的溶液于试管中,滴加紫色石蕊溶液.
溶液变色
猜想正确
实验二:小军在实验中用数字化传感器测得溶液的pH变化曲线如图所示。

(2)写出稀盐酸与氢氧化钠溶液反应的化学方程式。
(3)根据图示判断该实验是将滴入中。
(4)曲线上点表示酸和碱恰好完全反应。
(5)C点溶液中含有的溶质是。
-
2、某化学兴趣小组同学利用图中所示装置模拟炼铁:
 (1)、为了避免玻璃管a在加热时可能发生爆炸,加热前应。(2)、反应后a管中发生反应的化学方程式为 , B装置(填“能”或“不能”)用来收集CO。(3)、若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了2.4g,则加入a管中氧化铁的质量是g。
(1)、为了避免玻璃管a在加热时可能发生爆炸,加热前应。(2)、反应后a管中发生反应的化学方程式为 , B装置(填“能”或“不能”)用来收集CO。(3)、若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了2.4g,则加入a管中氧化铁的质量是g。 -
3、如图是甲、乙、丙三种固体物质的溶解度曲线。请根据图示填空:
 (1)、时,甲、乙、丙三种物质的溶解度大小关系是。(2)、时,乙物质的饱和溶液中溶质、溶剂的质量之比为(填最简整数比)。(3)、欲配制相同质量分数的乙、丙饱和溶液,应保持温度在℃。(4)、丙的不饱和溶液变成饱和溶液的方法是(填一种即可)。(5)、将时甲、乙、丙三种物质的饱和溶液各100g,分别降温至所得溶液质量的大小关系是。
(1)、时,甲、乙、丙三种物质的溶解度大小关系是。(2)、时,乙物质的饱和溶液中溶质、溶剂的质量之比为(填最简整数比)。(3)、欲配制相同质量分数的乙、丙饱和溶液,应保持温度在℃。(4)、丙的不饱和溶液变成饱和溶液的方法是(填一种即可)。(5)、将时甲、乙、丙三种物质的饱和溶液各100g,分别降温至所得溶液质量的大小关系是。 -
4、
早在春秋战国时期。我国就开始生产和使用铁器。
[认识铁及其来源]
(1)铁元素在自然界中主要以(填“单质”或“化合物”)形式存在。(2)工业上从含有金属元素并有开采价值的矿石中提炼金属。赤铁矿是常见铁矿石,其主要成分的化学式为。[认识铁的性质]
(3)菜刀、锤子用铁制而不用铝制,是利用铁具有的性质。(4)将铁片放入稀盐酸中,写出发生反应的化学方程式;将铁片放入硫酸锌和硫酸铜混合溶液中,写出发生反应的化学方程式。[铁的锈蚀和防护]
(5)下列环境中的铁制品最容易生锈的是(填字母)。A. 未擦干的铁锅 B. 喷油漆的栏杆 C. 盛水的不锈钢水杯 -
5、用化学用语填空。(1)、钠离子。(2)、氢元素。(3)、五氧化二磷分子。(4)、3个氮原子。(5)、甲烷。
-
6、从海水中得到的粗盐中往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。粗盐提纯的部分流程如图。有关该流程说法错误的是
 A、不溶性杂质主要是泥沙 B、过滤时玻璃棒的作用是引流 C、操作①②③依次加入的试剂可以为NaOH溶液、Na2CO3溶液、BaCl2溶液 D、蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
A、不溶性杂质主要是泥沙 B、过滤时玻璃棒的作用是引流 C、操作①②③依次加入的试剂可以为NaOH溶液、Na2CO3溶液、BaCl2溶液 D、蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干 -
7、稀盐酸与氢氧化钠溶液反应时溶液pH的变化如图所示。下列说法错误的是
 A、该反应属于复分解反应 B、如向n点时的溶液中滴入酚酞溶液,溶液显无色 C、该实验是将氢氧化钠溶液滴入稀盐酸中 D、p点所示溶液中的溶质只有NaOH
A、该反应属于复分解反应 B、如向n点时的溶液中滴入酚酞溶液,溶液显无色 C、该实验是将氢氧化钠溶液滴入稀盐酸中 D、p点所示溶液中的溶质只有NaOH -
8、类推是化学学习中常用的思维方法。以下类推结果正确的是A、浓盐酸有挥发性,所以浓硫酸也有挥发性 B、碱性溶液能使紫色石蕊溶液变蓝,所以能使紫色石蕊溶液变蓝的溶液一定呈碱性 C、金属铝与盐酸反应生成AlCl3和H2。所以铁和盐酸反应生成和 D、碳酸盐与盐酸反应放出气体,则与盐酸反应放出气体的物质一定是碳酸盐
-
9、下列有关溶液的说法正确的是A、NaCl的饱和溶液一定比不饱和溶液的溶质质量分数大 B、长期放置不分层的液体一定是溶液 C、降低饱和溶液的温度,一定有晶体析出 D、配制好的6%的NaCl溶液,装入试剂瓶中时不慎洒漏一部分,浓度不变
-
10、金属R与Hg(NO3)2溶液反应的化学方程式为R+Hg(NO3)2=R(NO3)2+Hg,下列说法中不正确的是A、R可能是铝 B、该反应为置换反应 C、R的金属活动性比Hg强 D、在金属活动性顺序表中,R不一定排在氢前面
-
11、化学与人体健康密切联系,下列说法正确的是A、用霉变的花生榨食用油 B、亚硝酸钠(NaNO2)用于烹调 C、甲醛浸泡的食物可以食用 D、小苏打用作食品的膨松剂
-
12、下列有关金属材料的说法错误的是A、纯金属和合金都是金属材料 B、生铁的主要成分是碳 C、金制成金箔是利用了金具有良好的延展性 D、一般来说,合金比组成它的纯金属硬度大
-
13、端午时节。粽叶飘香。粽子是用粽叶包裹糯米等蒸煮而成的食品。因粽叶中含有对乙烯基苯酚。会散发出清香。糯米的主要成分是淀粉。淀粉属于A、糖类 B、油脂 C、蛋白质 D、维生素
-
14、下列实验现象及结论都正确的是
选项
实验
现象
结论
A
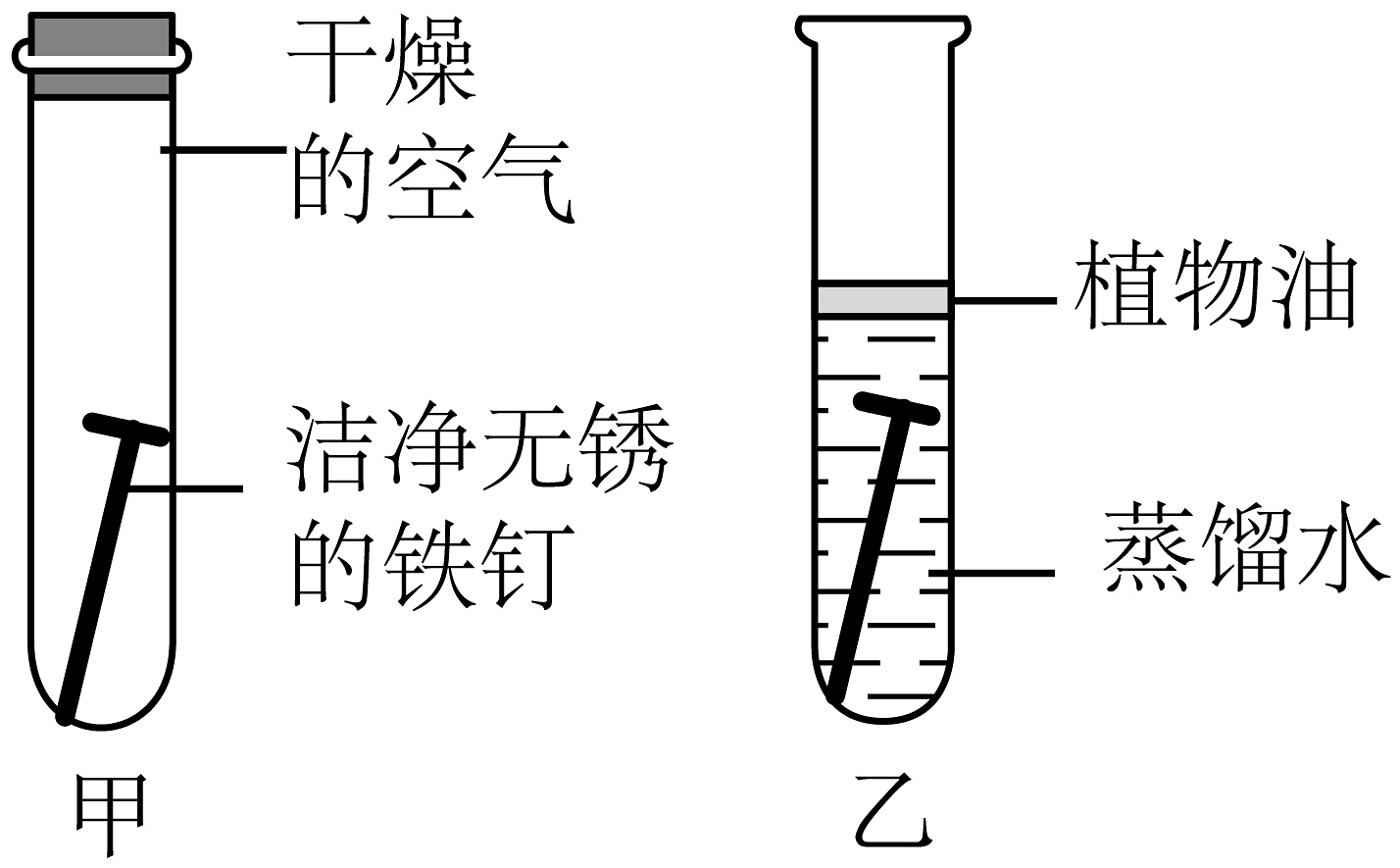
探究铁生锈的条件
乙试管中铁钉生锈
铁生锈需要与水接触
B
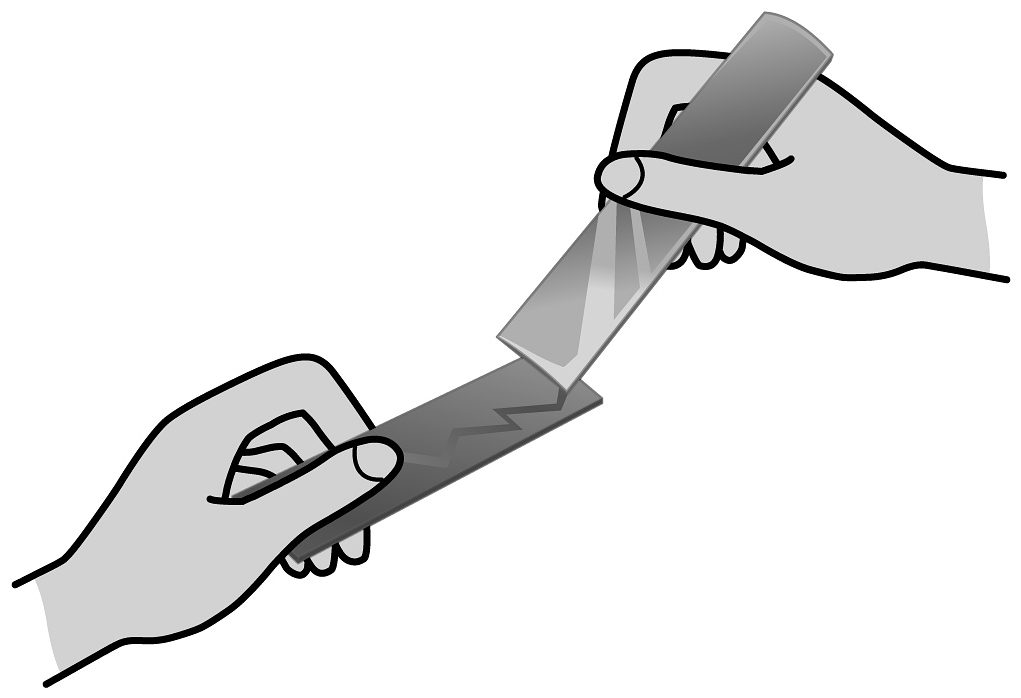
将纯铝和铝合金相互刻画
纯铝上留下划痕
铝合金的密度比纯铝大
C

探究CO2的性质
紫色石蕊溶液变红
CO2能使紫色石蕊溶液变红
D
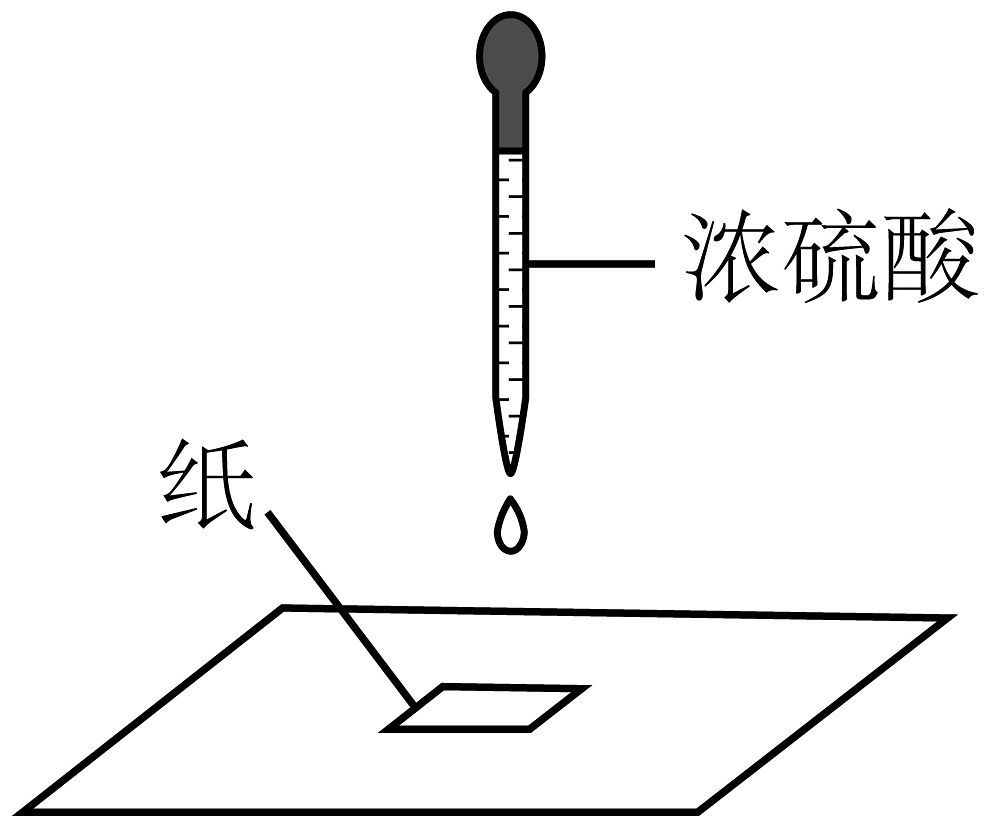
探究浓硫酸的性质
滴有浓硫酸的部位变黑
浓硫酸具有腐蚀性
A、A B、B C、C D、D -
15、下列实验方案中,不能达到目的的是
选项
混合物
方法
A
除去氯化钠溶液中混有的氯化钙
加入过量的碳酸钠溶液,过滤
B
除去MgCl2溶液中的少量盐酸
加入足量MgO固体(难溶于水)后过滤
C
鉴别NaOH溶液和Ca(OH)2溶液
取样,分别通入CO2 , 观察现象
D
鉴别稀盐酸和NaCl溶液
取样,滴加紫色石蕊溶液,观察颜色变化
A、A B、B C、C D、D -
16、如图通过加热铜粉来验证质量守恒定律,下列有关说法中,不正确的是
 A、铜粉加热后由红色变为黑色 B、气球先膨胀变大,冷却后缩小 C、不可以用玻璃棒来代替玻璃导管 D、反应前锥形瓶内铜粉氧气的总质量一定等于生成的氧化铜的质量
A、铜粉加热后由红色变为黑色 B、气球先膨胀变大,冷却后缩小 C、不可以用玻璃棒来代替玻璃导管 D、反应前锥形瓶内铜粉氧气的总质量一定等于生成的氧化铜的质量 -
17、化学项目小组用图1所示装置验证质量守恒定律。点燃红磷前电子天平示数为106.23g(见图1)。验证质量守恒定律后,待白烟完全沉降取下橡胶塞,片刻后再一起称量,电子天平示数稳定为106.28g(见图2)。
回答下列问题:
 (1)、托盘天平的精确度为g。(2)、计算参加反应红磷的质量(结果精确到0.01g)。
(1)、托盘天平的精确度为g。(2)、计算参加反应红磷的质量(结果精确到0.01g)。 -
18、
某同学对的制备和性质进行探究。
【阅读资料】①用与钙加热制得;
②钙遇水立即发生剧烈反应生成一种碱和一种气体;
③要密封保存,遇水反应也生成一种碱和一种气体。
【的制备】设计的制取装置如图所示。

(1)装置D的作用是;
(2)制备实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显色,该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是。
【的性质探究】
取少量上述装置C中的样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙。该同学继续探究。
(3)点燃产生的气体,火焰呈淡蓝色,将燃烧产物通入澄清石灰水中,无明显现象。该气体为(写化学式)。
(4)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH
猜想二:NaOH、
猜想三:NaOH、
猜想四:NaOH、、
经过讨论,大家一致认为猜想四不合理,请用化学方程式表示说其理由。
-
19、实验室里选用如图所示仪器制取气体(橡皮塞、导气管及试剂略去)。
 (1)、制取一瓶纯净的 , 若要使用双孔橡皮塞,需选用的仪器有(填字母)。(2)、用制取的化学方程式为;若用该方法制取 , 其发生装置需补充一种玻璃仪器,请在虚线框内画出该仪器。(3)、实验室里配制溶液:
(1)、制取一瓶纯净的 , 若要使用双孔橡皮塞,需选用的仪器有(填字母)。(2)、用制取的化学方程式为;若用该方法制取 , 其发生装置需补充一种玻璃仪器,请在虚线框内画出该仪器。(3)、实验室里配制溶液:①把1.0g高锰酸钾溶解于水配制成4.0g溶液。
②配制溶液的过程中,如下图,下列仪器中不需要的是(填写仪器名称)。

③配制上述实验中所用的溶液,若所配制溶液的溶质质量分数偏小,其原因可能是(填写字母序号)。
A.固体本身不纯 B.量水时仰视读数
C.向烧杯中倒水溶解时部分水洒出 D.装瓶时部分溶液洒出
-
20、空气中含有大量的氮气,如何将氮气在常温下转化为氨气成为近年研究的热点。一种将氮气转化为氨气的循环过程如图所示。回答问题:
 (1)、该过程中的LiOH属于(填“酸”“碱”或“盐”)。(2)、过程I中发生化合反应的化学方程式为。(3)、该过程中能循环使用的物质有。
(1)、该过程中的LiOH属于(填“酸”“碱”或“盐”)。(2)、过程I中发生化合反应的化学方程式为。(3)、该过程中能循环使用的物质有。