相关试卷
- 广东省清远市2016-2017学年九年级化学一模考试试卷
- 广西钦州港经济开发区2015-2016学年九年级上学期化学期末考试试卷
- 广西北海市合浦县教育局教研室2013-2014学年九年级上学期化学期末考试试卷
- 广西北海市合浦县2012-2013学年九年级上学期化学期末考试试卷
- 广东省肇庆市鼎湖中学2017-2018学年九年级上学期化学期中考试试卷
- 2016年广西钦州市中考化学试题
- 2015年广西钦州市中考化学试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西钦州地区2016-2017学年九年级化学中考模拟考试试卷
-
1、梳理知识脉络是提高学习效率的方法之一,下列归纳整理的化学知识均正确的是
A.化学与生活
B.化学与能源
①钙是人体必须的微量元素,碳酸钙可做补钙剂
②多吃蔬菜水果可提供身体发育所需蛋白质
③用小苏打、氢氧化镁都可以治疗胃酸过多
①天然气、沼气都是不可再生的化石燃料
②氢能源最突出优点是生成物水无污染
③太阳能、风能、潮汐能都属于清洁能源
C.化学与安全
D.化学与农业
①面粉厂、加油站附近应严禁接打电话
②进入久无人至的地窖前先做灯火试验
③炒菜时油锅不慎着火,立即盖上锅盖灭火
①硝酸钾属于钾肥
②铵态氮肥不能与碱性物质混合施用
③纯碱、烧碱都可以改良酸性土壤
A、A B、B C、C D、D -
2、条形码是呈现考生信息常用的一种方法,其背面黏性主要来源于胶黏剂丙烯酸(C3H4O2)。下列关于丙烯酸的说法正确的是
 A、1个丙烯酸分子中含有2个水分子 B、完全燃烧生成CO2和H2O C、属于无机物 D、碳、氢、氧元素的质量比为3:4:2
A、1个丙烯酸分子中含有2个水分子 B、完全燃烧生成CO2和H2O C、属于无机物 D、碳、氢、氧元素的质量比为3:4:2 -
3、下列说法错误的是A、点燃的火柴竖直向上,火柴梗不易继续燃烧,其原因是火柴梗接触氧气少 B、有水生成的基本反应类型有四种 C、青少年缺钙会患佝偻病,所以青少年一定要多吃含钙丰富的食物 D、向一未知固体中加入稀盐酸,有气泡产生,该固体不一定是碳酸盐
-
4、下列化学实验操作正确的是A、
 称取固体
B、
称取固体
B、 研磨固体
C、
研磨固体
C、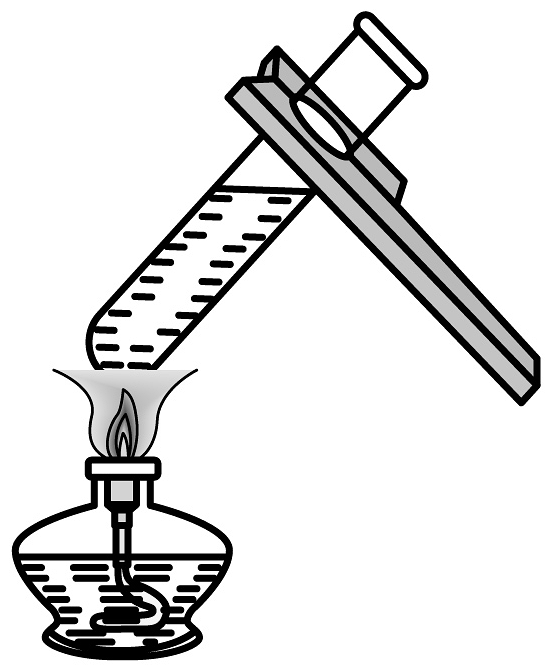 加热液体
D、
加热液体
D、 吸取液体
吸取液体
-
5、蛋类食物中含有丰富的褪黑素,有改善睡眠和抗氧化等功能。食用时还能提供较多的营养物质是A、水 B、糖类 C、蛋白质 D、无机盐
-
6、为测定某黄铜(铜、锌合金)中铜的质量分数,某同学取 20g 黄铜样品放入盛有 200g 稀盐酸的烧杯中,恰好完全反应,测得烧杯中剩余物质的总质量为219.8g,试计算:(1)、生成氢气的质量g;(2)、该黄铜样品中铜的质量分数。(写出计算过程)
-
7、小明同学在学完合金的知识后,知道了生活中常见的不锈钢中除了含有铁,还含有 金属铬(Cr)。铬与常见的铁和铜相比,金属活动性如何呢?他决定对 Fe、Cu、Cr 三种金属的活动性进行探究。
【知识回顾】铁是一种比较活泼的金属,请写出铁与稀硫酸反应的化学方程式。
【查阅资料】铬是一种银白色金属,能与稀硫酸反应生成能溶于水的 CrSO4并放出氢气。
【猜想与假设】根据教材中常见金属的活动性顺序和查阅的资料,他对以上三种金属的活动性作出了合理的猜想:
猜想①Cr > Fe > Cu;
猜想②。
【实验探究】把用砂纸打磨过的铁片和铬片分别放入等量等浓度的稀硫酸中,观察到的现象,证明了猜想①成立。
【实验反思】经过分析,他发现用铬片、FeSO4溶液和 , 通过实验探究也能判断Fe、Cu、Cr 三种金属的活动性顺序。
【拓展迁移】在硫酸铜和硫酸亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是 , 滤液中可能含 有的物质是。
-
8、某化学兴趣小组的同学利用下列实验装置,开展O2和CO2的实验室制取和有关性质的研究,请结合下列实验装置,回答有关问题。

(1)写出图中标有序号的仪器名称:①。
(2)实验室可用B和D装置制取并收集二氧化碳,写出反应的化学方程式:。
若实验室用高锰酸钾制取较纯净的氧气,可选用的发生装置和收集装置为 , 写出反应的化学方程式:。若用G装置盛满水收集氧气,则气体应从(填“a”或“b”)端通入。
(3)细铁丝在H装置中燃烧,可观察到的现象是。
(4)C装置与B装置相比,其优点是。
-
9、甲缩醛如果混入汽油中,易造成汽车线路漏油,还会挥发有害气体,污染环境,影响人体健康。甲缩醛的化学式为。请计算:(1)、甲缩醛是由种元素组成;(2)、甲缩醛中碳、氢、氧三种元素的质量比是;(3)、152g甲缩醛中氧元素的质量是。
-
10、在宏观、微观和符号之间建立联系是化学学科的重要思维方式.根据下列粒子结构示意图,回答问题:
 (1)、上述示意图中,共包含种元素,它们之间的本质区别是不同,属于非金属元素的有种。(2)、A、B、C、E中属于阴离子的是(填离子符号)。(3)、若D表示某元素的原子,则m= , 该粒子在化学变化中容易(选填“得到”或“失去”)电子。(4)、画出核外电子排布与E相同的原子结构示意图。(5)、B所属元素与D所属元素组成的化合物是由离子构成的,这个化合物的符号为。
(1)、上述示意图中,共包含种元素,它们之间的本质区别是不同,属于非金属元素的有种。(2)、A、B、C、E中属于阴离子的是(填离子符号)。(3)、若D表示某元素的原子,则m= , 该粒子在化学变化中容易(选填“得到”或“失去”)电子。(4)、画出核外电子排布与E相同的原子结构示意图。(5)、B所属元素与D所属元素组成的化合物是由离子构成的,这个化合物的符号为。 -
11、用恰当的化学用语填空.(1)、2个氮原子;(2)、3个亚铁离子;(3)、2个硫酸根离子;(4)、氩气。
-
12、一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法不正确的是
物质
X
Y
Z
W
反应前质量/g
10
3
90
0
反应后质量/g
3.2
3
待测
3.2
A、W可能是单质 B、Y可能是催化剂 C、该反应生成物是两种 D、反应后Z物质的质量为86.4g -
13、苏丹红一号是一种增色添加剂,可能使人体致癌,其化学式为 , 下列关于它的说法错误的是A、它的分子中,碳、氢、氮、氧原子个数比为16:12:2:1 B、它所含元素中,质量分数最高的是碳元素 C、它所含碳、氢、氮、氧元素的质量比为48:3:7:4 D、它是一种氧化物
-
14、下列关于碳和碳的氧化物的说法不正确的是A、金刚石、石墨物理性质不同是因为碳原子的排列方式不同 B、CO极易与血液中的血红蛋白结合 C、CO2含量过多会导致温室效应 D、金刚石、石墨和都是碳原子构成的单质
-
15、根据如图所示的实验,下列说法正确的( )A、②③对比说明物质燃烧需要与空气接触
 B、检验甲试管内的气体可以用燃着的木条
B、检验甲试管内的气体可以用燃着的木条 C、该实验说明二氧化碳能使紫色石蕊溶液变红
C、该实验说明二氧化碳能使紫色石蕊溶液变红 D、该实验的现象是产生淡蓝色火焰,放出热量,生成有刺激性气味的气体
D、该实验的现象是产生淡蓝色火焰,放出热量,生成有刺激性气味的气体
-
16、下图所示的实验操作中,正确的是


A.倾倒液体
B.检验氢气纯度


C.比较金属制品导热性
D.溶解
A、A B、B C、C D、D -
17、
某化学兴趣小组阅读课外资料得知:过氧化氢制氧气除了可用二氧化锰作为催化剂,还可以用氧化铜、马铃薯、铁锈、红砖粉末等物质作为催化剂,于是他们想检验生活中马铃薯是否能作为过氧化氢分解的催化剂。
【提出问题】马铃薯是否能作为过氧化氢分解的催化剂?
【查阅资料】马铃薯中含有过氧化氢酶,过氧化氢酶对过氧化氢的分解起催化作用。
【设计实验】
(1)化学兴趣小组的同学设计了一系列实验:
实验
实验步骤
实验现象
Ⅰ
取5%的过氧化氢溶液5mL,用带火星的木条伸入试管口
木条不复燃
Ⅱ
取5%的过氧化氢溶液5mL,加入0.5g马铃薯切成豆粒大
木条复燃
Ⅲ
待实验Ⅱ中没有气泡放出后,继续加入5%的过氧化氢溶液
木条________
(2)写出实验Ⅱ反应的符号表达式________;
(3)设计实验Ⅰ的目的是与实验Ⅱ________;
【得出结论】马铃薯能作为过氯化氢分解的催化剂。
【评价改进】
(4)大家认为此实验结论不严谨。若要确定该实验结论是否正确,还需要再增加一个实验,探究马铃薯的________在化学反应前后是否发生变化。
【实验拓展】某小组同学设计了如图所示装置,定量测定对比马铃薯与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据见表:
实验编号
3%过氧化氢溶液的体积
其他物质质量
待测数据
Ⅰ
20mL
马铃薯0.5g
Ⅱ
20mL
二氧化锰0.5g

(5)上述实验中“待测数据”是指________。
(6)若则可得出的结论是________。
【实验反思】
(7)影响化学反应速率的因素除了催化剂的种类外,还可能与下列哪些因素有关?______。
A. 催化剂的颗粒大小 B. 温度 C. 反应物的浓度 -
18、下列化学现象的描述,正确的是A、红磷在空气中燃烧,产生大量白色烟雾 B、硫在氧气中燃烧,发出微弱的淡蓝色火焰 C、木炭在氧气中燃烧比在空气中燃烧更旺,发出白光,并放出热量 D、铁丝在氧气中燃烧,火星四射,生成黑色的四氧化三铁
-
19、日常生活中常用的清洗剂有84消毒液和洁厕灵。84消毒液的有效成分是次氯酸钠(化学式为NaClO)。某品牌洁厕灵的标签如下。
名称:洁厕灵
功能:有效清除污垢、除异味
有效成分:HCl
注意事项:勿用于大理石的清洁
(1)、该洁厕灵标签上写有“勿用于大理石的清洁”,其原因是。(2)、“洁厕灵”和“84消毒液”不能混用,否则会产生有毒的氯气,反应的化学方程式 , 若不慎将10克7.3%的洁厕灵和足量84消毒液混合,能产生多少克有毒的氯气? -
20、
铜制品久置在户外容易生锈,失去金属光泽,需要定期除锈。某化学兴趣小组对对铜的锈蚀条件、铜锈的成分及除锈的方法进行如下项目式探究。
【项目一】探究铜的锈蚀条件
【实验1】探究铜生锈的条件,将大小相同的4小块铜片按下图装置所示放置1周,结果如下:
编号
甲
乙
丙
丁
实验




现象
铜片表面有绿色物质
无明显现象
无明显现象
无明显现象
(1)实验中使用的蒸馏水需“煮沸并迅速冷却”,其目的是。
(2)丙中除去空气中二氧化碳常用的方法,用化学方程式表示:。
(3)对比实验甲、丙得到的结论是;若要说明铜锈蚀还与氧气有关,则丁中方框里应该填写的内容是。
(4)结合上述实验,你对保存铜制品的建议是。
【项目二】探究铜锈的化学式
查阅资料:
①铜生锈是因为生成了碱式碳酸铜[]。
②碱式碳酸铜受热分解生成三种氧化物。
③NaOH溶液吸收 , 浓只吸收水。

【实验2】将4.44g碱式碳酸铜加热至完全分解,使产生的气体全部缓缓通过上图装置,测定生成气体的质量。(假设每步吸收均完全)
【数据】①浓硫酸增重0.36g;②NaOH溶液增重0.88g。
【结论】
(5)碱式碳酸铜的化学式为。
【项目三】探究铜制品表面除锈的方法
【实验3】物理除锈:小组同学利用砂纸打磨除去铜制品表面的铜锈,观察到铜制品是红色。
化学除锈:小组同学将生锈的铜制品浸泡在稀盐酸中,观察到有气泡冒出,溶液变蓝色。
(6)写出化学除锈的化学方程式。