相关试卷
-
1、按物质组成分类,KAl(SO4)2·12H2O属于A、酸 B、碱 C、盐 D、混合物
-
2、甲磺司特(M)是一种在临床上治疗支气管哮喘、特应性皮炎和过敏性鼻炎等疾病的药物。M的一种合成路线如下(部分试剂和条件省略)。

回答下列问题:
(1)、A的化学名称为。(2)、的反应类型为。(3)、D的结构简式为。(4)、由F生成G的化学方程式为。(5)、G和H相比,H的熔、沸点更高,原因为。(6)、K与E反应生成L,新构筑官能团的名称为。(7)、同时满足下列条件的I的同分异构体共有种。(a)核磁共振氢谱显示为4组峰,且峰面积比为;
(b)红外光谱中存在和硝基苯基(
 )吸收峰。
)吸收峰。其中,可以通过水解反应得到化合物H的同分异构体的结构简式为。
-
3、是火箭固体燃料重要的氧载体,与某些易燃物作用可全部生成气态产物,如:。下列有关化学用语或表述正确的是A、的形成过程可表示为
 B、中的阴、阳离子有相同的VSEPR模型和空间结构
C、在、石墨、金刚石中,碳原子有和三种杂化方式
D、和都能作制冷剂是因为它们有相同类型的分子间作用力
B、中的阴、阳离子有相同的VSEPR模型和空间结构
C、在、石墨、金刚石中,碳原子有和三种杂化方式
D、和都能作制冷剂是因为它们有相同类型的分子间作用力
-
4、侯氏制碱法工艺流程中的主反应为 , 其中W、X、Y、Z、Q、R分别代表相关化学元素。下列说法正确的是A、原子半径: B、第一电离能: C、单质沸点: D、电负性:
-
5、超氧化钾可用作潜水或宇航装置的吸收剂和供氧剂,反应为 , 为阿伏加德罗常数的值。下列说法正确的是A、中键的数目为 B、晶体中离子的数目为 C、溶液中的数目为 D、该反应中每转移电子生成的数目为
-
6、耦合反应制备丙烯酸甲酯的机理如图所示。下列叙述错误的是
 A、由步骤①②知:加成反应也可生成酯类物质 B、反应过程中存在C-H键的断裂 C、该反应的原子利用率为100% D、若将步骤②中换为 , 则产品将变为丙烯酸乙酯
A、由步骤①②知:加成反应也可生成酯类物质 B、反应过程中存在C-H键的断裂 C、该反应的原子利用率为100% D、若将步骤②中换为 , 则产品将变为丙烯酸乙酯 -
7、从古至今科学家对人类文明和社会可持续发展作出了重要贡献。下列选项正确的是A、拉瓦锡编制了元素周期表 B、门捷列夫提出了近代原子学说 C、道尔顿确定了空气的组成 D、侯德榜发明了联合制碱法
-
8、下图横坐标、纵坐标分别表示一定条件下氧化剂的氧化性、还原剂的还原性由弱到强的变化,1、2、3点表示了横纵坐标对应微粒在水溶液中反应的产物。下列说法正确的是
 A、反应1中的S失电子表现氧化性 B、反应2的离子方程式为: C、反应3的产物a是 D、从图可推得能氧化、
A、反应1中的S失电子表现氧化性 B、反应2的离子方程式为: C、反应3的产物a是 D、从图可推得能氧化、 -
9、下列有关硅及其化合物的说法中不正确的是A、在粗硅的提取中发生反应:2C+SiO22CO↑+Si,硅元素被还原 B、Si和SiO2均能与NaOH溶液反应生成硅酸钠 C、用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2 D、由Na2CO3+SiO2CO2↑+Na2SiO3可知硅酸的酸性强于碳酸
-
10、用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
I.向铝灰中加入过量稀H2SO4 , 过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)、溶解的离子方程式是。(2)、写出氧化的离子方程式(还原产物为)。(3)、已知:生成氢氧化物沉淀的pH(注:金属离子的起始浓度为)开始沉淀时
3.4
6.3
1.5
完全沉淀时
4.7
8.3
2.8
根据表中数据解释步骤Ⅱ的目的。
(4)、已知:一定条件下,可与反应生成。①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是 , 写出反应的离子方程式。
②Ⅳ中加入MnSO4的目的是。
-
11、某同学进行如下实验:
实验步骤
实验现象
I
将NH4Cl固体加入试管中,并将湿润的pH试纸置于试管口,试管口略向下倾斜,对试管底部进行加热
试纸颜色变化:黄色→蓝色(pH≈10)→黄色→红色(pH≈2);试管中部有白色固体附着
II
将饱和NH4Cl溶液滴在pH试纸上
试纸颜色变化:黄色→橙黄色(pH≈5)
下列说法不正确的是
A、根据I中试纸变蓝,说明NH4Cl发生了分解反应 B、根据I中试纸颜色变化,说明氨气比氯化氢气体扩散速率快 C、I中试纸变成红色,是由于NH4Cl水解造成的 D、根据试管中部有白色固体附着,说明不宜用加热NH4Cl的方法制备NH3 -
12、聚甲基丙烯酸羟乙酯(HEMA,结构简式为
 )可用于制作超薄镜片,其合成路线如下(加料顺序、反应条件略)
)可用于制作超薄镜片,其合成路线如下(加料顺序、反应条件略)
已知:反应⑤⑦均为加聚反应。
(1)、A的名称为 ,与A互为同系物的物质的结构简式:(任写一种) 。(2)、下列反应的反应类型:① ,④ 。(3)、C在Cu催化、加热条件被O2氧化为D,写出该反应的化学方程式: 。(4)、E的分子式为 ,F中官能团的名称为 。(5)、反应⑥的化学方程式为 。(6)、佩戴隐形眼镜最好常滴“人工眼泪”以滋润眼球,有一种“人工眼泪”的成分是聚乙烯醇( )。
)。(i)根据用途推测聚乙烯醇可能具有的物理性质: (写出一条即可)。
(ii)已知乙烯醇 (CH2=CHOH)不稳定,以乙炔(HC≡CH)为原料(其他无机原料任选),利用反应②的原理合成聚乙烯醇。基于你设计的合成路线,最后一步反应中,有机反应物的结构简式为 。
-
13、铁黄 (FeOOH) 难溶于水,可作颜料,也是制备饮水处理剂高铁酸钾的原料。 以烧渣(主要成分为Fe3O4、CuO 、SiO2等)为原料出产铁黄的流程如图。
 (1)、FeOOH 中 Fe的化合价为 , “酸浸”时,使用的酸为 。(2)、“滤渣1”的成分为 (填化学式)。(3)、“还原””涉及的离子方程式有、 。(4)、FeSO4·7H2O 的溶解度曲线如图,从滤液2中获得晶体的 另一种方法是 、冷却结晶。
(1)、FeOOH 中 Fe的化合价为 , “酸浸”时,使用的酸为 。(2)、“滤渣1”的成分为 (填化学式)。(3)、“还原””涉及的离子方程式有、 。(4)、FeSO4·7H2O 的溶解度曲线如图,从滤液2中获得晶体的 另一种方法是 、冷却结晶。 (5)、“氧化”中Fe2+参与反应的离子方程式为。(6)、以铁黄(FeOOH)等为原料制备高铁酸钾(K2FeO4)的工艺主要有两步:
(5)、“氧化”中Fe2+参与反应的离子方程式为。(6)、以铁黄(FeOOH)等为原料制备高铁酸钾(K2FeO4)的工艺主要有两步:①利用铁黄、NaClO和浓NaOH溶液反应制备Na2FeO4 , 该反应的氧化剂和还原剂的物质的量之比为 。
②向Na2FeO4溶液中加入浓KOH制备K2FeO4 , 该反应涉及原理是相同温度下溶解度:K2FeO4( 填“>”“<”“=”)Na2FeO4。
-
14、
研究氮及其化合物的性质对化工生产和环境保护有重要意义。
Ⅰ.某小组探究浓度对硝酸氧化能力的影响。
资料显示:浓硝酸能将NO氧化成NO2 , 而稀硝酸不能氧化NO;氢氧化钠溶液能吸 收NO2 , 但不能吸收 NO。该小组按如图装置进行验证实验(夹持仪器已略去)。
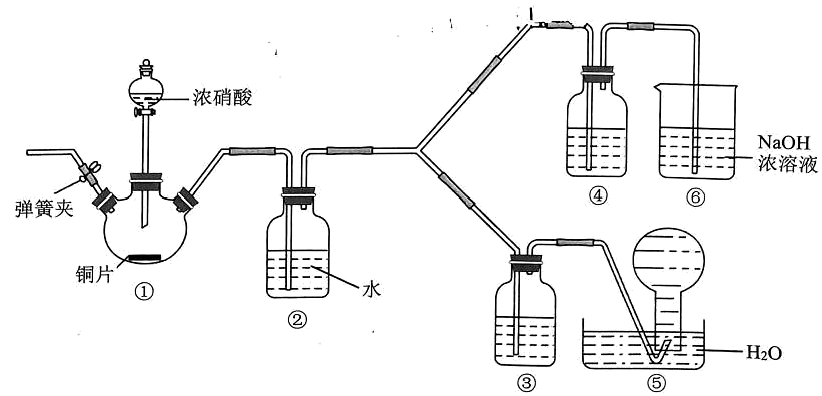 (1)装置②中反应的化学方程式为 ________。(2)装置③中盛放的试剂为________。(3)能证明不同浓度硝酸氧化能力的相对强弱的实验现象为________。
(1)装置②中反应的化学方程式为 ________。(2)装置③中盛放的试剂为________。(3)能证明不同浓度硝酸氧化能力的相对强弱的实验现象为________。Ⅱ.车尾气中的NOx是一种常见的大气污染物。在2L密闭容器中,800℃时发生反应:2NO(g)+O2 (g)=2NO2(g), 体系中n(NO) 随时间的变化如表:
时间/s
0
1
2
3
4
5
n(NO)/mol
0.020
0.010
0.008
0.007
0.007
0.007
(4)下图表示NO2的浓度变化的曲线是________。 (5)0-2s内 ,v(O2)= ________。(6)能说明该反应已达到平衡状态的是___________。
(5)0-2s内 ,v(O2)= ________。(6)能说明该反应已达到平衡状态的是___________。A. 容器内气体的颜色不再变化 B. 容器内气体的总质量保持不变 C. 正反应和逆反应的速率相等 D. NO、O2和NO2的物质的量之比为2:1:2 Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应N2H4+O2=N2+2H2O 为原理设计成利用率高的燃料电池,装置如图。
 (7)N极为电池的________ (填“正”或“负”)极, M 处电极反应式为________。
(7)N极为电池的________ (填“正”或“负”)极, M 处电极反应式为________。 -
15、在实验室里制取的乙烯中常混有少量的SO2 , 某化学兴趣小组设计了如图装置验证该混合气体中含有SO2和 C2H4。
 (1)、装置Ⅱ中反应的化学方程式为。(2)、能说明SO2、C2H4气体存在的现象分别是。(3)、下列操作中,可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中混有的乙烯的是。
(1)、装置Ⅱ中反应的化学方程式为。(2)、能说明SO2、C2H4气体存在的现象分别是。(3)、下列操作中,可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中混有的乙烯的是。A.将气体通入盛有水的洗气瓶中 B.将气体通入盛有足量溴水的洗气瓶中
C.将气体通入盛有溴的四氯化碳溶液的洗气瓶中 D.将气体通入盛有酸性高锰酸钾溶液的洗气瓶中
E.将气体通入盛有硫酸的洗气瓶中
(4)、该小组同学还利用下图装置测定空气中SO2的含量。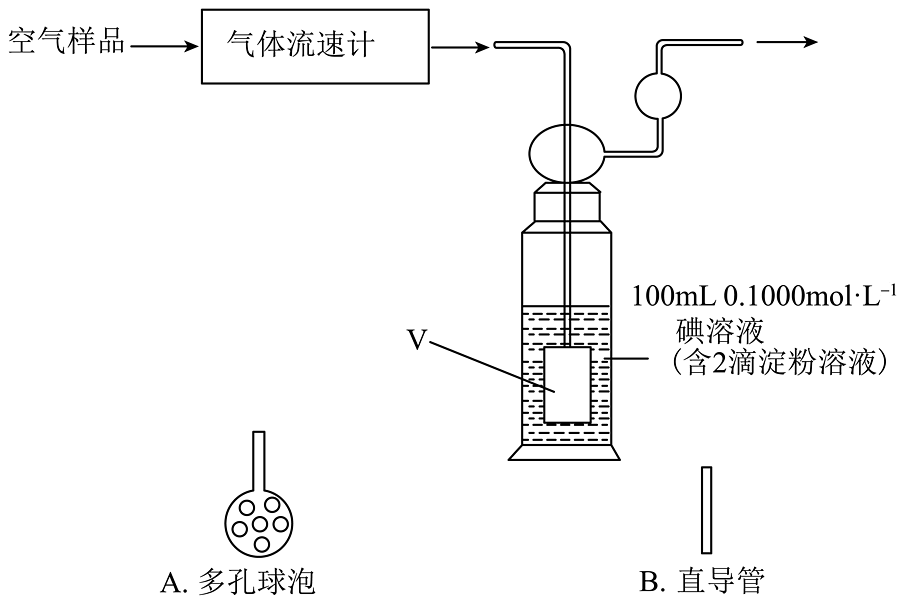
①为确保实验准确,图中V处应选择( 填“A”或“B”)连接到导管末端,否则会导致测量结果(填“偏大”或“偏小”)。
②该装置中反应的离子方程式为。
③若空气流速为a m3·min-1 , 当观察到装置内 时,结束计时,测定耗时t min。假定空气中的SO2可被溶液充分吸收,该空气样品中SO2的含量为 mg ·m-3。
-
16、基于Na2S2O3溶液与H2SO4溶液反应会出现浑浊,探究化学反应速率的影响因素,实验过程中的数据记录如下。下列说法不正确的是
实验编号
水浴温度/℃
Na2S2O3溶 液
H2SO4溶液
H2O
V/mL
c/(mol/L)
V/mL
c/(mol/L)
V/mL
1
40
2
0.1
2
0.1
0
2
20
2
0.1
2
0.1
0
3
20
1
0.1
2
0.1
a
4
40
1.5
0.1
2
0.1
1
A、通过比较出现浑浊所需时间的长短判断化学反应速率的快慢 B、该实验探究了温度、Na2S2O3溶液的浓度对化学反应速率的影响 C、实验1需先将Na2S2O3溶液和H2SO4溶液混合,再水浴加热至40℃ D、若实验2和3是探究浓度对化学反应速率的影响,则a=1 -
17、水煤气变换反应是放热反应,在双功能催化剂(能吸附不同粒子)催化下的反应过程示意 图如下下列说法正确的是
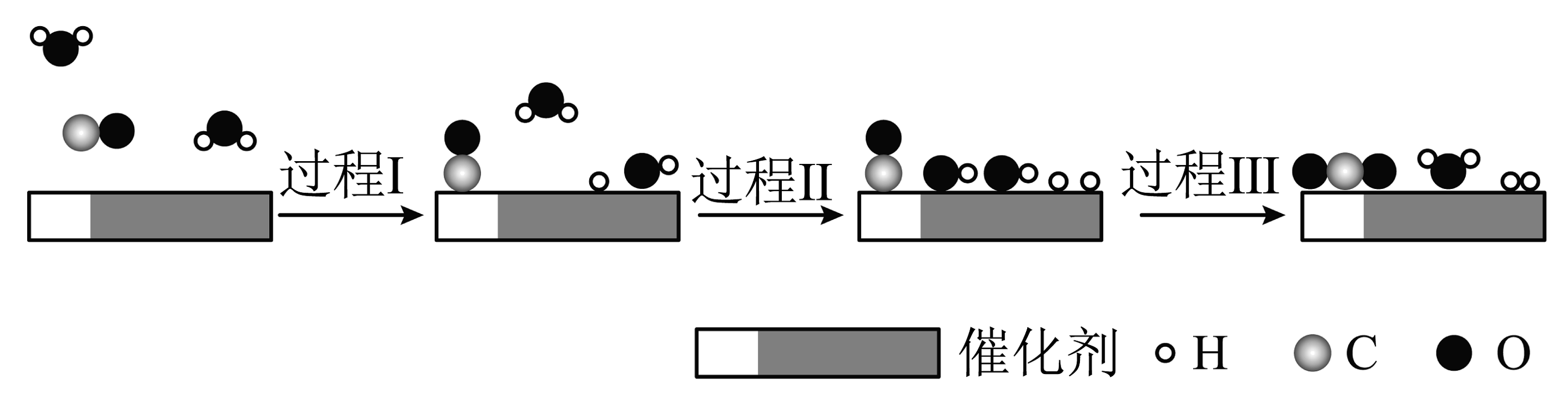 A、过 程I 中有非极性共价键断裂 B、过程Ⅱ和过程Ⅲ均为放热过程 C、该反应的化学方程式为CO+ H2O=CO2+H2 D、该反应中反应物的总能量小于生成物总能量
A、过 程I 中有非极性共价键断裂 B、过程Ⅱ和过程Ⅲ均为放热过程 C、该反应的化学方程式为CO+ H2O=CO2+H2 D、该反应中反应物的总能量小于生成物总能量 -
18、根据下列实验操作和现象所得到的结论正确的是
选项
实验操作和现象
实验结论
A
取少量待测液于试管中,先加入过量稀硝酸,再加入 氯化钡溶液,有白色沉淀生成
待测液中含有或Ag+
B
向某溶液中加入NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝
溶液中不含
C
在淀粉溶液中加入稀硫酸,加热。待溶液冷却后再加 入少量新制的Cu(OH)2 , 加热,无砖红色沉淀产生
淀粉未发生水解
D
向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色
黄色溶液中可能含有Br2
A、A B、B C、C D、D -
19、设 NA为阿伏加德罗常数的值。下列说法正确的是A、标况下,44.8L甲烷中含有的共用电子对数为8NA B、2L 0.5mol/L乙醇溶液中含有的氧原子数为NA C、5.6g铁粉在0.1molCl2中燃烧,转移电子数为0.3NA D、1mol所含的质子数为10NA
-
20、下列解释事实的化学用语不正确的是A、NaCl 溶液具有导电性:NaCl=Na++Cl- B、碳酸钙做抗酸药:+2H+=CO2↑+H2O C、NaOH 固体和铝粉混合疏通厨卫管道:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑ D、铝粉和氧化铁组成的铝热剂用于焊接钢轨