相关试卷
-
1、多姿多彩的艺术品是人类文明的见证,有些艺术瑰宝已有数百年甚至上千年的历史。下列颜料的颜色变化不涉及氧化还原反应的是A、朱砂: B、镉黄: C、红铅: D、铜绿:
-
2、南粤之地人杰地灵,文化灿烂。下列广东博物院馆藏文物中,一种文物的主要材料不同于其他三种文物的是A、南朝青铜盘 B、饕餮纹铜觚 C、南宋鎏金腰带 D、通雕蟹篓(木雕)
-
3、化学小组实验探究SO2与AgNO3溶液的反应。
(1)实验一:用如下装置(夹持、加热仪器略)制备SO2 , 将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。

①浓H2SO4与Cu反应的化学方程式是。
②试剂a是。
(2)对体系中有关物质性质分析得出:沉淀B可能为 、Ag2SO4或两者混合物。(资料:Ag2SO4微溶于水;Ag2SO3难溶于水)
实验二:验证B的成分

①写出Ag2SO3溶于氨水的离子方程式:。
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO3 , 进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是。
(3)根据沉淀F的存在,推测的产生有两个途径:
途径1:实验一中,SO2在AgNO3溶液中被氧化生成Ag2SO4 , 随沉淀B进入D。
途径2:实验二中,被氧化为进入D。
实验三:探究的产生途径
①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有:取上层清液继续滴加BaCl2溶液,未出现白色沉淀,可判断B中不含Ag2SO4。做出判断的理由:。
②实验三的结论:。
(4)实验一中SO2与AgNO3溶液反应的离子方程式是。
(5)根据物质性质分析,SO2与AgNO3溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时间,有Ag和生成。
(6)根据上述实验所得结论:。
-
4、淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征。现将淀粉和稀溶液混合,装在半透膜袋中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是A、加入溶液产生白色沉淀 B、加入碘水不变蓝 C、加入溶液没有白色沉淀产生 D、加入碘水变蓝
-
5、活性氧化锌(ZnO)常用于医药、涂料、陶瓷等。某科研小组以锌废料(主要成分是ZnSO4和ZnO,含少量的Fe、Cu、Pb、As等元素以及油污)为原料制备活性氧化锌及回收其他金属元素,流程如图。

已知几种金属离子生成氢氧化物的如下表:
金属离子
开始沉淀的
完全沉淀的
1.5
3.7
7.9
10.0
6.3
9.7
7.4
9.4
回答下列问题:
(1)、的原子结构示意图为 。中铁的化合价为。 (2)、“浸取”中,适当加热能提高浸取速率,但是温度过高,浸取速率反而降低,其主要原因是。(3)、a的范围为。“除铁”的离子方程式为。(4)、金属M的化学式为。(5)、①“活性炭”表现的性质是(填字母)。
。中铁的化合价为。 (2)、“浸取”中,适当加热能提高浸取速率,但是温度过高,浸取速率反而降低,其主要原因是。(3)、a的范围为。“除铁”的离子方程式为。(4)、金属M的化学式为。(5)、①“活性炭”表现的性质是(填字母)。A.氧化性 B.还原性 C.吸附性
②“沉锌”的滤液采用、 , 过滤、洗涤、干燥等一系列操作,得到铵态氮肥。
(6)、“高温焙烧”过程中发生反应的化学方程式为。 -
6、亚硝酰溴常用于有机合成等。工业上,常用与反应制取 , 其制备原理为。(1)、实验室常将液溴保存在水中,其原因是。实验室常用和浓硫酸混合共热制备 , 写出该反应的化学方程式:。(2)、在恒容恒温条件下,充入和 , 发生上述反应。下列情况表明反应达到化学平衡状态的是_______(填字母)。A、混合气体密度不随时间变化 B、混合气体压强不随时间变化 C、混合气体平均摩尔质量不随时间变化 D、生成速率等于消耗速率(3)、某条件下,该反应速率 , 其中为速率常数,只与温度、催化剂有关,为反应级数,可以取负数、正数;也可以取分数和整数。为了测定反应级数,实验结果如下:
实验
反应速率
Ⅰ
0.1
0.1
0.1
Ⅱ
0.2
0.1
0.1
Ⅲ
0.2
0.2
0.1
Ⅳ
0.4
0.2
0.2
①反应级数为。
②其他条件相同,升高温度,(填“增大”“减小”或“不变”)。
(4)、在体积相同的甲、乙容器中均充入和 , 在“恒温恒容”、“绝热恒容”条件下发生上述反应,测得压强与时间关系如图所示。提示:①绝热恒容指物质与能量与外界不交换,即对于放热反应,容器温度会升高;②对于恒温恒容条件下,气体总压强与气体总物质的量成正比例;③在体积相同的条件下,一定物质的量的气体,温度越高,压强越大。
①属于绝热恒容容器的是(填“甲”或“乙”),中反应物总能量(填“高于”或“低于”)产物总能量。气体总物质的量:(填“>”“<”或“=”)。
②点NO的转化率为。
-
7、为阿伏加德罗常数的值。下列叙述正确的是A、(重氨)含中子数为 B、乙烯和乙醇蒸气的混合物完全燃烧消耗分子数为 C、在中生成时转移电子数为 D、和足量乙醇反应生成酯基的数目为
-
8、近日,一款激素类药物“醋酸氢化可的松片”上热搜。它的键线式如图所示。已知:与四个互不相同的原子或基团相连接的碳原子叫手性碳原子。下列叙述错误的是
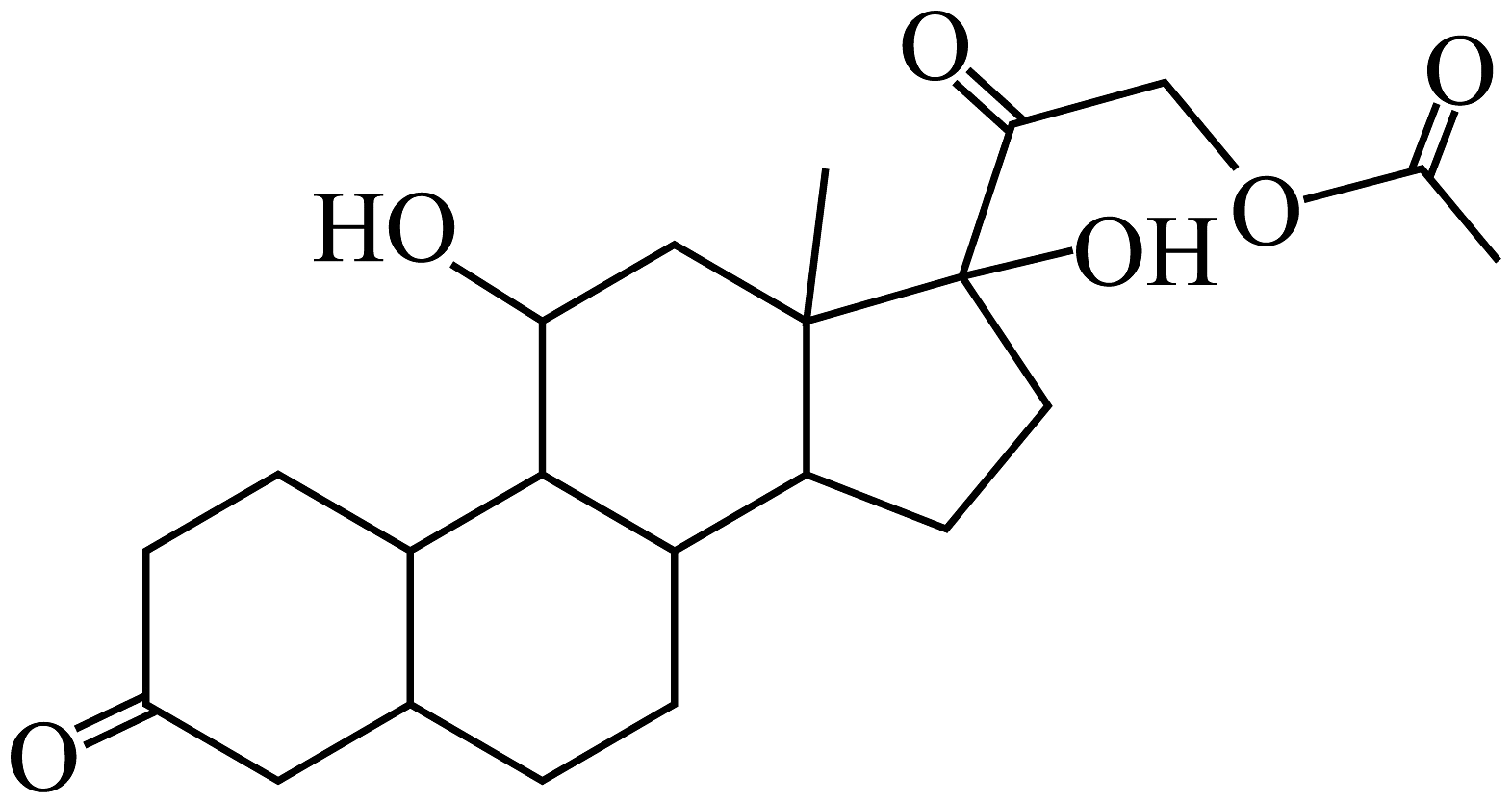 A、该物质中含有3个甲基 B、该物质分子含有手性碳原子 C、该物质能发生氧化、加成、取代反应 D、该物质能与溶液反应
A、该物质中含有3个甲基 B、该物质分子含有手性碳原子 C、该物质能发生氧化、加成、取代反应 D、该物质能与溶液反应 -
9、硅被誉为信息革命的“催化剂”。高纯硅的制备简易流程如图。下列叙述正确的是
 A、反应①的生成物有CO2、SiC B、反应②发生置换反应生成SiHCl3和H2 C、已知SiHCl3中H显﹣1价,则反应③中氧化剂是SiHCl3 , 还原剂是H2 D、制得的高纯硅可用于制造光导纤维
A、反应①的生成物有CO2、SiC B、反应②发生置换反应生成SiHCl3和H2 C、已知SiHCl3中H显﹣1价,则反应③中氧化剂是SiHCl3 , 还原剂是H2 D、制得的高纯硅可用于制造光导纤维 -
10、18世纪70年代瑞典化学家舍勒将软锰矿(主要成分为MnO2)和浓盐酸混合加热得到一种黄绿色气体——氯气。受此启发,某小组设计如下实验,能达到实验目的的是
 A、图A是制备氯气 B、图B是纯化氯气 C、图C是铁丝在氯气中燃烧 D、图D是证明氯气有漂白性
A、图A是制备氯气 B、图B是纯化氯气 C、图C是铁丝在氯气中燃烧 D、图D是证明氯气有漂白性 -
11、
学习小组开展了“设计和制作简易供氧器”的实践活动。
活动一 如图所示,该制氧机通过A、B两种物质产生氧气,其中A是过碳酸钠白色固体,B是二氧化锰黑色粉末。过碳酸钠加水溶解会分解生成和。

用该制氧机制氧时,在反应仓中加入适量水,再先后加入过碳酸钠和二氧化锰,反应仓内的现象为黑色粉末翻腾,溶液变得浑浊,仓壁变得温热,过滤仓底部导气管口有气泡冒出。
(1)反应仓中生成氧气,过滤仓中的水除了有过滤杂质提纯氧气的作用外,还可以起到的作用是(填字母)。
A.可以通过气泡观察氧气生成的速率 B.降低氧气温度 C.加快氧气的生成
(2)验证过滤仓导出的气体是氧气的方法是:将带放在 , 若出现的现象,则是氧气。
(3)反应仓中“通道”相当于下图装置中的(选填“c”或“d”)导管。

活动二 制作简易的家用制氧机
(4)同学们在充分思考交流的基础上,利用家庭中常见材料,设计并制作了简易家用制氧机(如图),其中C瓶的作用相当于仓(反应或过滤)。

-
12、化学科学十分重视实证和理性思维。在课堂学习中,通过选用典型物质进行实验,来探究物质的有关性质。下图所示是探究氧气化学性质的实验,请回答:
 (1)、实验一:木炭在图②中燃烧与在图①中燃烧剧烈程度(选填“不同”或“相同”),图③的实验目的是。(2)、实验二:图⑤中可观察到的现象是剧烈燃烧, , 放出大量热,产生黑色固体,反应的方程式为。(3)、实验三:观察到硫在氧气中比在空气中燃烧得更旺,生成有气味的气体,反应的方程式为;集气瓶⑦底预先放少量水来吸收生成气体二氧化硫,说明二氧化硫具有的物理性质是。(4)、比较归纳:根据上述实验,说明氧气的化学性质(填“比较活泼”或“不活泼”)。
(1)、实验一:木炭在图②中燃烧与在图①中燃烧剧烈程度(选填“不同”或“相同”),图③的实验目的是。(2)、实验二:图⑤中可观察到的现象是剧烈燃烧, , 放出大量热,产生黑色固体,反应的方程式为。(3)、实验三:观察到硫在氧气中比在空气中燃烧得更旺,生成有气味的气体,反应的方程式为;集气瓶⑦底预先放少量水来吸收生成气体二氧化硫,说明二氧化硫具有的物理性质是。(4)、比较归纳:根据上述实验,说明氧气的化学性质(填“比较活泼”或“不活泼”)。 -
13、化学兴趣小组的同学为了比较氧化铁和二氧化锰对过氧化氢分解的催化效果。用如图所示的装置先后进行了两次实验。
 (1)、实验1:取过氧化氢溶液与粉末状二氧化锰混合。
(1)、实验1:取过氧化氢溶液与粉末状二氧化锰混合。实验2:取过氧化氢溶液与混合。
(2)、在检查装置的气密性后,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,注入双氧水的方法是(填序号)。A.快速推注射器活塞 B.缓慢推注射器活塞
(3)、依据“相同时间内用二氧化锰作催化剂的反应收集的氧气体积较大”,得出结论:二氧化锰对过氧化氢分解的催化效果比氧化铁。(4)、实验过程中发现U型管内右侧液面上升,原因是该反应(填“放热”或“吸热”)(5)、为比较二氧化锰和氧化铁对过氧化氢分解快慢的不同影响,用下图装置进行实验:启动传感器,注入过氧化氢溶液。氧气体积分数随时间变化情况如下: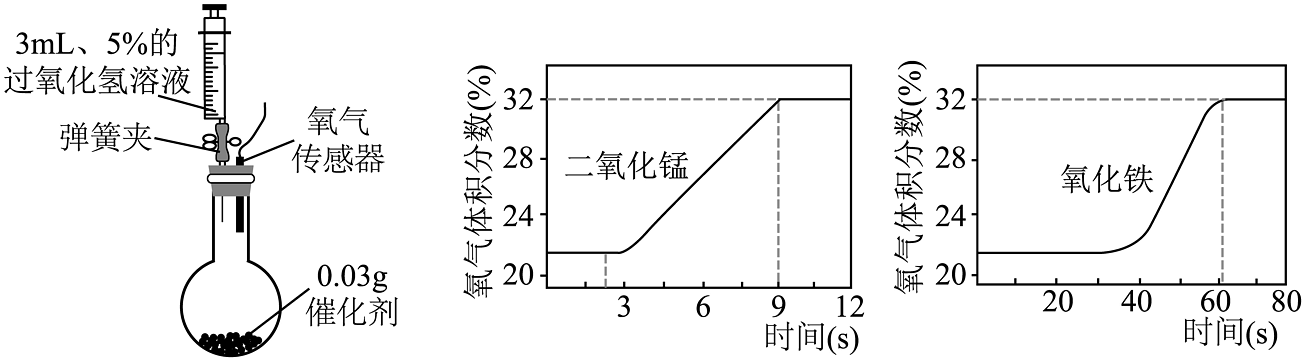
①初始时氧气的体积分数不为0,原因是。
②使过氧化氢分解较快的催化剂是(填二氧化锰或氧化铁)。
-
14、
氧气的制取
I.工业制取氧气
分离液态空气法。
膜分离技术法。利用高分子富氧膜让空气中氧分子优先通过的特性,收集高浓度的氧气。膜的渗透孔径只有几个纳米,细菌和病毒不能通过。
(1)由此判断:氧分子直径细菌直径(选填“大于”或“小于”)。
Ⅱ.实验室制取氧气
实验室有如图所示的仪器:

(2)写出仪器的名称:①。
(3)实验室用加热高锰酸钾的方法制取 , 发生装置应选用的仪器是(填仪器序号),发生反应的符号表达式为:;若用排水法收集的一瓶氧气不纯,原因可能是(写出1点即可)。
(4)若用排水法收集氧气时,当看到导管口有气泡放出时,再收集氧气。
(5)若用过氧化氢制取氧气,还需要用到一种药品是 , 该物质起作用。
(6)若用下图装置G收集氧气,气体应从导管口(填“a”或“b”通入:用该装置检验氧气已收集满的操作是。

(7)若用如下图方法收集氧气:图1的集气瓶中装有80%的水,用排水法收集氧气后,集气瓶中仍留有15%的水,如图2所示,图2集气瓶气体中氧气的体积分数是。(按空气中氧气的体积分数为21%计算,结果精确至0.1%

-
15、
为了更全面地认识氧气,兴趣小组同学以氧气为核心,开展以下主题式学习。
氧气的发现
(1)唐代化学家马和最先发现氧气,他认为空气中存在“阴阳二气”,阳气比阴气多得多。则氧气属于马和认为的(填“阳气”或“阴气”)。
(2)现代科学认为空气中的氧气主要来源于植物的。
氧气的含量
(3)二百多年前,法国化学家拉瓦锡采用图1装置,研究了空气的成分,得出了空气由氧气和组成的结论。

(4)仿照该实验的原理,同学们采用图2装置测定空气的成分。该实验中红磷燃烧,放出大量热,有黄色火焰,产生大量。该实验还说明集气瓶中剩余气体具有的性质是(合理即可)(写1条)。

-
16、按要求填空
实验室某无色液体含有物质A,为了探究其成分,实验小组进行了如下实验:
①用试管取适量该液体,向其中加入少量的黑色粉末B,在常温下能迅速产生无色气体C,而B的质量在反应前后没有改变;
②将产生的气体C收集起来;把燃着的红磷置于盛有C的集气瓶中,红磷剧烈燃烧;
③把燃着的硫置于盛有C的集气瓶中,硫剧烈燃烧,生成了一种有刺激性气味的气体D.请回答下列问题。
(1)、写出各物质的名称:A、B、C、D。(2)、请写出上述实验中发生的化学反应的符号表达式及基本反应类型。符号表达式
基本反应类型
①
①
②
②
-
17、某兴趣小组利用氧气传感器来检测足量红磷燃烧过程中氧气的含量,如图所示,下列判断不正确的是
 A、a点时容器内氮气的体积分数小于85% B、容器内水的作用主要是降温和防止污染 C、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 D、此实验测得空气中氧气的质量分数为18%
A、a点时容器内氮气的体积分数小于85% B、容器内水的作用主要是降温和防止污染 C、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 D、此实验测得空气中氧气的质量分数为18% -
18、英国科学家法拉第曾用蜡烛(主要成分为石蜡)做过一个有趣的母子“火焰”实验,如图所示,下列有关分析错误的是
 A、母火焰的外焰部分石蜡燃烧充分,无石蜡蒸气 B、若导管太长,石蜡蒸气易冷凝,不能从导管末端导出 C、导管的一端要插入母火焰的中心部位,是因为该处氧气充足 D、实验现象说明石蜡的沸点较低,受热易变成气态
A、母火焰的外焰部分石蜡燃烧充分,无石蜡蒸气 B、若导管太长,石蜡蒸气易冷凝,不能从导管末端导出 C、导管的一端要插入母火焰的中心部位,是因为该处氧气充足 D、实验现象说明石蜡的沸点较低,受热易变成气态 -
19、某学生量取液体,仰视读数为50mL,将液体倒出一部分后,俯视读数为40mL,则该同学实际倒出的液体体积为A、大于10mL B、小于10mL C、等于10mL D、无法确定
-
20、下列物质中,前者属于混合物,后者属于纯净物的是A、碘盐、酱油 B、雨水、冰水混合物 C、红磷、稀有气体 D、可乐、食醋