相关试卷
-
1、在恒容条件下,能使正反应速率增大且活化分子的百分数也增加的措施是A、增大的浓度 B、减小的浓度 C、通入使气体的压强增大 D、升高反应的温度
-
2、下列实验操作不能达到实验目的的是A、用酸式滴定管准确量取酸性溶液 B、做中和热测定实验时,在大小烧杯之间填满碎泡沫塑料以防止热量散失 C、实验室取用金属钠,多余的钠要放到废弃桶 D、做酸碱中和滴定实验时,盛装标准液的滴定管应用标准液润洗次
-
3、下列变化中,放出热量的反应是A、与固体反应 B、高温分解反应 C、生石灰跟水反应 D、盐酸与碳酸氢钠溶液反应
-
4、下列仪器使用之前不需检查漏水的是A、
 B、
B、 C、
C、 D、
D、
-
5、下列物质属于弱电解质的是A、 B、 C、 D、
-
6、弱电解质的电离平衡和盐类的水解平衡均属于化学平衡。请回答:(1)、已知在水中存在以下平衡: , , 溶液显(填“酸性”“碱性”或“中性”);等体积等物质的量浓度的溶液和NaOH溶液混合后,所得溶液中离子浓度由大到小的顺序是。(2)、在 , 溶液吸收后,若溶液 , 则溶液中;若溶液 , 则以下浓度关系正确的是(填标号)。
a.
b.
c.
(3)、常温下,向的氨水中逐滴加入的盐酸,所得溶液的pH、溶液中和的物质的量分数与加入盐酸的体积的关系如下图所示。
①的电离常数为。
②当加入盐酸的体积为25mL时,溶液中mol/L(用计算式表示)。
-
7、水是生命的源泉,水溶液中的离子平衡与我们的生产生活密切相关。(1)、时,向水的电离平衡体系中加入少量醋酸钠固体,得到pH为11的溶液,由水电离出的mol/L。(2)、时,已知 , , 则溶液的 , 溶液中离子浓度由大到小的顺序为。(3)、向溶液中滴加NaOH溶液至中性后,各离子浓度由大到小的顺序为。(4)、(亚硫酰氯)极易与水反应,生成两种酸性物质,写出该反应的化学方程式。(5)、时,向20mL的的溶液滴加amL0.1mol/L的溶液时,混合溶液的pH恰好为7。则的电离平衡常数Kb=(用含有a的式子表示)。
-
8、
目前,常利用催化技术将汽车尾气中的NO和CO转化成和。为研究如何增大该化学反应的速率,某课题组进行了以下实验探究。
【提出问题】在其他条件不变的情况下,温度或催化剂的比表面积(单位质量的物质所具有的总面积)如何影响汽车尾气的转化速率?
【查阅资料】使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响。
(1)【实验设计】请填写下表中的空白。编号
t/℃
催化剂的比表面积/(m·g)
Ⅰ
280
80.0
Ⅱ
12.0
Ⅲ
360
80.0
【图像分析与结论】
三组实验中CO的浓度随时间的变化如图所示。
 (2)写出该反应的化学方程式。(3)第Ⅰ组实验中,达到平衡时NO的浓度为(4)由曲线Ⅰ、Ⅱ可知,增大催化剂的比表面积,该化学反应的速率将(填“增大”“减小”或“无影响”)。(5)由实验Ⅰ和Ⅲ可得出的结论是。
(2)写出该反应的化学方程式。(3)第Ⅰ组实验中,达到平衡时NO的浓度为(4)由曲线Ⅰ、Ⅱ可知,增大催化剂的比表面积,该化学反应的速率将(填“增大”“减小”或“无影响”)。(5)由实验Ⅰ和Ⅲ可得出的结论是。 -
9、在一个容积不变的密闭容器中发生反应: , 其平衡常数(K)和温度(t)的关系如下表所示。
t/℃
700
800
830
1000
1200
K
0.6
0.9
1.0
1.7
2.6
请填写下列空白。
(1)、该反应的平衡常数表达式为;该反应0(填“等于”或“不等于”)。(2)、在时,向容器中充入、 , 保持温度不变,反应达到平衡后,其平衡常数1.0(填“大于”“小于”或“等于”)。(3)、若时,在某时刻反应混合物中、、、的浓度分别为、、、 , 则此时上述反应的平衡移动方向为(填“正反应方向”“逆反应方向”或“不移动”)。理由是。(4)、在时,向1L容器中充入和 , 保持温度不变,反应达到平衡后,的平衡转化率为。 -
10、按要求完成下列各小题(1)、由固体配置溶液的操作为。(2)、4g硫粉在中完全燃烧生成 , 放出37kJ热量,写出S燃烧的热化学方程式。(3)、明矾可用于净水,其净水原理(用离子方程式表示)。(4)、已知: 。在实际生产中,选定的温度为的主要原因 , 通入过量空气的目的是。
-
11、下列实验操作、现象、解释或结论都正确的是
选项
实验操作
现象
解释或结论
A
将氯化镁溶液加热灼烧
有固体析出
该固体是氯化镁
B
氯化铜溶液中有氯化铁杂质,加入氧化铜除杂
有红褐色物质析出
调节pH使铁离子水解平衡右移,生成沉淀
C
将充满的密闭玻璃球浸泡在热水中
红棕色变深
反应的
D
向的溶液中加入4滴的NaCl溶液,再加5滴的NaI溶液,再振荡
先生成白色沉淀,后产生黄色沉淀
A、A B、B C、C D、D -
12、下列说法正确的是:
①、都是强电解质
②三氧化硫的水溶液能导电,但三氧化硫是非电解质
③氨气溶于水中能导电,所以氨气是电解质
④在水溶液及熔融状态下均可电离出、、
⑤室温下,溶液与溶液的pH不同
A、①②③ B、②③⑤ C、③④⑤ D、①②⑤ -
13、是重要的消毒剂、氧化剂,研究其分解反应有重要意义。KI能催化的分解。
①不加KI:
②加入KI:;
分解反应过程中能量变化如图所示。下列判断不正确的是
 A、加入KI后:为慢反应;为快反应 B、加入KI后改变了反应的反应热 C、是吸热反应 D、KI降低了该反应的活化能
A、加入KI后:为慢反应;为快反应 B、加入KI后改变了反应的反应热 C、是吸热反应 D、KI降低了该反应的活化能 -
14、在溶液中加入溶液,所得溶液呈A、弱酸性 B、强酸性 C、碱性 D、中性
-
15、下列反应的离子方程式不正确的是A、气体通入NaClO溶液: B、明矾溶液中加入过量NaOH溶液: C、向血红色溶液加入过量铁粉: D、向硫化锌悬浊液滴加硫酸铜溶液:
-
16、下列说法中正确的是A、在时,pH约为6的纯水呈酸性 B、将盐酸稀释至1000mL,所得溶液的pH为9 C、在常温下,当水电离出的为时,此溶液的pH可能为1 D、将的盐酸和醋酸各1mL分别稀释至100mL,所得溶液的pH,醋酸大于盐酸
-
17、为了除去 MgCl2 酸性溶性中的 Fe3+ , 可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸,这种试剂是A、NH3·H2O B、MgO C、Na2CO3 D、NaOH
-
18、在相同温度时,醋酸与醋酸相比较,下列数值中,前者大于后者的是A、溶液中的物质的量 B、的电离常数 C、中和时所需NaOH的物质的量 D、溶液中的物质的量
-
19、下列反应的离子方程式不正确的是A、氧化铝溶于盐酸反应: B、碳酸银溶于稀盐酸: C、次氯酸溶液见光分解: D、溶液中通入少量氯气:
-
20、分别取40 mL 0.50 mol·L-1盐酸与40 mL 0.55 mol·L-1 氢氧化钠溶液进行中和反应反应热的测定实验。下列说法错误的是
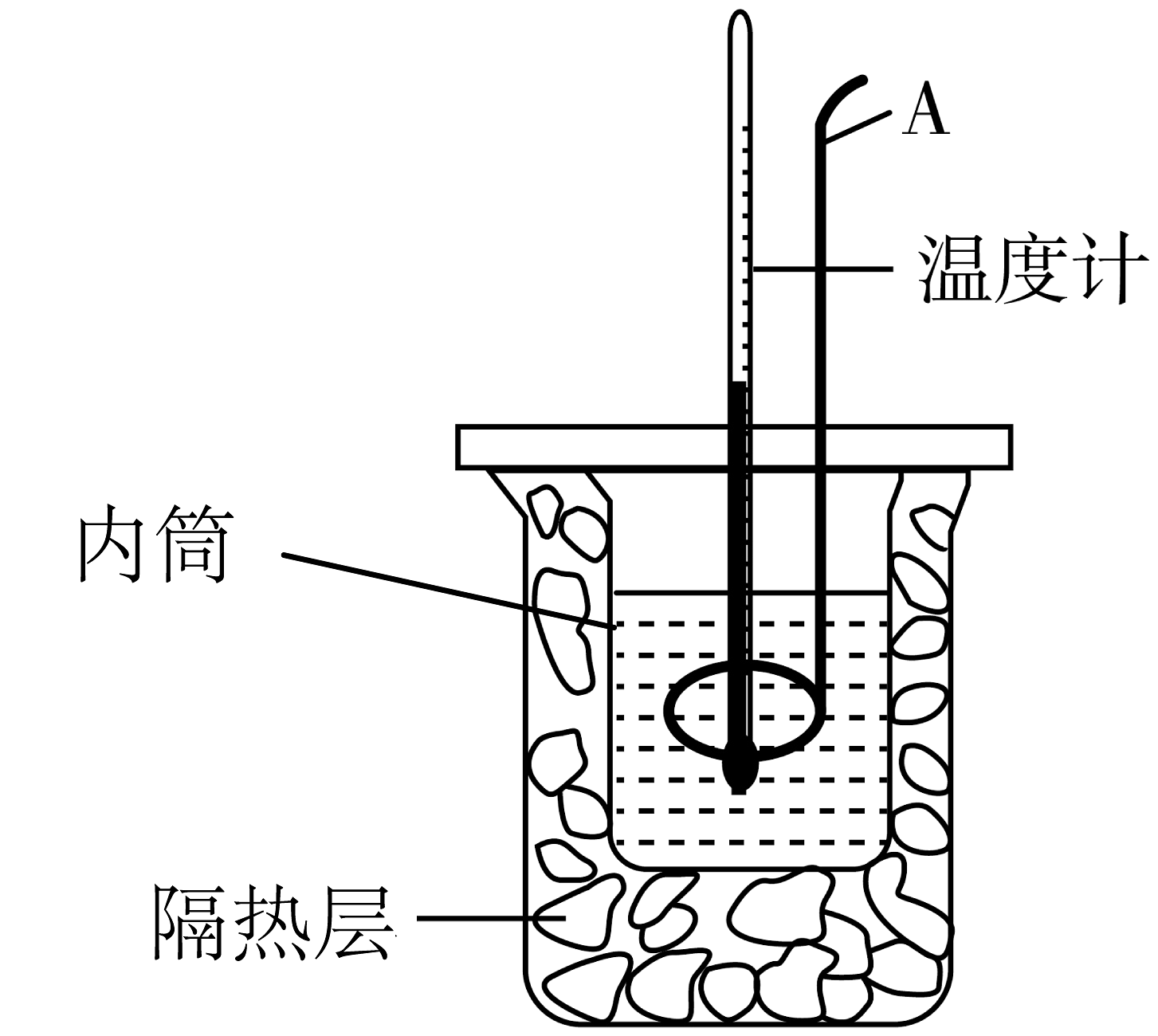 A、加入稍过量的氢氧化钠的目的是确保盐酸完全反应,减小实验误差 B、仪器A的名称是玻璃搅拌器 C、在实验过程中,测量完盐酸的温度后,把温度计上的酸用水冲洗干净后再测量NaOH溶液的温度 D、用稀醋酸代替稀盐酸,结果是一样的
A、加入稍过量的氢氧化钠的目的是确保盐酸完全反应,减小实验误差 B、仪器A的名称是玻璃搅拌器 C、在实验过程中,测量完盐酸的温度后,把温度计上的酸用水冲洗干净后再测量NaOH溶液的温度 D、用稀醋酸代替稀盐酸,结果是一样的