相关试卷
-
1、下列溶液一定显碱性的是A、能与硫酸反应的溶液 B、滴加甲基橙显黄色的溶液 C、的溶液 D、的溶液
-
2、下列物质中属于弱电解质的是A、 B、 C、 D、
-
3、二氧化碳催化加氢制甲醇有利于减少温室气体排放。涉及的主要反应如下:
Ⅰ.
Ⅱ.
Ⅲ.
(1)、 , 该反应一般认为通过反应Ⅱ和反应Ⅲ两步来实现,若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是(填标号)。A.
 B.
B.
C.
 D.
D. (2)、一定条件下,恒容密闭容器中和发生上述反应。下列说法正确的是________A、当混合气体密度不变时说明体系达到平衡状态 B、反应达到平衡状态后通入氦气,体系压强增大,反应速率不变,平衡不移动 C、使用高效催化剂,可提高甲醇的生产效率,但不能改变甲醇的平衡产率 D、实际生产中温度越低越有利于甲醇的合成(3)、不同压强下,按照投料,实验测得的平衡转化率和的平衡产率随温度的变化关系如下图所示。
(2)、一定条件下,恒容密闭容器中和发生上述反应。下列说法正确的是________A、当混合气体密度不变时说明体系达到平衡状态 B、反应达到平衡状态后通入氦气,体系压强增大,反应速率不变,平衡不移动 C、使用高效催化剂,可提高甲醇的生产效率,但不能改变甲醇的平衡产率 D、实际生产中温度越低越有利于甲醇的合成(3)、不同压强下,按照投料,实验测得的平衡转化率和的平衡产率随温度的变化关系如下图所示。
已知:的平衡转化率 , 的平衡产率其中纵坐标表示平衡转化率的是图(填“甲”或“乙”),压强、、由大到小的顺序为 , 图乙中温度时,三条曲线几乎交于一点的原因是。
(4)、一定条件下,向体积为1L的恒容密闭容器中通入1mol和3mol发生上述反应,经10分钟达到平衡,此时的转化率为80%,且体系中。的平均反应速率 , 反应Ⅱ的平衡常数。(5)、我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上反应的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
写出该历程中决速步骤的化学方程式:。
-
4、
某学习小组为了探究一定温度下(简写为HAc)电离平衡的影响因素,进行了如下实验。
Ⅰ.【实验一】测定HAc的浓度。
(1)用(填仪器名称)准确移取20.00mL HAc溶液,转移至锥形瓶,加入2滴。(填“酚酞”“石蕊”或“甲基橙”)作指示剂,用0.1000mol/L NaOH溶液滴定,平行测定4次,消耗NaOH溶液的体积分别为20.05mL、20.00mL、18.40mL、19.95mL,则。
(2)①实验操作中,滴定管盛装NaOH溶液后排气泡动作正确的是(填字母,下同)。
A.
 B.
B.  C.
C.
②下列有关实验操作的说法错误的是。
A.锥形瓶盛装HAc溶液前未干燥,对测定结果无影响
B.滴定时,左手控制滴定管活塞,右手握持锥形瓶,眼睛注视滴定管中的液面变化
C.滴定前仰视读数,滴定后读数正确,测得醋酸浓度偏低
D.接近终点时,改为滴加半滴NaOH溶液,溶液出现颜色变化,即达到滴定终点
(3)滴定醋酸溶液的过程中:
①时,溶液 , 则其中离子浓度由大到小的顺序为。
②当时,溶液pH7(填“”、“”或“”)。
Ⅱ.【实验二】探究25℃下HAc电离平衡的影响因素。
将实验一中的HAc溶液和与其等浓度的(简写为NaAc)溶液按一定体积比混合,测pH。
序号
pH
Ⅰ
40.00
/
0
2.86
Ⅱ
4.00
a
b
0
3.36
Ⅶ
4.00
c
d
4.53
Ⅷ
4.00
4.00
32.00
4.65
(4)根据表中信息,补充数据: , 。
(5)对比实验Ⅰ和Ⅱ可得结论:稀释HAc溶液,电离平衡正向移动;结合表中数据,给出判断理由:;由实验Ⅱ~Ⅷ可知,增大浓度,HAc电离平衡向移动(填“正”、“逆”)。
(6)25℃时,醋酸;次氯酸;碳酸 , ;亚硫酸 , 。、、和中结合能力最强的是。往NaClO溶液中通入少量 , 离子方程式为:。
-
5、
甲烷及其衍生物在国民经济中有着重要的作用。
Ⅰ.可利用与制备“合成气”(CO、)
某温度下,在刚性密闭容器中充入、的物质的量之比为 , 起始总压为35kPa,使其发生及应:
(1)研究表明CO的生成速率 , 某时刻测得 , 则该时刻________。
(2)达到平衡后,测得CO的产率为50%,则该反应的平衡常数________。
(3)如该反应改为在恒容绝热容器中进行,反应达到平衡状态的标志是________(填字母)。
A.混合气体的总质量保持不变 B.、CO的浓度比为
C.容器内混合气体的压强保持不变 D.容器内混合气体的密度保持不变
E.容器内温度保持不变 F.
Ⅱ.工业上还可以用催化还原消除氮氧化物的污染
(4)已知: , 向体积为1L的刚性密闭容器中加入1.4mol和一定量NO在不同温度下发生该反应,的浓度变化如图所示,下列说法正确的是________(填序号)。
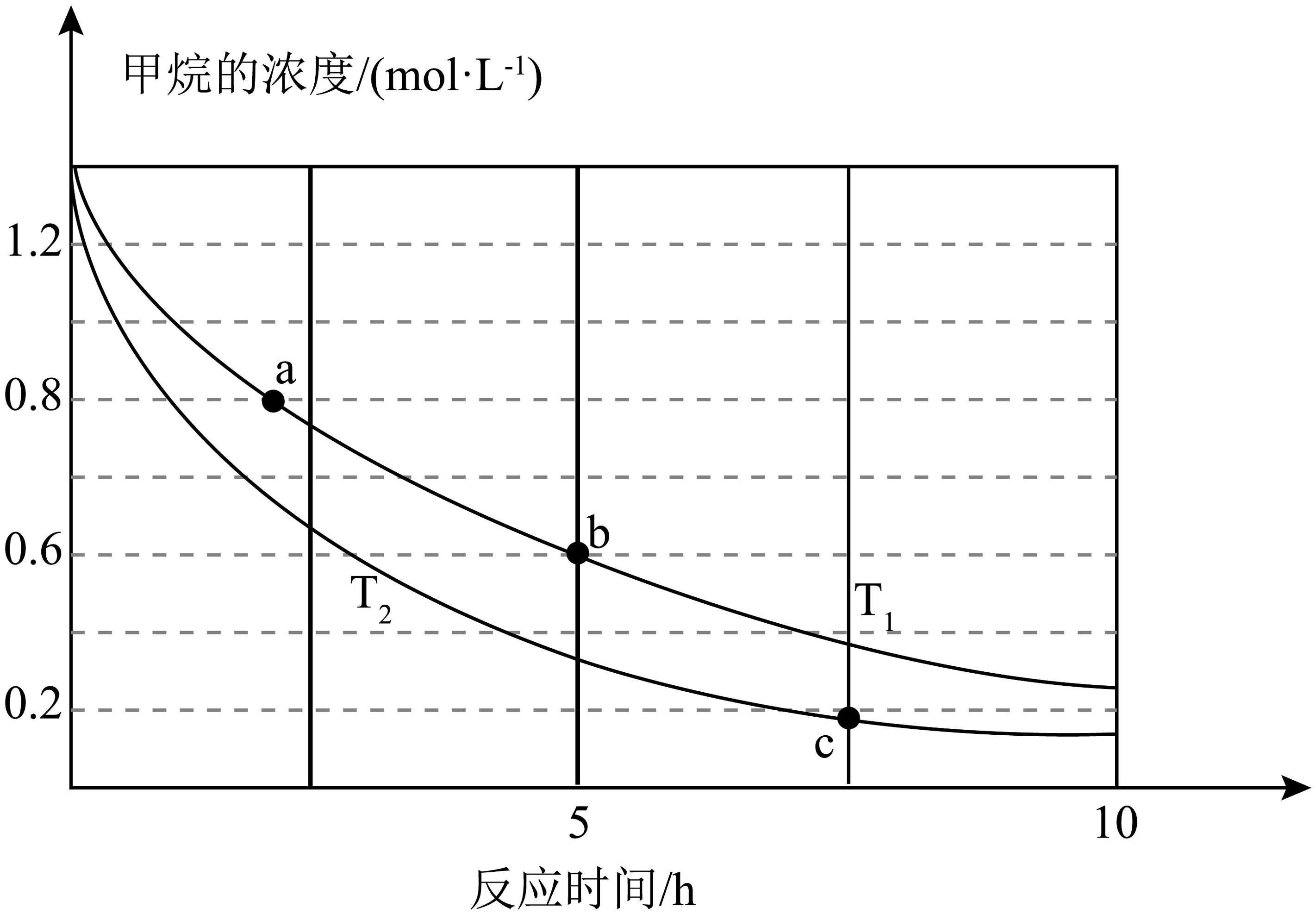
A. B. b点时氮气的浓度为1.6mol/L C. a点正反应速率大于b点的逆反应速率 D. a点的反应速率比c点的反应速率小 (5)查阅资料可知NO氧化反应历程分两步:(其中k为速率常数)
①(快)
②
一定温度下,反应达到平衡状态,请写出用、、、表示的平衡常数表达式________。
-
6、回答下列问题:(1)、已知一些化学键的键能数据如表所示:
化学键
C—H
C—F
H—F
F—F
键能
414
489
565
155
请根据键能数据写出和反应生成和的热化学方程式:。
(2)、25℃时,的NaOH溶液中由水电离出的 , 向其中加入的盐酸溶液直至过量,水的电离程度变化情况为。(3)、若在木卫六上某地,水的离子积常数 , 利用我们的地球经验,木卫六上该地的温度(填“大于”“小于”或“等于”)25℃。若用pH试纸测定该温度下纯水的pH,则试纸显色。(4)、某温度下 , 将的溶液与等物质的量浓度的溶液等体积混合,所得混合液的。(5)、常温下的电离平衡常数 , , 用NaOH溶液吸收得到的溶液,试计算溶液中。 -
7、温度为时,用的盐酸分别滴定的氨水和溶液(碱性:强于),溶液的与或的关系如图所示,。下列说法错误的是
 A、曲线I对应的是滴定的曲线 B、a点对应的溶液 C、b、e点溶液中水的电离程度: D、f点溶液中
A、曲线I对应的是滴定的曲线 B、a点对应的溶液 C、b、e点溶液中水的电离程度: D、f点溶液中 -
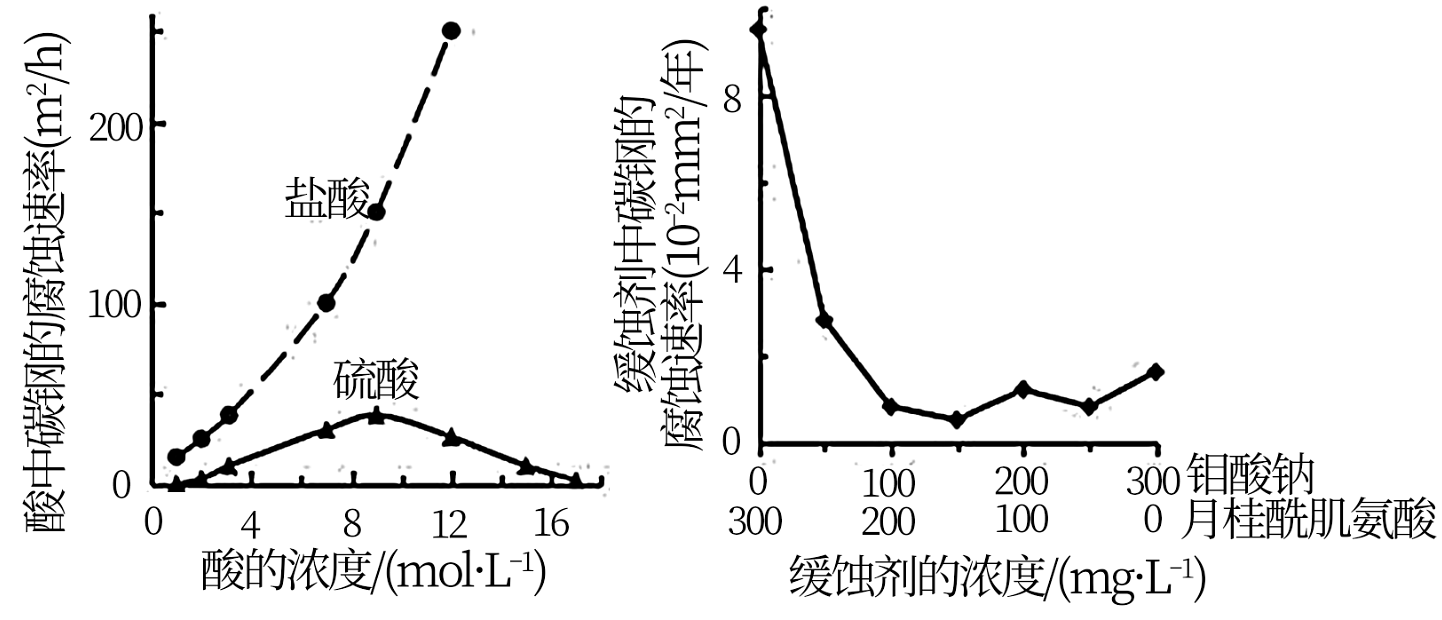
8、钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。
下列说法不正确的是
A、盐酸的浓度越大,腐蚀速率越快 B、钼酸钠和月桂酰肌氨酸的浓度相等时,缓蚀效果最好 C、碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正相关 D、对比盐酸和硫酸两条曲线,可知Cl-也会影响碳素钢的腐蚀速率 -
9、下列装置及设计不能达到实验目的的是
 A、测定中和反应的反应热 B、比较Fe3+和Cu2+对H2O2分解反应的催化效果 C、测定锌与稀硫酸反应生成氢气的速率 D、探究温度对化学平衡的影响
A、测定中和反应的反应热 B、比较Fe3+和Cu2+对H2O2分解反应的催化效果 C、测定锌与稀硫酸反应生成氢气的速率 D、探究温度对化学平衡的影响 -
10、如图,向1 L恒容密闭容器中充入2 mol NO和1 mol , 发生反应 kJ/mol,下列说法正确的是
 A、 , B、200℃时,0~10min内 C、12分钟时,200℃和T℃下该反应化学平衡常数恰好相等 D、若起始时向容器中充入4 mol NO和2 mol , 则200℃平衡后,NO的物质的量小于3.7 mol
A、 , B、200℃时,0~10min内 C、12分钟时,200℃和T℃下该反应化学平衡常数恰好相等 D、若起始时向容器中充入4 mol NO和2 mol , 则200℃平衡后,NO的物质的量小于3.7 mol -
11、已知电离常数: , , 。下列离子方程式书写正确的是A、饱和碳酸钠溶液中通入 B、氢氧化铁溶于氢碘酸(强酸): C、向中通入少量的气体: D、同浓度同体积的溶液与NaOH溶液混合:
-
12、某温度下,密闭容器中发生反应aX(g)bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积扩大到原来容积的两倍,当达到新平衡时,物质Y和Z的浓度均是原来的0.6倍。则下列叙述正确的是A、可逆反应的化学方程式的化学计量数:a<b+c B、扩大容器的容积时,v正增大,v逆减小 C、达到新平衡时,物质X的转化率减小 D、达到新平衡时,混合物中Z的质量分数减小
-
13、某化学兴趣小组的同学将溶液和溶液倒入淀粉和的混合溶液中,该实验的反应原理有①;②;③(橙红色)。观察到的现象为先产生橙红色沉淀,几秒钟后溶液颜色变为蓝色。下列说法错误的是A、反应①对反应②的进行有促进作用 B、该实验条件下,反应速率:③>② C、反应后混合液的pH减小 D、可以用溶液代替溶液进行上述实验
-
14、下列溶液一定呈中性的是A、pH=7的溶液 B、的溶液 C、由酸碱中和反应得到的溶液 D、非电解质溶于水得到的溶液
-
15、下列事实可用化学平衡移动原理解释的是A、在容器中充入一定量的与 , 达到平衡后压缩容器容积以增大压强,混合物颜色加深 B、实验室制备氢气时,选择纯度不高的粗锌与稀硫酸反应 C、将肝脏研磨液加入过氧化氢溶液,发现有气泡产生,加热后气泡产生速率减慢 D、实验室可用排饱和食盐水的方法收集氯气
-
16、对于常温下pH=3的醋酸溶液,下列说法正确的是A、加水稀释后,溶液中c(H+)和c(OH-)都减小 B、加水稀释到原体积的10倍后,溶液pH变为4 C、加入少量醋酸钠固体,溶液pH降低 D、与等体积pH=3的盐酸比较,醋酸跟足量锌粒反应产生的H2更多
-
17、下列关于化学反应与能量的说法正确的是A、已知正丁烷的燃烧热为 , 则表示正丁烷燃烧热的热化学方程式为 B、1mol甲烷气体和2mol氧气的总能量大于1mol二氧化碳气体和2mol液态水的总能量 C、热化学方程式书写时须注明反应的温度和压强,不注明时表明温度和压强分别是0℃和101kPa D、已知 , 则金刚石比石墨稳定
-
18、下列关于工业合成氨的叙述正确的是A、合成氨工业温度选择为450℃左右,主要是为了提高的平衡产率 B、使用催化剂和施加高压,都能提高反应速率,但对化学平衡无影响 C、将液化分离以及、循环使用均能提高合成氨反应速率和原料转化率 D、为了提高氢气的转化率,可适当增加氮气浓度
-
19、下列关于自发反应的说法正确的是A、反应产物的分子数比反应物多,则该反应 B、反应的 C、室温下不能自发进行,说明该反应的 D、非自发过程在任何条件下都不可能转变为自发过程
-
20、
明年是苯发现的两百周年,以苯为代表的芳香族化合物在各领域有广泛应用。
Ⅰ.苯乙烯()是重要的化工原料,工业上制苯乙烯的主流方法是乙苯()脱氢法,包括多种不同工艺路线,其主反应相同,最大区别是原料中添加的气体不同:传统乙苯脱氢(添加水蒸气稀释),氧化脱氢(添加),氧化脱氢(添加)。其中涉及的主要反应方程式如下:
ⅰ:(主反应)
ⅱ:(氧化脱氢还涉及的反应)
ⅲ:(氧化脱氢还涉及的反应)
请回答:
(1)氧化脱氢工艺中发生反应ⅳ:。
①________。
②反应ⅳ自发进行的条件是________。
(2)在恒温恒压条件下进行传统乙苯脱氢(反应ⅰ),可能发生2个副反应(活化能接近):
ⅴ:
ⅵ:
①以乙苯和水蒸气为原料,仅发生反应ⅰ、ⅴ、ⅵ,平衡时测得乙苯转化率为50%,芳香烃产物苯乙烯、苯、甲苯()的选择性S()分别为80%、10%、10%,反应ⅵ的平衡常数________(用分数表示)。
②下列说法正确的是________。
A.水蒸气温度较高,可为反应提供热量,且有利于减少催化剂表面的积碳
B.若其他条件不变,用等物质的量的替换水蒸气,可增大乙苯的平衡转化率
C.氧化脱氢法中苯乙烯易被过度氧化,使产品纯度降低
D.随着反应进行,和的增大程度相同
Ⅱ.重氮化反应是制备芳香族化合物的重要反应。若以Br为催化剂,作氧化剂,盐酸酸化(浓度恒定),反应方程式为:。在恒温密闭容器中反应,总反应的速率为v,反应历程中的三个基元反应如下,且基元反应ⅷ的。
ⅶ: (快速平衡)
ⅷ: (慢反应)
ⅸ: (快反应)
(3)下列说法正确的是__________。
A. 在反应过程中几乎不变 B. 其他条件不变,v与近似成正比 C. 增大 , v显著增大 D. 若且其他条件相同,和可能相等 (4)某反应条件下,反应过程中随时间t的变化如图。其他条件不变,增大初始 , 在图中画出随时间t变化的曲线________(注意曲线极值点的坐标)。
