相关试卷
-
1、填空(1)、硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:(已知S、Se、Te为同一主族元素)
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
①写出步骤ii中的化学方程式:。
②下列说法合理的是(填字母)。
a.SeO2既有氧化性又有还原性,其还原性比SO2强
b.浓硒酸可能具有强氧化性、脱水性
c.热稳定性:H2Se<HCl<H2S
d.酸性:H2SeO4<HBrO4<HClO4
(2)、碲(Te)广泛用于彩色玻璃和陶瓷生产。工业上用精炼铜的阳极泥(主要含有TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如图:
已知TeO2微溶于水,易溶于较浓的强酸和强碱溶液。
①“碱浸”时发生反应的离子方程式为
②碱浸后的“滤渣”可以部分溶于稀硝酸,发生反应的化学方程式是。
③“酸溶”过程中发生的化学方程式为:。
-
2、氯酸钾和浓盐酸制备的中含有水蒸气和 , 某同学设计如图实验装置(部分夹持仪器已省略),验证混合气中的水蒸气和 , 并验证氯气的某些性质。

已知:①能与溶液反应生成血红色溶液;
②易溶于不溶于。
回答下列问题:
(1)、若将换成 , 使用装置A能否产生?(填“能”或“否”),原因是。(2)、装置B的作用是。(3)、装置E中的现象是湿润的有色布条 , 其原因是(用离子方程式表示)。(4)、验证具有氧化性的现象是。(5)、验证混合气中有的现象是。(6)、装置G中发生的离子反应方程式是。 -
3、有一无色透明溶液可能含有下列离子中的某些离子:、、、、、、和。为确定该溶液中所含离子,分别取四份溶液进行以下操作。
操作Ⅰ:向第1份溶液中滴入紫色石蕊溶液,溶液呈蓝色。
操作Ⅱ:向第2份溶液中滴入溶液,无白色沉淀产生。
操作Ⅲ:向第3份溶液中先滴加稀硝酸再加溶液,产生白色沉淀。
操作Ⅳ:向第4份溶液中滴入少量溶液,产生白色沉淀。
请回答下列问题:
(1)、根据题干中“无色透明溶液”判断原溶液中肯定不存在的离子有。(2)、根据操作Ⅰ判断原溶液中肯定存在的离子有;肯定不存在的离子有。(3)、根据操作Ⅱ判断原溶液中肯定不存在的离子有。(4)、操作Ⅲ离子方程式。(5)、根据操作Ⅳ判断原溶液中肯定存在的离子有。(6)、根据以上操作无法判断是否存在的离子有。 -
4、室温下,向溶液中加入稀溶液,溶液中主要微粒的分布系数【如的分布系数】以及随变化如图。

下列叙述错误的是
A、溶液中 , 水电离受到促进 B、加入稀溶液过程中,溶液满足关系式 C、 D、加入少量时,先与发生主要反应 -
5、有机物液流电池因其电化学性能可调控等优点而备受关注。南京大学研究团队设计了一种水系分散的聚合物微粒“泥浆”电池(图1)。该电池在充电过程中,聚对苯二酚(图2)被氧化,下列说法错误的是
 A、放电时,电流由a电极经外电路流向b电极 B、充电时,a电极附近的pH减小 C、充电时,b电极的电极反应方程式为
A、放电时,电流由a电极经外电路流向b电极 B、充电时,a电极附近的pH减小 C、充电时,b电极的电极反应方程式为 +4ne-+4nH+=
+4ne-+4nH+= D、电池中间的隔膜为特殊尺寸半透膜,放电时H+从a极区经过半透膜向b极区迁移
D、电池中间的隔膜为特殊尺寸半透膜,放电时H+从a极区经过半透膜向b极区迁移
-
6、1~20号元素R、X、Y、Z的原子序数依次增大,“毅力”号火星车收集的岩石成分之一是 ZYR3 , R、Y的原子序数之和为22,最外层电子数之和为10,R、X的简单阴离子的电子层结构相同。下列推断正确的是A、原子半径:Z> Y> X B、最简单氢化物的稳定性:X>Y>R C、ZR2只含一种化学键 D、工业上通过电解熔融的ZX2来制备Z的单质
-
7、已知“凡气体分子总数增加的反应都是熵增大的反应”。下列反应在任何温度下都不自发进行的是A、2O3(g)=3O2(g) H<0 B、2CO(g)=2C(s)+O2(g) H>0 C、N2(g)+3H2(g)=2NH3(g) H<0 D、CaCO3(s)=CaO(s)+CO2(g) H>0
-
8、铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:①②③。下列离子氧化性比较顺序正确的是A、 B、 C、 D、
-
9、NA代表阿伏加 德罗常数的值。下列说法正确的是A、1molHC≡CH分子中所含σ键数为5 NA B、1L0.1 mol·L-1的Na2CO3溶液含的数目为0.1 NA C、78 g Na2O2与足量水完全反应,电子转移数为NA D、标准状况下,2.24 L C2H5OH所含氢原子数为0.6 NA
-
10、下列说法不正确的是A、①正丁烷②异丁烷沸点由高到低的顺序是①>② B、聚乙烯能使溴水褪色 C、丙烯与HCl加成可以得到互为同分异构体的两种有机物 D、由甲烷结构可知CCl4也是正四面体结构,而丙烯所有原子不可能共面
-
11、下列各组中的离子,能在无色透明的溶液中大量共存的是A、、、、 B、、、、 C、、、、 D、、、、
-
12、下列关于物质分类的正确组合是
碱
酸
盐
碱性氧化物
酸性氧化物
A
NaHSO4
Al2O3
B
NaOH
HCl
NaCl
CO
C
Mg(OH)Cl
Mn2O7
D
KOH
H2S
CaO
A、A B、B C、C D、D -
13、某课题小组拟选择如图所示部分装置制备并收集二氧化氯来探究其漂白性(装置不可重复使用)。
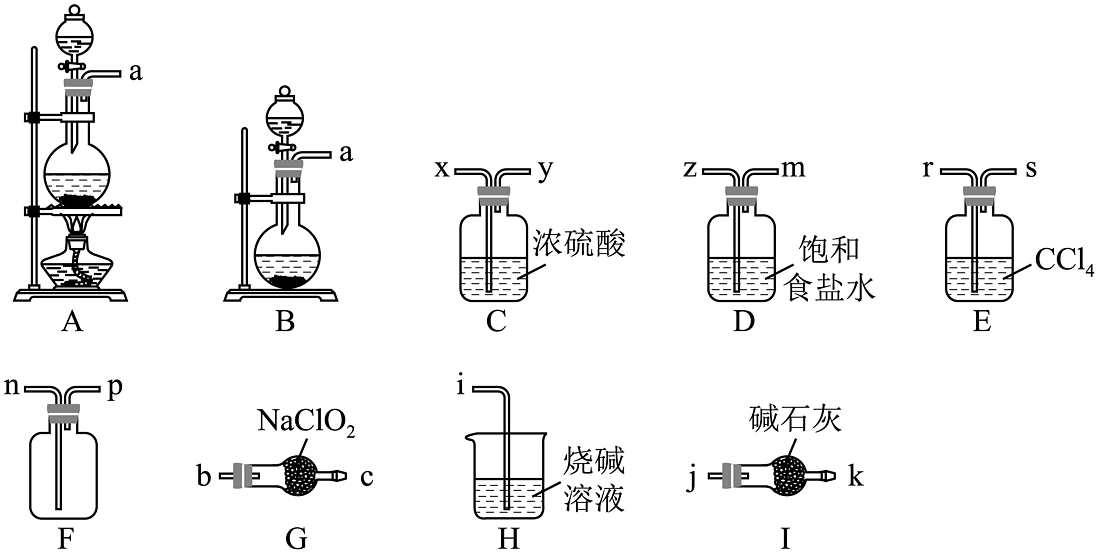
已知:①常温下,亚氯酸钠(NaClO2)与氯气反应的生成物之一为二氧化氯;②常温常压下,ClO2是一种易溶于水而难溶于有机溶剂的气体
②Cl2是一种易溶于有机溶剂而难溶于水的气体
回答下列问题:
(1)、制备干燥、纯净的氯气。气体发生装置是(填字母),反应的离子方程式为。(2)、制备二氧化氯。导管口连接顺序为a→→n→p→j。本实验选择装置I而不选择装置H的原因是。(3)、写出装置G中发生反应的化学方程式为。(4)、装置E的作用是 , 装置D的作用是。(5)、二氧化氯还会与H2O2和NaOH的混合溶液反应,其产物之一是NaClO2 , 写出该反应的化学方程式。 -
14、
Ⅰ.“价—类二维图”是一种体现“元素观”“分类观”“转化观”指导下实现元素化合物知识结构化的工具,它的核心是元素,方法是分类,内涵是转化。如图为钠及其化合物的“价—类二维图”,请回答下列问题:
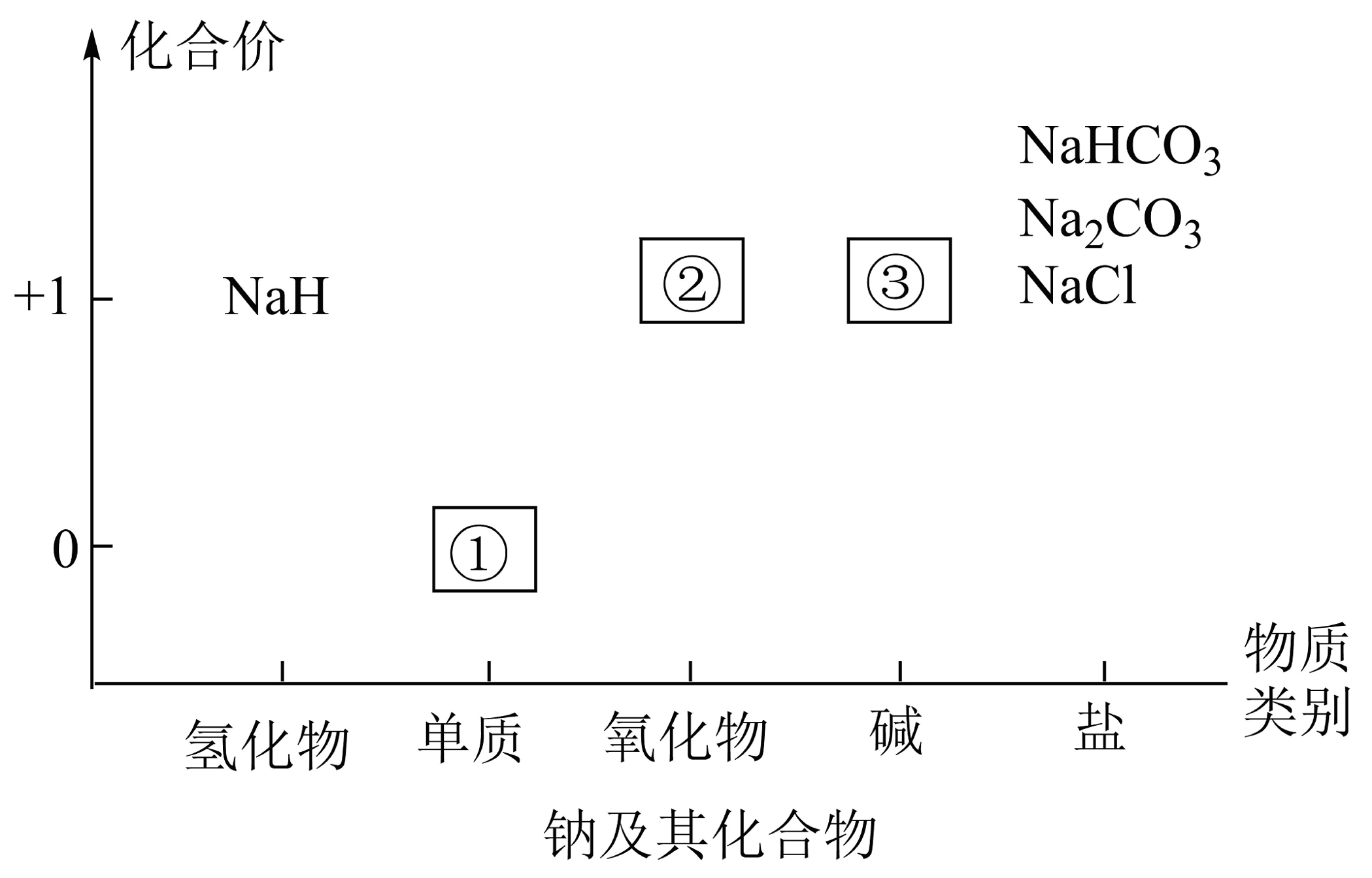
(1)①在空气中燃烧产物的阴阳离子个数比为。
(2)与水反应的化学方程式为 , NaH作剂。1molNaH参与反应,转移的电子数为
(3)写出③与NaHCO3反应的离子方程式。
Ⅱ.实验室工作人员用晶体配制溶液。
(4)选择仪器:所必需的玻璃仪器除烧杯、玻璃棒外,还有。
(5)计算,称量:需用天平称量克固体。溶解:恢复到室温,转移、洗涤、定容。定容的操作是:继续向容量瓶中加入蒸馏水,直到液面离刻度线时改用胶头滴管加水至溶液凹液面最低处与刻度线相切,盖好瓶塞,反复上下颠倒,摇匀。
(6)下列操作会使标准液浓度偏低的是。
A.定容时,加水超过刻度线,用胶头滴管吸取多余的液体
B.容量瓶未经干燥即用来配制溶液
C.定容时,俯视刻度线
D.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
E.碳酸钠晶体不纯,其中混有氯化钠
-
15、现有八种物质:①Ba(OH)2;②熔融KCl;③KHSO4;④乙醇;⑤液态氯化氢;⑥澄清石灰水;⑦CO2;⑧Zn;⑨FeCl2溶液,回答下列问题:(1)、上述物质中属于电解质的是(填序号,下同),属于非电解质的是 , 属于盐的是。(2)、写出物质③溶于水的电离方程式。(3)、写出过量③加入①中发生反应的离子方程式。(4)、检验⑨中的阳离子。
-
16、不同条件下,当KMnO4与KI按照反应①②的化学计量比恰好反应,结果如下。
反应序号
起始酸碱性
KI
KMnO4
还原产物
氧化产物
物质的量/mol
物质的量/mol
①
酸性
0.001
n
Mn2+
I2
②
中性
0.001
10 n
MnO2
IO
已知:MnO的氧化性随酸性减弱而减弱。下列说法正确的是
A、反应①,n(Mn2+)∶n(I2)=1∶5 B、对比反应①和②,x=5 C、反应①方程式:10I-+2MnO+16H+=2Mn2++5I2+8H2O D、随反应进行,体系碱性变化:①增强,②不变 -
17、三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是A、当它们的温度和压强均相同时,三种气体的密度: B、当它们的温度和密度都相同时,三种气体的压强: C、当它们的质量和温度、压强均相同时,三种气体的体积: D、当它们的压强和温度均相同时,三种气体的质量:
-
18、体积为VmL,密度为的ρg/cm3含有相对分子质量为M的某种物质的溶液,其中溶质为mg,其物质的量浓度为cmol/L,溶质的质量分数为w%,则下列表示正确的是A、 B、 C、c= D、
-
19、如图为铁元素的价类二维图,“”表示物质间的转化关系。下列说法正确的是
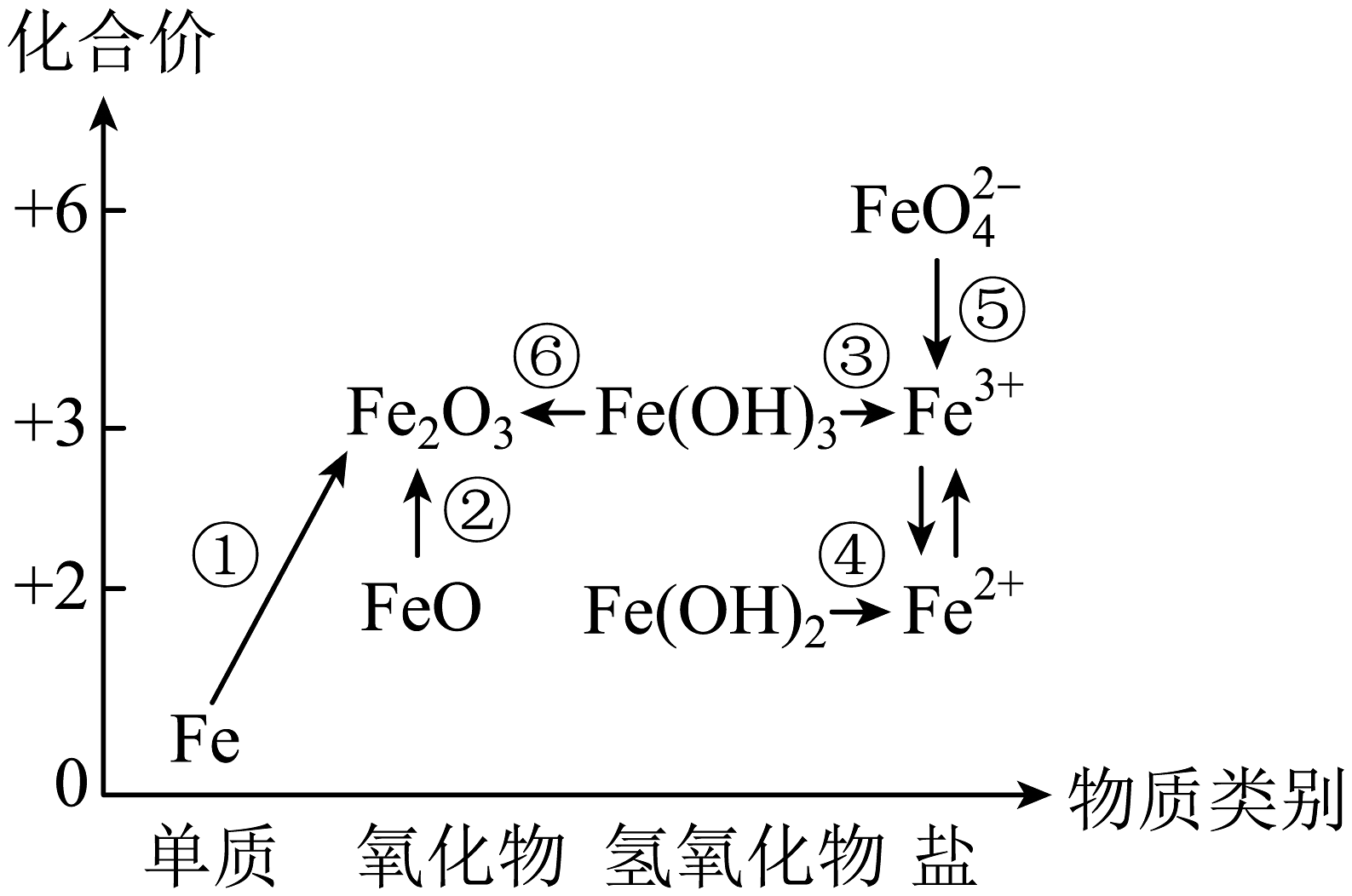 A、铁与水蒸气在高温条件下反应可实现转化① B、FeO在空气中受热可实现转化② C、溶解于足量稀硝酸可实现转化④ D、高铁酸盐(FeO)具有强氧化性,可用于杀灭水中细菌
A、铁与水蒸气在高温条件下反应可实现转化① B、FeO在空气中受热可实现转化② C、溶解于足量稀硝酸可实现转化④ D、高铁酸盐(FeO)具有强氧化性,可用于杀灭水中细菌 -
20、下列各离子组在指定的溶液中能够大量共存的是A、无色透明溶液中:、、、 B、使紫色石蕊溶液呈红色的溶液中:、、、 C、使酚酞试液呈红色的溶液中:、、、 D、溶液加入铝片可以产生:、、、