相关试卷
-
1、下列离子方程式书写正确的是( )A、氢氧化钠溶液和稀盐酸反应:H++OH-=H2O B、大理石与盐酸反应制取二氧化碳:+ 2H+=H2O + CO2↑ C、铁粉投入FeCl3溶液中:Fe + Fe3+=2Fe2+ D、用小苏打治疗胃酸过多:+ 2H+=CO2↑+H2O
-
2、下列生活中常见物质的俗名与化学式相对应的是( )A、纯碱—NaHCO3 B、石灰石—Ca(OH)2 C、铁红—FeO D、酒精—C2H5OH
-
3、下列各组选项中属于同位素的是( )A、与 B、O2与O3 C、与 D、金刚石和石墨
-
4、下列说法正确的是( )A、石墨导电,所以是电解质 B、SO2的水溶液导电,所以SO2是电解质 C、固体NaCl不导电,所以NaCl是非电解质 D、CaCO3虽然难溶于水但CaCO3是电解质
-
5、胶体在人们的日常生活中随处可见。下列分散系属于胶体的是( )A、泥水 B、豆浆 C、生理盐水 D、油水混合物
-
6、某含锰废料中主要含及少量的 , 、 , 以此为原料制备的流程如下:
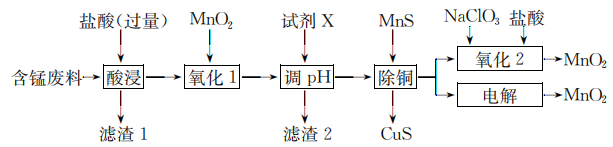
Ⅰ.氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物
开始沉淀时
8.3
6.3
2.7
4.7
完全沉淀时
9.8
8.3
3.7
6.7
Ⅱ.常温下、。
回答下列问题:
(1)、滤渣1的主要成分是(填化学式)。(2)、“氧化1”的目的是(用离子方程式表示)。(3)、“调”时,试剂X为(任写一种),|的调节范围为。(4)、“除铜”时,当溶液中 , 溶液中=。(5)、“氧化2”制备(恰好完全反应)时,=();“电解”制备的阳极电极反应式为。 -
7、水溶液中的离子反应与平衡在生产和生活中有广泛的用途。回答下列问题:(1)、25℃时,若向氨水中加入少量硫酸铵固体,则溶液中将(填“增大”“减小”或“不变”)。(2)、25℃时,若向氨水中加入稀硫酸,使氨水恰好被中和,写出反应的离子方程式:;所得溶液的7(填“>”“<”或“=”),用离子方程式表示其原因:。(3)、25℃时,若向氨水中加入稀硫酸至溶液的 , 此时溶液中 , 则=。(4)、25℃时,为配制:溶液,取固体少许溶于2~3mL水中,有白色沉淀产生,此溶液的7(填“<”“>”或“=”),配制;溶液的正确方法是。(5)、在化学分析中,以标准溶液滴定溶液中的时,采用为指示剂,利用与反应生成砖红色沉淀指示滴定终点。当溶液中的恰好沉淀完全(浓度等于)时,溶液中= , =(结果保留两位有效数字。已知:25℃时、的分别为和。)
-
8、酸性锌锰干电池是一种常用的一次电池,其结构如图所示。该电池在放电过程中产生和。回答下列问题:
 (1)、该电池的正极为(填“”或“”)极,该电池总反应的化学方程式为。(2)、如图为电解100mL溶液的装置,该装置的电源为上述酸性锌锰干电池。
(1)、该电池的正极为(填“”或“”)极,该电池总反应的化学方程式为。(2)、如图为电解100mL溶液的装置,该装置的电源为上述酸性锌锰干电池。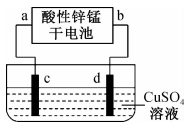
①电解一段时间后,石墨电极出现的现象为;石墨电极上的电极反应式为。
②当上述电池消耗3.25g时,电解后溶液中为(忽略电解前后溶液体积变化)。欲将电解后的溶液恢复至原溶液,应加入的试剂是 , 其质量为g。
-
9、在1L密闭容器中发生反应: , 其化学平衡常数与温度的关系如下表:
(℃)
650
700
800
830
1000
0.5
0.6
0.9
1.0
1.7
回答下列问题:
(1)、该反应的(填“>”或“<”)0。(2)、某温度时,测得平衡体系中各物质的物质的量浓度相等,则此时对应的温度为℃。保持温度和体积不变,充入一定量的 , 则平衡常数(填“增大”“减小”或“不变”)。(3)、下列措施不能提高的平衡转化率的是____(填字母)。A、选择适当的催化剂 B、增大压强 C、及时分离出 D、升高温度(4)、650℃时,将2mol和3mol投入上述容器中开始反应,达到平衡时的转化率为。(5)、800℃时,某时刻测得 , , ¹、 , 则此时反应是否达到平衡状态(填“是”或“否”),此时,(填“>”“<”或“=”)。 -
10、某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,装置如图所示。其中乙装置中X为阳离子交换膜。下列有关说法错误的是( )
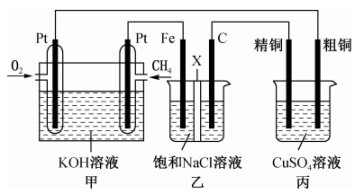 A、通入的极为正极,该电极反应式为 B、乙装置中铁电极为阴极,电极反应式为 C、反应一段时间后,乙装置中在铁电极区生成氢氧化钠溶液 D、反应一段时间后,丙装置中硫酸铜溶液浓度可能减小
A、通入的极为正极,该电极反应式为 B、乙装置中铁电极为阴极,电极反应式为 C、反应一段时间后,乙装置中在铁电极区生成氢氧化钠溶液 D、反应一段时间后,丙装置中硫酸铜溶液浓度可能减小 -
11、强碱的溶液和等体积、等物质的量浓度的弱酸的溶液混合后,溶液中有关离子浓度的大小关系是( )A、 B、 C、 D、
-
12、现进行下列实验。
将溶液和溶液等体积混合,得到悬浊液;将悬浊液过滤,得到滤液和白色沉淀。
向滤液中滴加溶液,滤液出现浑浊。
向沉淀中滴加溶液,沉淀变为黄色。
下列关于上述实验的分析错误的是( )
A、悬浊液中存在沉淀溶解平衡: B、滤液中不含 C、实验(3)表明转化为 D、实验可以证明的比的小 -
13、下列装置或操作正确且对应的实验能达到实验目的的是( )A、测定溶液的浓度
 B、测定中和反应反应热
B、测定中和反应反应热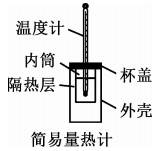 C、通过注射器活塞右移,验证与反应放热
C、通过注射器活塞右移,验证与反应放热 D、研究 , 对分解速率的影响
D、研究 , 对分解速率的影响
-
14、在一定条件下,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图所示,则下列叙述正确的是( )
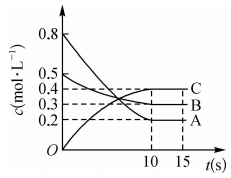 A、该反应的化学方程式为 B、反应物A的平衡转化率为60% C、0~10s内,A的平均反应速率为 D、在10~15s内,
A、该反应的化学方程式为 B、反应物A的平衡转化率为60% C、0~10s内,A的平均反应速率为 D、在10~15s内, -
15、常温下,下列各组离子在指定溶液中一定能大量共存的是( )A、的溶液:、 , 、 B、含的溶液:、、、 C、滴加甲基橙试液显红色的溶液:、 , , D、水电离出来的的溶液:、、、
-
16、将金属X连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。下列有关说法错误的是( )
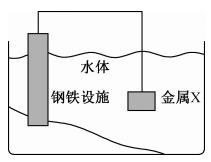 A、钢铁设施表面因有电子流入而被保护 B、钢铁设施的电极反应式为 C、形成电化学保护时,金属X作负极 D、通常情况下,钢铁设施在海水中的腐蚀速率比在河水中的快
A、钢铁设施表面因有电子流入而被保护 B、钢铁设施的电极反应式为 C、形成电化学保护时,金属X作负极 D、通常情况下,钢铁设施在海水中的腐蚀速率比在河水中的快 -
17、恒温下气体反应达到化学平衡,平衡常数。恒容时,若降低温度,D的浓度增大。下列说法错误的是( )A、该反应的化学方程式为 B、增大、 , 减小 C、恒容时,向容器中充入 , 反应速率不变 D、正反应为放热反应
-
18、实验室用标准溶液滴定未知浓度的溶液,下列说法或操作正确的是( )A、滴定前锥形瓶用溶液润洗2~3次 B、将标准溶液置于碱式滴定管中备用 C、滴定前俯视读数、滴定后仰视读数会导致滴定结果偏高 D、当锥形瓶内溶液颜色由浅绿色变为紫红色时,立即记下滴定管液面所在刻度
-
19、与的反应分①②两步进行,其能量曲线如图所示,下列有关说法正确的是( )
 A、反应①、反应②均为吸热反应 B、活化能:反应①<反应② C、反应速率:反应①>反应② D、
A、反应①、反应②均为吸热反应 B、活化能:反应①<反应② C、反应速率:反应①>反应② D、 -
20、下列叙述中错误的是( )A、生铁中含有碳,抗腐蚀能力比纯铁弱 B、用锡焊接的铁质器件,焊接处易生锈 C、在铁制品上镀铜时,铁制品为阳极,铜盐为电镀液 D、铁管上镶嵌锌块,铁管不易被腐蚀