相关试卷
-
1、金属材料是人类社会发展的见证者,在人类社会各个转型期起到了举足轻重的作用,即使在信息材料、功能材料、纳米材料飞速发展的今天,金属材料的地位仍举足轻重。下列关于金属材料的说法中正确的是( )A、合金具有金属特性,合金中不含非金属元素 B、铜比铁先成功冶炼的原因是铜比铁活泼 C、储氢合金能大量吸收氢气,并与氢气结合成金属氢化物 D、生铁具有良好的延展性,可以锻轧和铸造
-
2、高铁酸钠是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体.某工厂利用废金属屑(主要成分为和 , 含有少量)制取并回收金属 , 工艺流程如下:
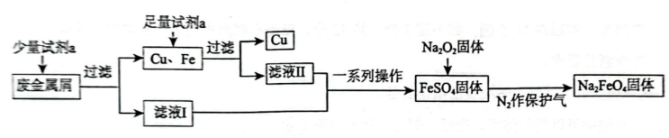 (1)、试剂为(填化学式);在过滤操作中要使用玻璃棒,其作用是 .(2)、证明滤液Ⅰ中无的实验方法是;用离子方程式解释滤液Ⅰ不含有可能的原因 .(3)、流程中固体不可暴露在空气中时间过长,原因是(用化学方程式表示).(4)、高铁酸钠中铁的化合价为价.高铁酸钠处理水过程中所发生的化学反应主要为(胶体) , 该反应中物质的氧化性强弱关系是(填“>”或“<”) . 净水时能吸附悬浮物的原因是 .
(1)、试剂为(填化学式);在过滤操作中要使用玻璃棒,其作用是 .(2)、证明滤液Ⅰ中无的实验方法是;用离子方程式解释滤液Ⅰ不含有可能的原因 .(3)、流程中固体不可暴露在空气中时间过长,原因是(用化学方程式表示).(4)、高铁酸钠中铁的化合价为价.高铁酸钠处理水过程中所发生的化学反应主要为(胶体) , 该反应中物质的氧化性强弱关系是(填“>”或“<”) . 净水时能吸附悬浮物的原因是 . -
3、“84”消毒液是生活中常见的消毒剂,可用与溶液在冷水浴中制备.(1)、Ⅰ.配制溶液:
配制溶液时,一般有以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其正确的操作顺序为(填标号).
A.①②④⑤⑦⑥③ B.②①③⑤⑥⑦④ C.②①⑥③⑤④⑦ D.①②⑥③⑦⑤④
实验中必须用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、 .
(2)、下列操作使所配溶液浓度偏低的是____(填标号).A、在天平两边放相同大小的滤纸后,再进行称量 B、未冷却至室温就将溶液转移到容量瓶中 C、定容时俯视刻度线 D、未洗涤溶解固体的烧杯 E、固体在称量前已部分变质(3)、Ⅱ.“84”消毒液的制备(装置如图所示):
已知是实验室制取氯气的装置,中广口瓶内为溶液,中试剂为 , 中发生反应的化学方程式为 , 的作用为 .
(4)、某同学设计实验探究84消毒液的漂白性.a.在消毒液中加入水后,放入红色纸片,观察到纸片慢慢褪色.
b.在消毒液中加入白醋后,放入红色纸片,观察到纸片迅速褪色.
c.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示.
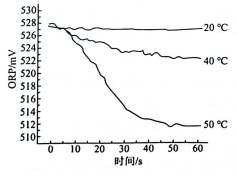
已知ORP表示水溶液中物质的氧化性或还原性强弱.ORP值越大,氧化性越强.
①实验a、b现象不同的原因是 .
②实验c中,随时间的变化ORP值不同的原因可能是 .
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度.已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,则需加水的质量为g.
-
4、下表是元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题.
族
周期
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
二
①
②
③
④
⑤
三
⑥
⑦
⑧
⑨
(1)、④、⑧、⑨三种元素的常见简单离子的半径由小到大的顺序为(用离子符号表示).(2)、④、⑦、⑨三种元素形成的化合物中含有的化学键类型为 .(3)、写出⑧的单质与⑥的最高价氧化物对应的水化物反应的离子方程式 .(4)、写出②元素和④元素形成的化合物的电子式 .(5)、②、③、④三种元素的简单氢化物中最稳定的是(填化学式).(6)、用电子式表示⑥与⑨形成的化合物的形成过程;该化合物属于(填“共价”或“离子”)化合物.(7)、镓是31号元素,镓的化合物氮化镓和砷化镓作为第三代半导体材料,具有耐高温、耐高电压等特性,随着技术的发展,它们的商用价值进入“快车道”.下列有关说法正确的是(填标号).a.位于元素周期表第四周期ⅣA族
b.为门捷列夫预言的“类铝”
c.的最高价氧化物对应水化物的碱性比⑧元素最高价氧化物对应水化物的碱性强
d.元素在第四周期第ⅤA族,则酸性: ,
-
5、(1)、Ⅰ.现有以下几种物质:
① ②氢氧化钠固体 ③ ④ ⑤盐酸 ⑥酒精 ⑦熔融硝酸钾 ⑧液氯
其中属于电解质的是(填序号),能导电的是(填序号).(2)、写出④在熔融状态下的电离方程式 .(3)、Ⅱ. 亚硝酸钠被称为工业盐,有毒,但在肉类制品加工中又可以加入极少量用作发色剂、防微生物剂、防腐剂,在漂白、电镀和金属处理等方面有应用.已知能发生反应:
配平上述化学方程式,并在方程式上面用“双线桥”经明电子转移的方向和数目 .
(4)、该反应中表现的性质是;氧化剂与还原剂的物质的量之比为;当反应转移电子时,则在标准状况下生成NO的体积为L.(5)、误食会导致血红蛋白中的转化为而中毒,可服用维生素解毒,维生素C在解毒过程中作剂. -
6、某无色溶液仅由中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
①加过量盐酸无明显现象,且阴离子种类不改变;进行焰色试验显黄色,透过蓝色钴玻璃观察,未见紫色;②取操作①后的溶液,加入过量溶液,产生白色沉淀.
下列推断错误的是( )
A、原溶液中一定存在 B、②中的白色沉淀只有 C、溶液中一定不含 D、由溶液呈电中性可知溶液中一定含有 -
7、下列选项所示的物质间转化能一步实现的是( )A、 B、 C、 D、
-
8、下列“实验结论”与“实验操作及现象”不相符的一组是( )
实验操作及现象
实验结论
A
某溶液中先加入溶液有白色沉淀产生,再加盐酸,
沉淀不消失
该溶液不一定有
B
向饱和 , 溶液中加入足量氯水,有无色气体产生
氯水中含
C
向饱和 , 溶液中通入足量 , 有白色固体析出
溶解度:
D
把绿豆大的和K分别投入水中,K与水反应更剧烈
金属性:
A、A B、B C、C D、D -
9、歌曲《青花瓷》唱道“䆖外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是(碱式碳酸铜).铜在潮湿的空气中生锈的化学反应为 . 下列有关该反应的说法错误的是( )A、碱式碳酸铜既是氧化产物,又是还原产物 B、该反应属于氧化还原反应,化合价发生改变的只有两种元素 C、该反应中铜失电子,氧气得电子 D、若有铜单质参与反应,则转移电子的物质的量为
-
10、已知① ② , ③ , 请依据上述反应判断还原性由强到弱的顺序是( )A、 B、 C、 D、
-
11、设为阿伏加德罗常数的值,下列说法正确的是( )A、含的浓盐酸与足量反应生成的分子数目为 B、与过量铁反应,转移的电子数为 C、溶液中含有的原子数目为 D、标准状况下,含共用电子对数为
-
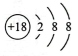
12、下列有关化学用语的说法正确的是( )A、质子数为53、中子数为78的碘原子: B、互为同位素 C、次氯酸的结构式为 D、的结构示意图:
-
13、下列实验装置能达到实验目的的是( )

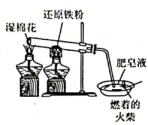

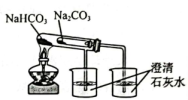
A.制备胶体
B.验证铁与水蒸气反应能生成
C.转移溶液
D.比较D.比较
A、A B、B C、C D、D -
14、下列离子方程式书写正确的是( )A、小苏打治疗胃酸过多: B、用醋酸除去水垢: C、将钠加入硫酸铜溶液中: D、将覆铜板放到溶液中制作图案:
-
15、下列有关物质的分类正确的是( )A、均属于酸性氧化物 B、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 C、四种物质均属于化合物 D、生铁、不铭钢、有色玻璃、碘水都属于混合物
-
16、关于等物质的量的和 , 则下列说法不正确的是( )A、氧原子数目比为 B、摩尔质量之比为 C、同温同压下,密度之比为 D、常温常压下,所占体积比为
-
17、下列药品的保存措施不正确的是( )A、漂白粉保存在敞口容器中 B、浓盐酸密封保存在试剂瓶中 C、金属钾保存在煤油中 D、硫酸亚铁溶液加铁粉保存
-
18、下列各组离子在无色透明的酸性溶液中能大量共存的是( )A、 B、 C、 D、
-
19、化学让生活更美好,下列说法错误的是( )A、碳酸钠可以用于纺织、造纸、制皂、制玻璃等工业 B、漂白液、漂白粉和漂粉精可作漂白棉、麻、纸张的漂白剂 C、因为硬铝熔点比纯铝低,所以硬铝是制造飞机的理想材料 D、茂密树林中的道道光柱,既是一种自然现象又是光学现象,也与胶体知识有关
-
20、我国向世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和。而研发二氧化碳捕捉和碳利用技术则是关键,其中催化加氢合成甲酸反应为:是一种很有前景的方法,且生成的甲酸是重要化工原料。回答下列问题:(1)、已知:298K时,部分物质的相对能量如表所示。
物质
相对能量/()
-393
0
-423.9
则=。反应中应控制合适的投料比,随与的投料比增大,的转化率将。
(2)、催化加氢合成甲酸的过程中,不断升高温度,下列图像正确的是(填标号)。A
B
C
D



 (3)、恒容密闭容器中充入一定量的和合成 , 下列能说明该反应达到平衡状态的是____(填标号)。A、(浓度熵)不再变化 B、和的物质的量相等 C、气体的密度不再变化 D、的质量分数不再改变(4)、在某催化剂的作用下,和反应生成 , 同时发生副反应:
(3)、恒容密闭容器中充入一定量的和合成 , 下列能说明该反应达到平衡状态的是____(填标号)。A、(浓度熵)不再变化 B、和的物质的量相等 C、气体的密度不再变化 D、的质量分数不再改变(4)、在某催化剂的作用下,和反应生成 , 同时发生副反应:。维持容器容积1L不变,按照固定投料比将和按一定流速通过该催化剂,平衡时,测得如下数据:
温度(K)
转化率(%)
甲酸选择性(%)
323
40.0
50.0
343
54.6
48.3
注:甲酸的选择性是指发生反应的中转化为甲酸的百分比。
①数据表明,升高温度,转化率提高而甲酸选择性降低,其原因是;
②323K下,与各按1mol投料,平衡时,的物质的量为 , 主反应的平衡常数=。