相关试卷
-
1、氨是无碳的能源载体和潜在的储氢燃料,广泛应用于化肥、塑料和炸药的生产。回答下列问题:(1)、已知: , 。
在下列温度下,该反应可能自发进行的是____(填字母)。
A、 B、 C、 D、(2)、反应历程中各步势能变化如下图所示,其中吸附在催化剂表面的物种用“ad”表示。
产物从催化剂上脱附(填“释放”或“吸收”)能量;该反应历程中有个基元反应,决速步骤的反应可以表示为。
(3)、在容积为的恒容密闭容器内充入和 , 加入合适催化剂(体积可以忽略不计),在不同催化剂作用下,相同时间内的转化率随温度的变化如下图所示:
在催化剂Ⅱ作用下的转化率随温度升高先增大后减小的原因可能是(不考虑温度对催化剂活性的影响);c点(填“大于”或“小于”)b点 , 简述其原因:。
(4)、在某催化剂作用下,合成氮的反应速率为(k为速率常数,只与温度、催化剂有关,与浓度无关。为反应级数,可取正数、负数、0,也可取分数),为了测定反应级数,下进行实验,结果如表所示:序号
反应速率
I
0.1
0.1
0.1
v
II
0.2
0.1
0.1
III
0.2
0.4
0.1
IV
0.1
0.9
0.3
则。
(5)、利用催化剂通过电化学反应在室温下合成氨的原理如下图所示,该装置中阴极的电极反应式为。
-
2、“天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙奥秘离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。元素铼()的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含)中提取铼,其工艺流程如图所示:

回答下列问题:
(1)、矿样粒度与浸出率关系如下图所示,则“浸出”时应将富铼渣粉碎至____目(填字母)。 A、60 B、80 C、100 D、120(2)、已知“浸出”时反应中转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:。(3)、实验室中,操作Ⅲ所用装置应选用____(填字母)。A、
A、60 B、80 C、100 D、120(2)、已知“浸出”时反应中转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:。(3)、实验室中,操作Ⅲ所用装置应选用____(填字母)。A、 B、
B、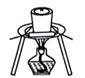 C、
C、 D、
D、 (4)、“一系列操作”包括①(填操作名称,下同)、冷却结晶、过滤、洗涤和②;从下列仪器中选出①②中需使用的仪器,依次为(填字母)。
(4)、“一系列操作”包括①(填操作名称,下同)、冷却结晶、过滤、洗涤和②;从下列仪器中选出①②中需使用的仪器,依次为(填字母)。A.
 B.
B. C.
C. D.
D. (5)、已知高铼酸铵是白色片状晶体,微溶于冷水,易溶于热水,欲得纯度更高的高铼酸铵晶体,可通过法提纯;“热还原”反应中氧化剂与还原剂的物质的量之比为。(6)、晶胞结构如下图所示,其中氧原子配位数为 , 铼原子填在了氧原子围成的(填“四面体”“立方体”或“八面体”)空隙中。
(5)、已知高铼酸铵是白色片状晶体,微溶于冷水,易溶于热水,欲得纯度更高的高铼酸铵晶体,可通过法提纯;“热还原”反应中氧化剂与还原剂的物质的量之比为。(6)、晶胞结构如下图所示,其中氧原子配位数为 , 铼原子填在了氧原子围成的(填“四面体”“立方体”或“八面体”)空隙中。
-
3、四氮化四硫( , S为价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于等有机溶剂,可用与(红棕色液体)反应制备,反应装置如图所示(夹持装置已省略)。
已知:

回答下列问题:
(1)、氨气发生装置可以选用(填字母)。a.
 b.
b.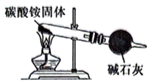 c.
c.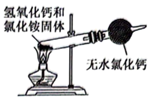 d.
d. (2)、装置B中生成的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为;证明反应完全的现象是。(3)、装置C的作用是 , 其中的作用是。(4)、测定产品纯度:
(2)、装置B中生成的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为;证明反应完全的现象是。(3)、装置C的作用是 , 其中的作用是。(4)、测定产品纯度:i.蒸氨:取固体样品加入三颈烧瓶中,再加入足量溶液并加热,将蒸出的通入含有标准溶液的锥形瓶中。
ii.滴定:用的溶液滴定剩余的 , 记录消溶液的体积。重复实验3次,数据如下表所示:
实验序号
初始读数()
最终读数()
①
0.20
20.22
②
0.40
24.85
③
1.00
20.98
用标准溶液滴定硫酸溶液之前,需要润洗滴定管,润洗滴定管的操作为 , 滴定时选用的指示剂为 , 制得的的纯度为(保留两位有效数字)。
-
4、已知和都是难溶的铅盐。时,分别向和溶液中滴加的溶液,滴加过程中[ , M为或]与溶液体积(V)的变化关系如图所示(假设溶液总体积等于各溶液体积之和)。下列说法正确的是( )
 A、曲线表示 B、若将溶液的浓度换成 , 则N点将迁移至X点 C、反应可以转化完全(时转化完全) D、向含有和的混合溶液中滴加溶液,先生成沉淀
A、曲线表示 B、若将溶液的浓度换成 , 则N点将迁移至X点 C、反应可以转化完全(时转化完全) D、向含有和的混合溶液中滴加溶液,先生成沉淀 -
5、如图所示电解装置中,通电后石墨电极Ⅱ上有生成,逐渐溶解,下列判断错误的是( )
 A、a极电势低于b极电势 B、交换膜c为质子交换膜 C、随着电解的进行,溶液浓度变小 D、当完全溶解时,外电路中通过电子
A、a极电势低于b极电势 B、交换膜c为质子交换膜 C、随着电解的进行,溶液浓度变小 D、当完全溶解时,外电路中通过电子 -
6、我国科学家合成了富集的非碳导热材料立方氮化硼晶体,晶胞参数为 , 晶胞结构如图所示,下列说法正确的是( )
 A、和互为同素异形体 B、该晶体的化学式为 C、该晶胞中含有配位键,提供空轨道的原子是B原子 D、该晶体中N原子和B原子的最近距离为
A、和互为同素异形体 B、该晶体的化学式为 C、该晶胞中含有配位键,提供空轨道的原子是B原子 D、该晶体中N原子和B原子的最近距离为 -
7、将与、溶液混合,发生反应:。已知混合溶液中的初始浓度相同,不同温度下,达到平衡时的脱除率与的初始浓度的关系如图所示。下列说法错误的是( )
 A、 B、反应中为氧化剂 C、的键角小于的键角 D、a点小于b点
A、 B、反应中为氧化剂 C、的键角小于的键角 D、a点小于b点 -
8、根据下列实验操作、现象得出的结论正确的是( )
选项
实验操作
现象
结论
A
向鸡蛋清溶液中滴加饱和(NH4)2SO4溶液
溶液变浑浊,再加水浑浊消失
说明蛋白质发生了盐析
B
向酸性高锰酸钾溶液中加入甲苯,振荡
溶液紫色褪去
甲苯同系物均有此性质
C
在坩埚中加入 , 加热一段时间,在干燥器中冷却,称量剩余固体质量
质量为
加热后坩埚内固体为和混合物
D
在试管中加入溶液,再加5滴稀溶液,混匀后加入乙醛,加热
没有砖红色沉淀生成
乙醛没有还原性
A、A B、B C、C D、D -
9、短周期主族元素R、X、Y、M原子序数依次增大,Y为地壳中含量最高的元素,M与Y元素不同周期且M原子的核外未成对电子数为1,由R、X、Y、M组成的物质结构式如图所示。下列说法错误的是( )
 A、分子的模型为四面体形 B、简单氢化物的稳定性: C、该化合物中X原子最外层均满足结构 D、图示结构式中X原子的杂化方式有两种
A、分子的模型为四面体形 B、简单氢化物的稳定性: C、该化合物中X原子最外层均满足结构 D、图示结构式中X原子的杂化方式有两种 -
10、脱落酸(X)是一种抑制生长的植物激素,常用于植物组织分化、培养实验,其结构简式如图所示,下列关于X的说法错误的是( )
 A、X中含氧官能团有三种 B、每个X分子中含有1个手性碳原子 C、X分子中所有原子不可能共平面 D、最多消耗
A、X中含氧官能团有三种 B、每个X分子中含有1个手性碳原子 C、X分子中所有原子不可能共平面 D、最多消耗 -
11、对于下列实验,能正确描述其反应的离子方程式是( )A、金属与溶液反应: B、将粉末浸没在足量的蓝矾溶液中: C、向溶液中通入: D、(弱酸)与酸性溶液反应:
-
12、一种工业制备无水氯化镁的工艺流程如下:

下列说法错误的是( )
A、“沉镁”时可能发生反应: B、在实验室中“煅烧”时使用的仪器为坩埚,同时需要用玻璃棒不断搅拌 C、“氯化”过程中发生的反应为气体分子数增加的反应 D、不可以通过直接灼烧晶体的方法得到无水固体 -
13、下列各组物质分离提纯方法及依据均正确的是( )
选项
分离提纯方法
依据
A
过滤法除去溴苯中混有的苯
溶解度不同
B
加热法除去固体中的
热稳定性不同
C
饱和食盐水洗气法除去中的
物质溶解性不同
D
加热法除去中的
热稳定性不同
A、A B、B C、C D、D -
14、用代表阿伏加德罗常数的值,下列说法正确的是( )A、的甲酸溶液中氢离子数目为 B、乙烷中含有杂化的原子数目为 C、分子中含极性键数目一定是 D、标准状况下,中键的数目为
-
15、实验是化学探究的一种重要途径。下列有关实验的描述正确的是( )A、用干燥的红色石蕊试纸检验 B、在中和热测定的实验中,做三次平行实验最少要使用6次温度计 C、进行焰色试验时,可用玻璃棒替代铂丝 D、称取固体配制溶液
-
16、化学用语可以表示反应过程,下列化学用语的表达错误的是( )A、硫化钠溶液和稀硝酸混合: B、常温下,溶液的 , 是因为溶液中存在平衡: C、用电子式表示的形成过程:
 D、溶液可使紫色石蕊试液变红的原因:
D、溶液可使紫色石蕊试液变红的原因:
-
17、宏观辨识与微观探析是化学学科核心素养之一,下列说法正确的是( )A、乙醚的分子式: B、乙炔的结构简式: C、中子数为8的碳原子: D、丙烷的键线式:

-
18、化学与生产、生活、科技等密切相关。下列说法错误的是( )A、潜水器“奋斗者”号使用的碳纤维材料是有机高分子材料 B、古壁画使用铁红作红色颜料,是由于其在空气中性质稳定 C、海洋开发走向“深蓝时代”,大型舰船的底部常镶嵌锌块,以防止船体腐蚀 D、“天问一号”火星车的热控保温材料——纳米气凝胶,可产生丁达尔效应
-
19、某研究小组按下列路线合成药物库潘尼西(K).

已知:

回答下列问题:
(1)、化合物A的官能团名称是.(2)、下列说法不正确的是____.A、B→C的反应只涉及加成反应、消去反应两步反应 B、在D→E的反应中的与作用与流程中的相同 C、K可在酸性或碱性条件下发生水解反应 D、流程中所涉及的有机物中有五种可与发生显色反应(3)、化合物D的结构简式是.(4)、写出的化学方程式.(5)、以、 为原料合成有机物F.设计该合成路线(用流程图表示,无机试剂任选). (6)、写出同时符合下列条件的化合物C的同分异构体的结构简式.
为原料合成有机物F.设计该合成路线(用流程图表示,无机试剂任选). (6)、写出同时符合下列条件的化合物C的同分异构体的结构简式.①分子中除含有苯环不含其他环;
②谱和谱检测表明:分子中共有4种不同化学环境的氢原子,有
 、 , 无羟基、氮氧键.
、 , 无羟基、氮氧键. -
20、某学习小组利用相对密度法测定分子量,实验装置如图:

简要步骤如下:
步骤Ⅰ:利用上图装置获取纯净;
步骤Ⅱ:取一只洁净而干燥的锥形瓶(E),用合适的橡胶塞塞紧后在塞子上作上标记,用电子天平称量,质量:.用E收集.
集满后,在电子天平上称量,质量(+瓶+塞子):.
步骤Ⅲ:分子量的测定
依据阿伏加德罗定律的推论: ,
可得:
请回答下列问题:
(1)、写出装置A反应的离子方程式:.(2)、的纯净程度是保证实验结果准确的关键.B、C、D装置是的净化装置,请按顺序选择最适当的试剂:.a.水 b.浓硫酸 c.无水氯化钙及玻璃纤维
d.饱和碳酸氢钠溶液 e.碱石灰及玻璃纤维
(3)、E没有设置防对流,能否收集到纯净 , 说明理由:.(4)、下列说法正确的是____.A、当装置B、C中有气泡时,即可以开始收集 B、即是锥形瓶的质量 C、对E进行称量时,应缓缓取出导管,再塞上橡胶塞至标记处,称量 D、通过对E反复称量,对比质量的变化,即可判断是否集满(5)、通过向锥形瓶装水至橡胶塞塞至的标记处,用托盘天平称量,质量(水+瓶+塞子): , 此时,水的质量远大于空气,可测定锥形瓶的体积:mL.若体积折算成标准状况,则(用、、的计算式表示,无需化简)。