相关试卷
-
1、已知:① ΔH1=-2878kJ·mol-1;
② ΔH2=-2869kJ·mol-1。
下列说法错误的是
A、CH3CH2CH2CH3与CH(CH3)3互为同分异构体 B、稳定性:CH3CH2CH2CH3>CH(CH3)3 C、CH3CH2CH2CH3(g)= CH(CH3)3(g) ΔH=-9kJ·mol-1 D、反应①、②可分别表示CH3CH2CH2CH3、CH(CH3)3的燃烧热的热化学方程式 -
2、用Na2CO3与醋酸(CH3COOH)反应可制取CO2。下列有关说法错误的是A、电离方程式:H2CO32H++CO B、该反应的离子方程式:CO+2CH3COOH=2CH3COO-+H2O+CO2↑ C、常温下,电离常数:K(CH3COOH)>Ka1(H2CO3) D、向醋酸溶液中加水,醋酸电离程度增大
-
3、已知W→Z的能量变化与反应进程的关系如图所示:

下列关于三个反应进程的说法错误的是
A、生成Z的速率:Ⅲ>Ⅱ>Ⅰ B、平衡时W的转化率:Ⅰ=Ⅱ=Ⅲ C、ΔH(Ⅰ)=ΔH(Ⅱ)=ΔH(Ⅲ) D、X、Y分别参与了进程Ⅱ、Ⅲ的反应 -
4、N2O5在一定温度下可发生反应: ΔH>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
时间/s
0
500
1000
1500
c(N2O5)/(mol·L-1)
5.00
3.52
2.50
2.50
下列说法错误的是
A、500s内NO2的平均生成速率为5.92×10-3mol·L-1·s-1 B、T1温度下发生该反应,N2O5的平衡转化率为50% C、T1、T2温度下的平衡常数分别为K1、K2 , 若T1>T2 , 则K1>K2 D、平衡后,其他条件不变,将容器体积变为原来2倍,则c(N2O5)=1.25mol·L-1 -
5、下列说法中正确的是A、反应 在任何温度下都不能自发进行 B、知道了某过程有自发性之后,就能确定该过程一定会发生 C、一定温度下,反应的ΔH>0 ΔS>0 D、在低温条件下能自发进行的反应在高温条件下也一定能自发进行
-
6、工业制氢原理:。改变下列条件能提高产生氢气的速率且提高活化分子百分率的是A、将炭块改为炭粉 B、加入高效催化剂 C、降低反应温度 D、增大水蒸气浓度
-
7、速率控制在生产生活中较为常见。下列操作或措施与速率控制无关的是A、煅烧硫铁矿时将其粉碎 B、合成氨时采用高温条件 C、食品抽真空包装 D、净水时加入明矾
-
8、下列应用涉及的反应属于吸热反应的是A、煤油与液氧作为火箭推进剂 B、Al和Fe2O3反应焊接钢轨 C、灼热的炭与CO2反应制CO D、乙炔与氧气反应用于切割金属
-
9、已知298K,101kPa时,。该反应在密闭的刚性容器中分别于T1、T2温度下进行,CO2的初始浓度为 , 关系如图所示。下列说法错误的是
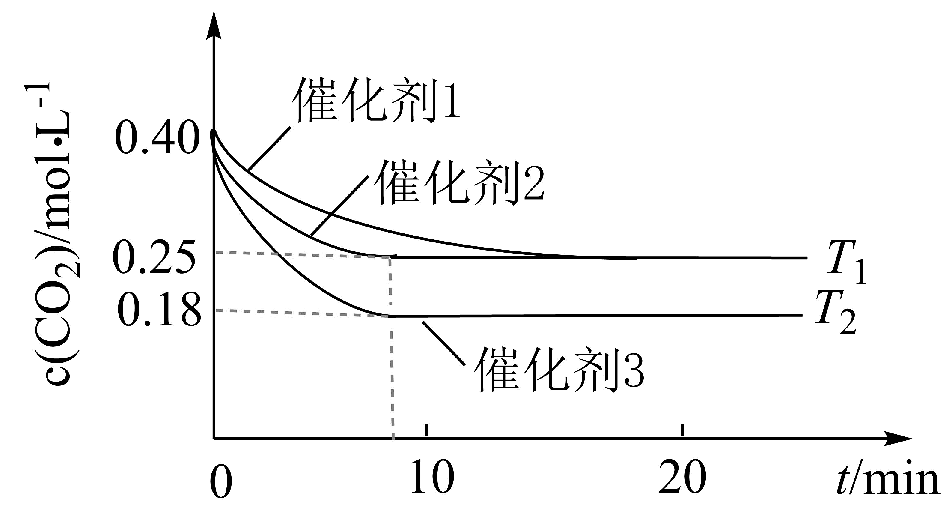 A、T1>T2 B、T1下反应达到平衡时 C、使用催化剂1的反应活化能比催化剂2的大 D、使用催化剂2和催化剂3的反应历程相同
A、T1>T2 B、T1下反应达到平衡时 C、使用催化剂1的反应活化能比催化剂2的大 D、使用催化剂2和催化剂3的反应历程相同 -
10、某同学进行如下实验:
实验
操作和现象
Ⅰ
向溴水中滴加少量CCl4 , 振荡,CCl4层显橙色
Ⅱ
向碘水中滴加少量CCl4 , 振荡,CCl4层显紫色
Ⅲ
向KBr、KI的混合液中加入CCl4。滴加氯水,振荡后CCl4层显紫色;再滴加氯水,振荡后紫色褪去;继续滴加氯水,振荡后CCl4层变为橙色
下列分析不正确的是
A、Ⅰ中CCl4层显橙色,说明CCl4层含Br2 B、Ⅱ中的现象说明I2在CCl4中的溶解性大于在水中的溶解性 C、Ⅲ中CCl4层显紫色,说明Cl2的氧化性强于I2 D、Ⅲ中CCl4层变为橙色时,水层中仍含有大量I- -
11、
水合肼(N2H4∙H2O)是一种用途广泛的化工原料,是具有较强还原性的碱性液体,在空气中会与CO2反应产生烟雾。制备N2H4∙H2O的实验流程如下图所示:

回答下列问题:
I.步骤I制备NaClO的装置如图1所示。

已知:①是放热反应;
②。
(1)装置B发生反应的离子方程式为: , 装置D中盛装的试剂是。
(2)为了提高NaClO的产率,防止副反应发生,装置需要采用冰水浴,实验中除控制温度外还需采取的措施是。
Ⅱ.由步骤Ⅱ和步骤Ⅲ获得N2H4∙H2O的装置如图2所示,利用NaClO与含尿素的NaOH溶液在三颈烧瓶中合成N2H4∙H2O,再通过减压蒸馏在锥形瓶H中收集。

(3)干燥管e中盛装的试剂为 , 实验中通过仪器c缓慢滴加的溶液是(填“尿素溶液”或“NaClO溶液”),原因是。
(4)三颈烧瓶中合成N2H4∙H2O的化学方程式是。
(5)产品水合肼含量的测定:称取样品液体0.1500g,加入适量NaHCO3固体,配成溶液,滴入几滴淀粉溶液,用0.1000mol∙L-1的标准I2溶液滴定。实验测得消耗标准I2溶液的体积为36.00mL,则样品中N2H4∙H2O的质量分数为(已知:)。
-
12、合成氨反应是人工固氮的重要形式,该反应的热化学方程式为 。设为阿伏加德罗常数的值,下列说法不正确的是A、每放出的热量,生成的分子数目为 B、与足量充分反应后转移的电子数目为 C、25℃时,的氨水中所含的数目为 D、完全溶于足量稀盐酸后所得的数目少于
-
13、下列离子方程式与所给事实不相符合的是A、制备84消毒液(主要成分是NaClO): B、食醋去除水垢中的: C、0.1mol/L醋酸溶液pH>1: D、向中逐滴加入溶液使恰好沉淀完全:
-
14、氨气()是一种极易溶于水的气体,实验中常用固体氢氧化钙与氯化铵混合加热的方法制备,请回答下列问题:
 (1)、实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气化学方程式是 , 应选用上图中的装置(填序号)。(2)、下列试剂不能用于干燥的是(填字母)。
(1)、实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气化学方程式是 , 应选用上图中的装置(填序号)。(2)、下列试剂不能用于干燥的是(填字母)。A.碱石灰 B.浓硫酸 C.NaOH固体
(3)、已知氨气难溶于 , 下列装置可用于实验室吸收多余氨气并能防倒吸的是(填字母)(4)、氨气进到氯化氢时,会迅速反应生成氯化铵晶体,该反应的化学方程式为。 (5)、如图所示,是铁的价态二维图,反应③的主要现象为。
(5)、如图所示,是铁的价态二维图,反应③的主要现象为。 (6)、钛和钛合金是21世纪的重要的金属材料。工业上冶炼金属钛的原理是:在氩气环境和高温条件下,利用金属镁和 , 反应生成氯化镁和金属钛,该反应的方程式为。
(6)、钛和钛合金是21世纪的重要的金属材料。工业上冶炼金属钛的原理是:在氩气环境和高温条件下,利用金属镁和 , 反应生成氯化镁和金属钛,该反应的方程式为。 -
15、有机物种类繁多,可利用结构决定性质的原理,加速对有机物性质的理解和记忆。(1)、乙基芳樟醇(A)可用于各种花香型日化香精,其结构简式如图所示。

①写出A含氧官能团的电子式:。
②A可能具有的化学性质有(填标号)。
A.能使溴水褪色 B.能与金属钠反应
C.不能发生反应生成高聚物 D.在铜催化下加热能被氧气氧化生成醛
(2)、以月桂烯为原料制取乙酸香叶酯的流程如图:
①B中官能团的名称为。
②乙酸香叶酯的化学式为。
③反应Ⅰ的反应类型是。
④反应Ⅱ的化学方程式是。
(3)、已知乙烯与异丁烯[CH2=C(CH3)2]互为同系物,写出异丁烯在一定条件下生成聚异丁烯的化学方程式:。 -
16、研究化学反应中的能量变化对生产生活有着重要意义。某兴趣小组进行下列探究:(1)、甲同学探究反应(稀)中的能量变化。向装有铁片的试管中加入的 , 观察到试管内有气泡产生,触摸试管外壁,温度升高。结论:。(2)、乙同学设计如图所示原电池实验装置。
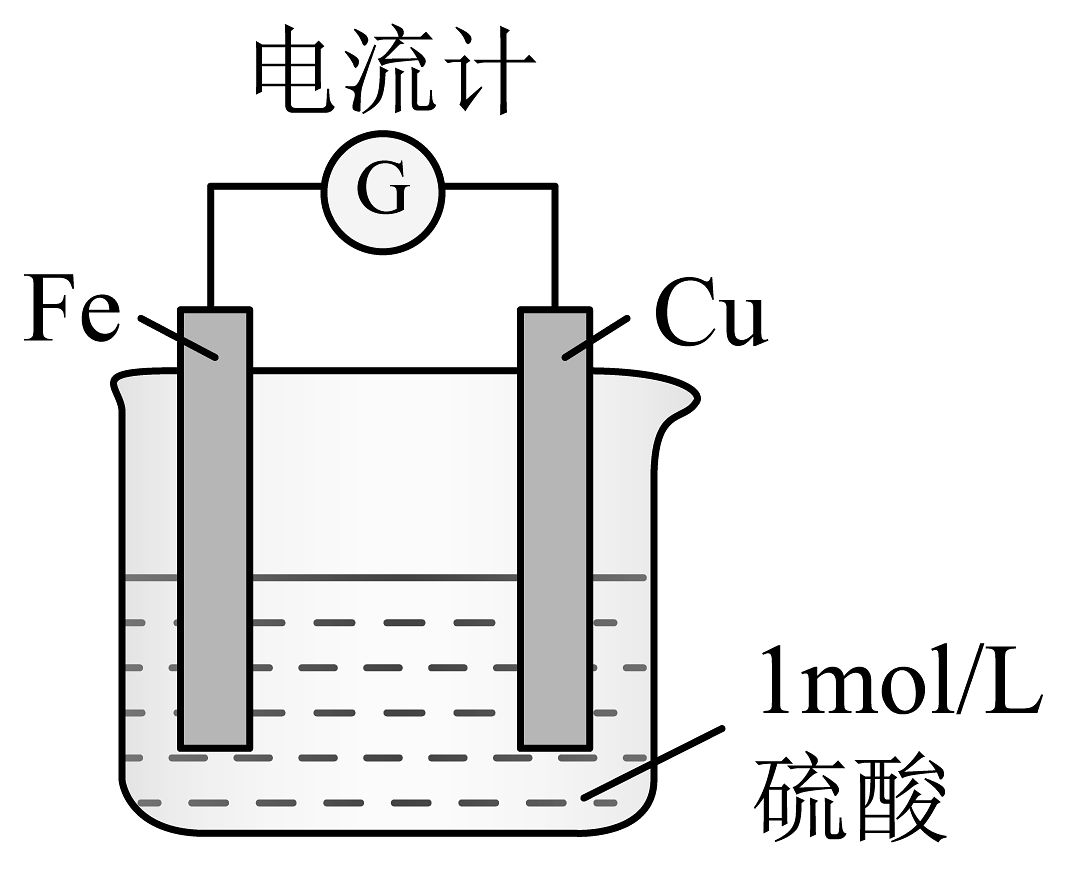
外电路中电子由极流向极(填“正”或“负”);铁片上的电极反应式为。
(3)、下列反应能通过原电池实现化学能直接转化为电能的是(填序号)。① ② ③
(4)、用和组合形成的质子交换膜燃料电池的结构如下图:
①移向(填“正极”或“负极”)。
②气体b为 , 若线路中转移电子,则该燃料电池理论上消耗的在标准状况下的体积为L。
-
17、
Ⅰ、以甲烷为原料合成聚苯乙烯等产品的一种流程如下(部分产物及反应条件略去)

(1)反应④的反应类型为________,化学方程式为________。
(2)写出符合下列条件的乙苯的同分异构体的结构简式,属于芳香烃且分子中不同化学环境的氢原子数比为6:2:1:1________。
Ⅱ、乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题:

(3)可以鉴别乙烷和乙烯的试剂是________ (填写一种试剂即可)。
(4)下列物质中,可以通过乙烯发生加成反应得到的是_______ (填字母序号)。
A. CH3CH3 B. CH3CHCl2 C. CH3CH2OH D. CH3CH2Br Ⅲ、某课外小组设计实验室制取乙酸乙酯的装置如下:
(5)试管II中装有 ________溶液。
(6)写出乙酸和乙醇反应制取乙酸乙酯的方程式________。
-
18、甜橙醇的结构如下。下列有关甜橙醇的叙述不正确的是
 A、分子式为 B、该分子中所有原子可能共面 C、能发生氧化反应、加成反应、取代反应 D、1mol甜橙醇在一定条件下最多可以和2mol氢气发生反应
A、分子式为 B、该分子中所有原子可能共面 C、能发生氧化反应、加成反应、取代反应 D、1mol甜橙醇在一定条件下最多可以和2mol氢气发生反应 -
19、为阿伏加德罗常数的值。下列说法正确的是A、标准状况下,和的混合气体含有的质子数为 B、12g熔融中含有的阳离子数为 C、与足量反应,转移的电子数为 D、标准状况下,含有的氧原子数为
-
20、短周期主族元素X、Y、Z、M、N的原子序数依次增大。X的最外层电子数为内层电子数的2倍,Z是地壳中含量最高的元素,M的原子半径在短周期主族元素中最大,N的最外层电子数等于最内层电子数。下列说法错误的是A、金属性: B、简单氢化物的热稳定性: C、简单离子半径: D、最高价氧化物对应水化物的酸性: