相关试卷
-
1、硼及其化合物在材料制造、有机合成等方面应用广泛。图(a)为一种无限长单链状结构的多硼酸根,图(b)硼氢化钠晶胞结构。下列说法正确的是
 A、图a中多硼酸根的化学式为 [BO3] B、硼氢化钠晶体中BH周围紧邻且等距的Na+数为4 C、图(a)中O-B-O的键角大于BH中的H-B-H的键角 D、硼氢化钠晶体属于混合晶体,有较强的还原性
A、图a中多硼酸根的化学式为 [BO3] B、硼氢化钠晶体中BH周围紧邻且等距的Na+数为4 C、图(a)中O-B-O的键角大于BH中的H-B-H的键角 D、硼氢化钠晶体属于混合晶体,有较强的还原性 -
2、工业通过高温煅烧焦炭与SrSO4(硫酸锶)混合物,并通入一定量的空气,采用反应一或反应二制备SrS(s):
反应一:SrSO4(s) + 2C(s) 2CO2(g) + SrS(s) ΔH1
反应二:SrSO4(s) + 4CO(g) 4CO2(g) + SrS(s) ΔH2 = -118.8kJ·mol−1
已知:CO2(g) + C(s) = 2CO(g) ΔH3 = +172.5kJ·mol−1
C(s) + O2(g) = CO2(g) ΔH4 = -393.5kJ·mol−1
随温度升高,反应产物种类、物质的量的变化如图所示:
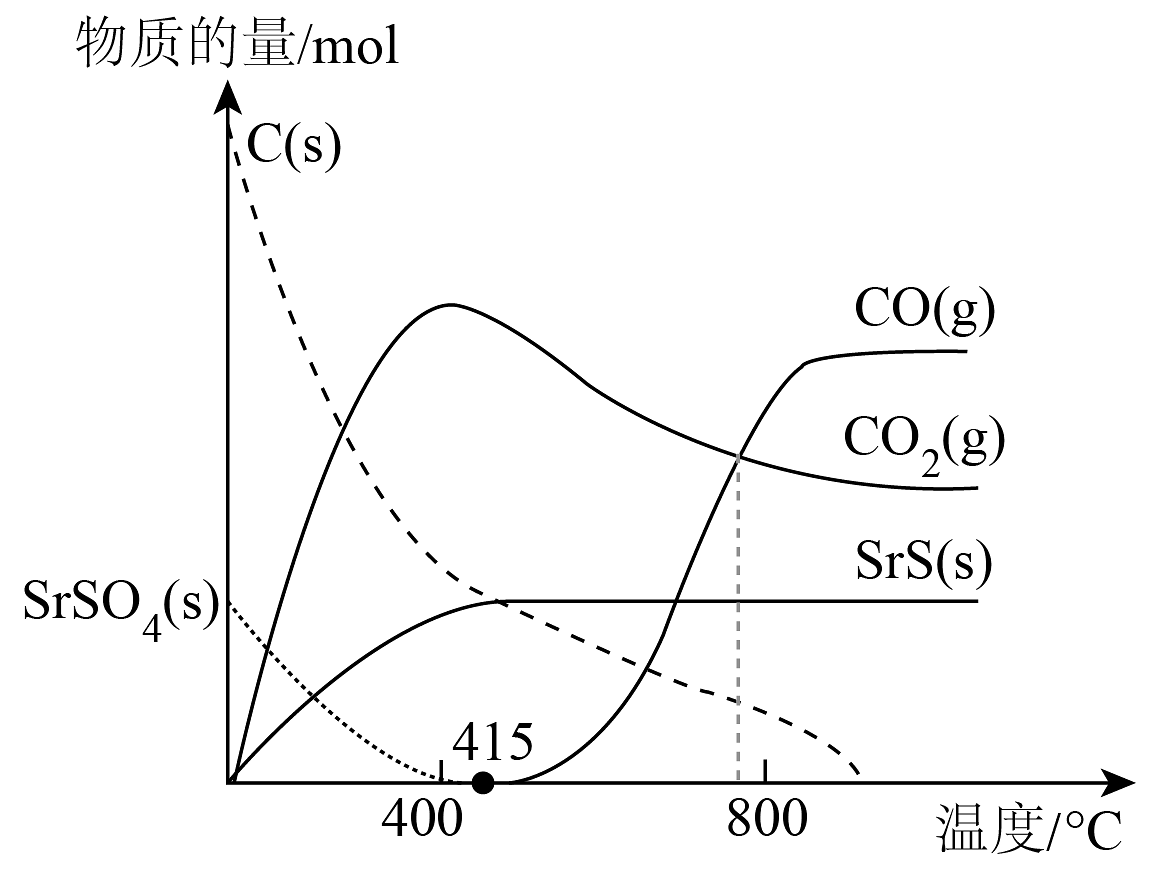
下列说法正确的是
A、ΔH1 = -226.2kJ·mol−1 B、800℃时,反应二的平衡常数K<1 C、当温度高于415℃时,体系内的主反应变为SrSO4(s)+ 4C(s)= 4CO(g)+ SrS(s) D、通入空气的作用是只是利用CO和O2反应放出的热量为制备过程供能 -
3、有机物P是一种治疗心律失常的药物,其部分合成路线如图所示(部分反应条件已略去)。

下列说法中错误的是
A、M→N为取代反应 B、M与溴水反应最多消耗 C、P完全氢化后有4个手性碳 D、P不能使酸性高锰酸钾溶液褪色 -
4、下列离子方程式书写正确的是A、烧碱溶液吸收少量二氧化硫:SO2+OH-=HSO B、草酸(H2C2O4)与酸性KMnO4溶液反应:5C2O+2MnO+16H+=10CO2↑+2Mn2++8H2O C、向Mg(HCO3)2溶液中加入足量NaOH溶液:Mg2++2HCO+4OH-=Mg(OH)2↓+2CO+2H2O D、CO2通入足量的NaClO溶液中:CO2+2ClO-+H2O=2HClO+CO
-
5、关于反应2MnSO4+5Na2S2O8+8H2O=2NaMnO4+4Na2SO4+8H2SO4 , 下列说法正确的是A、MnSO4是氧化剂 B、Na2S2O8中S元素化合价为+7价 C、生成284 g NaMnO4时转移10 mol电子 D、Mn位于第四周期VIB族
-
6、结构决定性质,性质决定用途。下列结构或性质不能解释其用途的是A、植物油可通过催化加氢提高饱和度,可制取肥皂 B、乙醇极性较小,可将95%乙醇加入[Cu(NH3)4]SO4溶液中析出深蓝色晶体 C、维生素C具有强还原性,可做水果罐头中常用的抗氧化剂 D、石墨中C原子未杂化的p轨道重叠,电子在整个平面内运动,可制成导电材料
-
7、下列有关实验的说法中不正确的是A、对于含重金属离子的废液,可利用沉淀法进行处理 B、发生火情时,若火势不大,可用湿布或石棉布覆盖火源以灭火 C、实验室中未用完的白磷:放回原试剂瓶 D、如果不慎将苯酚沾到皮肤上,应立即用大量水冲洗,再用乙醇溶液冲洗
-
8、下列性质的比较正确的是A、酸性:硬脂酸>CH3COOH B、化合物中键的极性:NCl3>NF3 C、原子半径:Mg>Si>O D、第一电离能: Li<Na<K
-
9、下列描述原子结构的化学用语正确的是A、氨基的电子式:
 B、乙烯分子的结构简式为
C、基态铜原子的价层电子排布式:3d94s2
D、H2O的VSEPR模型:
B、乙烯分子的结构简式为
C、基态铜原子的价层电子排布式:3d94s2
D、H2O的VSEPR模型:
-
10、下列分子属于非极性分子的是A、CH2Cl2 B、CS2 C、NCl3 D、H2S
-
11、叶酸作为水溶性维生素B族中的一种,是人类不可缺少的营养素。在实验室可利用如下合成路线制备叶酸。

回答下列问题:
(1)、A→B的反应类型为;(2)、化合物G的名称为;化合物J中含氧官能团的名称为;(3)、D+H→I的化学方程式为;(4)、F的同分异构体中含-NH2 , 且直接与苯环相连的有种;其中核磁共振氢谱峰面积比为2:2:2:1的结构简式为;(5)、TAHP( )是一种碱性有机化合物,将下列化合物按碱性由强到弱排序:(填字母)(已知:孤电子对所占s轨道成分越少,越易给出电子,碱性越强)。
)是一种碱性有机化合物,将下列化合物按碱性由强到弱排序:(填字母)(已知:孤电子对所占s轨道成分越少,越易给出电子,碱性越强)。a.
 b.
b.  c. NH3(6)、结合上述合成路线,设计以乙醛为原料合成化合物M(
c. NH3(6)、结合上述合成路线,设计以乙醛为原料合成化合物M( )的合成路线(无机试剂任选),已知CH3CHO
)的合成路线(无机试剂任选),已知CH3CHO 。
。 -
12、采用热分解法去除沼气中的H2S过程中涉及的主要反应如下:
反应Ⅰ: ;
反应Ⅱ: 。
回答下列问题:
(1)、写出(g)吸收H2S(g)生成CS2(g)和H2(g)的热化学方程式:。(2)、保持100kPa不变,将与按体积比2∶1投入密闭容器中,发生反应Ⅰ、Ⅱ,并通入一定量的稀释,在不同温度下反应达到平衡时,所得、与的体积分数如图所示。
①1050℃时,下列能说明容器中反应达到平衡状态的有(填标号)。
A.容器的体积保持不变
B.容器内气体密度保持不变
C.v(CH4) = v(CS2)
D.S2和H2的物质的量之比为1∶2
②X所在曲线代表的是(填化学式)的体积分数。
③Y所在曲线随温度的升高先增大后减小的原因是。
④1000℃达到平衡时,H2S的体积分数为0.25%,则该温度下达到平衡后H2S的去除率为(保留三位有效数字,下同),反应Ⅰ压强平衡常数Kp=(用平衡分压代替平衡浓度计算,平衡分压=总压×体积分数)。
(3)、催化剂对反应有高选择性,理论计算得到反应主要路径如图所示,表示状态2的为(填选项)。
A.
 B.
B.  C.
C.
-
13、软锰矿的主要成分为MnO2 , 含少量Al2O3和SiO2.闪锌矿主要成分为ZnS,含少量FeS、CuS杂质。现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如下:

已知:Ⅰ.矿石中所有金属元素在滤液中均以离子形式存在。
Ⅱ.常温下各种金属离子开始沉淀和完全沉淀的如下表:
开始沉淀
完全沉淀
回答下列问题:
(1)、为了加快矿石的酸浸速率,通常采用的方法有。(2)、步骤①中发生多个反应,其中、与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出、与硫酸共热发生反应的离子方程式:。(3)、步骤②中Zn的作用是。(4)、步骤③中物质X用于调节溶液的 , X可选用的是。A. NaOH B. Ca(OH)2 C. ZnO D. Zn(OH)2
调节pH的范围是。
(5)、步骤④结合流程图分析用惰性电极进行电解时阳极的电极反应式为。(6)、锰的某种氧化物MnOx的四方晶胞及其在xy平面的投影如图所示,当MnOx晶体有O原子脱出时,出现O空位,Mn的化合价(填“升高”“降低”或“不变”)。 (7)、MnOx可作转化为的催化剂(见下图)。的熔点远大于 , 除相对分子质量存在差异外,另一重要原因是。
(7)、MnOx可作转化为的催化剂(见下图)。的熔点远大于 , 除相对分子质量存在差异外,另一重要原因是。
-
14、[Co(NH3)5Cl]Cl2 ()是一种易溶于热水,难溶于乙醇的紫红色晶体。可通过如下实验制备(实验装置如图)。

Ⅰ.将适量氯化铵溶于浓氨水中,搅拌下,将混合溶液缓慢滴加至1.00g研细的CoCl2·6H2O (M=238g·mol-1),得到[Co(NH3)6]Cl2沉淀。
Ⅱ.边搅拌边慢慢滴入足量30% H2O2溶液,得到[Co(NH3)5 H2O]Cl3溶液。
Ⅲ.慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤。
Ⅳ.依次用不同试剂洗涤晶体,烘干,得到0.80g产品。
已知:a. Co(OH)2 是不溶于水的沉淀;b. H2O2参与反应时,明显放热。回答下列问题:
(1)、仪器b的名称是。仪器d中的药品为。(2)、步骤Ⅰ中,如果不加NH4Cl固体,对制备过程的不利影响是。(3)、步骤Ⅱ中滴加H2O2时应选择___________(填序号)。A、冷水浴 B、温水浴(约为60℃) C、沸水浴 D、酒精灯直接加热(4)、制备[Co(NH3)5Cl]Cl2的总反应化学方程式为。(5)、步骤Ⅳ中依次使用冷水、冷的盐酸、(填试剂名称)洗涤晶体。(6)、本实验的产率为(保留两位小数)。(7)、已知: ; 。则在水溶液中的稳定性:(填“大于”或“小于”)。 -
15、常温下,向饱和AgAc溶液(有足量AgAc固体)中滴加稀硝酸,调节体系pH促进AgAc溶解,总反应为AgAc(s)+H+(aq)Ag+(aq)+HAc(aq),平衡时lgc(Ag+)、分布系数δ(M)与pH的变化关系如图所示〔其中M代表HAc或Ac,δ(HAc)= , Ag+水解忽略不计]。

已知:常温下,pKsp(AgAc)=-lgKsp(AgAc)=2.71。
下列叙述错误的是
A、曲线代表lgc(Ag+)与pH的关系 B、pH=4.5时,溶液中c(HAc)<c() C、pH=6时,溶液中>10 D、AgAc(s)+H+(aq)Ag+(aq)+HAc(aq)的平衡常数K=102.04 -
16、硫酸工业尾气中可用CO处理并回收S,涉及的反应有:
反应I:
反应II:
恒压条件下,按充入原料,其中的平衡转化率以及COS和S的平衡选择性随温度的变化如图所示。已知曲线b表示的平衡选择性。
(X的平衡选择性 , X为COS或S)。

下列说法不正确的是
A、曲线c表示S的平衡选择性 B、 C、1400K下,反应的平衡常数 D、其它条件不变,增大体系压强的平衡转化率不变 -
17、下列实验操作、现象和结论都正确的是
选项
实验操作
实验现象
实验结论
A
适量的通入溶液中
有气泡生成
非金属性:
B
向Mg(OH)2悬浊液中滴加0.1mol/L
的CuCl2溶液,振荡
沉淀由白色变为蓝色
Cu(OH)2的溶解度
小于Mg(OH)2
C
向苯酚浓溶液中滴入少量溴水,振荡
无白色沉淀产生
苯酚与溴水不反应
D
乙醇和浓硫酸共热至170℃后,将
生成的气体通入酸性KMnO4溶液中
KMnO4溶液褪色
乙烯能使KMnO4
溶液褪色
A、A B、B C、C D、D -
18、硫化锂的纳米晶体是开发先进锂电池的关键材料,晶体为立方晶胞,其结构如图。已知为阿伏加德罗常数的值,晶体密度为。下列说法错误的是
 A、Li+位于形成的四面体空隙中 B、晶胞沿轴方向的投影图为
A、Li+位于形成的四面体空隙中 B、晶胞沿轴方向的投影图为 C、该晶胞参数为
D、B点的原子分数坐标为
C、该晶胞参数为
D、B点的原子分数坐标为
-
19、在浓HNO3和浓H2SO4混合溶液中加入苯,反应过程中能量变化示意图如下。下列说法错误的是
 A、对于生成Y的反应,浓H2SO4作催化剂 B、X为苯的加成产物,Y为苯的取代产物 C、由苯得到M时,苯中的碳原子杂化方式没有变化 D、从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
A、对于生成Y的反应,浓H2SO4作催化剂 B、X为苯的加成产物,Y为苯的取代产物 C、由苯得到M时,苯中的碳原子杂化方式没有变化 D、从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ -
20、某种可充电固态锂电池放电时工作原理如图所示,下列说法错误的是
 A、电极电势:b极>a极 B、放电时电子流向:a极→负载→b极 C、充电时,阳极电极反应为:LiLaZrTaO-xe-=xLi++Li1-xLaZrTaO D、外电路通过1mol电子时,理论上两电极质量变化差值为7g
A、电极电势:b极>a极 B、放电时电子流向:a极→负载→b极 C、充电时,阳极电极反应为:LiLaZrTaO-xe-=xLi++Li1-xLaZrTaO D、外电路通过1mol电子时,理论上两电极质量变化差值为7g