相关试卷
-
1、镁基储氢材料MgH2具有储氢量高、成本低廉等优点,发展前景广阔。
Ⅰ.MgH2热分解放出H2 , 反应的能量变化如图所示。
 (1)、写出MgH2热分解的热化学方程式。(2)、提高H2平衡产率的措施有(答1条即可)。(3)、Ⅱ.MgH2水解制备H2
(1)、写出MgH2热分解的热化学方程式。(2)、提高H2平衡产率的措施有(答1条即可)。(3)、Ⅱ.MgH2水解制备H2MgH2与H2O反应制备H2的化学方程式是。
(4)、资料:25℃时,有关物质的溶度积常数如下物质
Mg(OH)2
Ni(OH)2
Cu(OH)2
Ksp
5.6×10−12
5.5×10−16
2.2×10−20
①MgH2与H2O反应时,最初生成H2的速率很快,但随后变得缓慢,原因是。
②在水中加入优先与OH-结合的离子,能够避免①中现象发生,提升H2的制备效率。下列物质中,能达到此目的的是。
a.NaNO3 b.NiCl2 c.CuCl2
-
2、研究电解质在水溶液中的离子反应与平衡有重要的意义。(1)、常温下,用0.100 mol/L NaOH溶液滴定10 mL 0.100 mol/L CH3COOH溶液的滴定曲线如右图所示。a、b、c三点中:

①c(Na+) =c(CH3COO−)的点是.(填“a”、“b”或“c”,下同)。
②水的电离程度最大的点是 。
(2)、已知:25 ℃时CH3COOH、H2CO3和HClO的电离平衡常数:化学式
CH3COOH
H2CO3
HClO
电离平衡常数
(Ka)
1.75×10–5
Ka1=4.5×10–7
Ka2=4.7×10–11
4.0×10–8
①CH3COOH的电离平衡常数表达式Ka=。
②比较等物质的量浓度溶液的pH:pH(NaClO) pH(CH3COONa) (填“>”、“<”或“=”)。
③预测下列化学反应能够发生的是。
A.HClO + CH3COONa = CH3COOH + NaClO
B.CO2 + H2O + NaClO = NaHCO3 + HClO
C.2CH3COOH + Na2CO3 = 2CH3COONa + H2O+CO2
-
3、锂(Li)元素在新能源领域应用广泛。(1)、基态Li原子的电子排布式是 。(2)、Li元素在周期表中的位置是(填写周期、族、区)。(3)、比较第一电离能的大到小:I1(Li) I1(Na)(填“>”、“=”或“<”),从原子结构的角度解释原因。(4)、碳酸锂(Li2CO3)是一种电池原料,其中所含元素的电负性从大到小的顺序是>>。
-
4、某实验小组研究经打磨的镁条与1 mol·L−1 NaHCO3溶液(pH≈8.4)的反应。室温时,用CO2传感器检测生成的气体,并测定反应后溶液的pH。实验如下表:
实验装置
编号
锥形瓶中的
试剂
实验现象
锥形瓶内CO2的浓度变化
①
6.0 g 1 mol·L−1 NaHCO3溶液
有极微量气泡生成,15 min后测得溶液的pH无明显变化

②
6.0 g 1 mol·L−1 NaHCO3溶液和0.1g镁条
持续产生大量气泡(净化后可点燃),溶液中有白色浑浊生成。15 min后测得溶液的pH上升至9.0
③
6.0 g H2O(滴有酚酞溶液)和0.1 g镁条
镁条表面有微量气泡,一段时间后,镁条表面微红
下列说法不正确的是( )
A、由①可知,NaHCO3在溶液中可发生分解反应 B、由②可知,镁与NaHCO3溶液反应,生成的气体中有H2 C、对比②③可知,室温下,NaHCO3溶液中c(H+)大于水中c(H+) D、由②③推测,HCO3-可能对镁与H2O反应生成的Mg(OH)2覆膜有破坏作用 -
5、“中国芯”的主要原料是单晶硅,“精炼硅”反应历程中的能量变化如下图所示。
下列有关描述正确的是( )
 A、历程Ⅰ是吸热反应 B、历程Ⅱ发生了化学变化 C、历程Ⅲ的热化学方程式是:SiHCl3(l) + H2(g) = Si(s)+3HCl(g) ΔH=+238 kJ/mol D、实际工业生产中,粗硅变为精硅的过程无需外界能量供给
A、历程Ⅰ是吸热反应 B、历程Ⅱ发生了化学变化 C、历程Ⅲ的热化学方程式是:SiHCl3(l) + H2(g) = Si(s)+3HCl(g) ΔH=+238 kJ/mol D、实际工业生产中,粗硅变为精硅的过程无需外界能量供给 -
6、回收利用工业废气中的CO2和SO2 , 实验原理示意图如下。

下列说法不正确的是( )
A、废气中SO2排放到大气中会形成酸雨 B、装置a中溶液的作用是吸收废气中的CO2和SO2 C、装置a中溶液显碱性的原因是HCO3-的水解程度大于HCO3-的电离程度 D、装置b中的总反应为 -
7、相同温度下,在三个密闭容器中分别进行反应:H2(g) + I2(g) 2HI(g)。达到化学平衡状态时,相关数据如下表。下列说法不正确的是( )
实验
起始时各物质的浓度/(mol·L-1 )
平衡时物质的浓度/(mol·L-1 )
c(H2)
c(I2)
c(HI)
c(H2)
Ⅰ
0.01
0.01
0
0.008
Ⅱ
0.02
0.02
0
a
Ⅲ
0.02
0.02
0.04
A、该温度下,反应的平衡常数为0.25 B、实验Ⅱ达平衡时,a=0.016 C、实验Ⅲ开始时,反应向消耗H2的方向移动 D、达到化学平衡后,压缩三个容器的体积,平衡均不发生移动 -
8、用0.100 0 mol·L−1 HCl溶液滴定未知浓度的NaOH溶液。下列说法不正确的是( )A、锥形瓶盛装未知浓度的NaOH溶液前必须保持干燥 B、使用滴定管前,要先检查活塞是否漏水,在确保不漏水后方可使用 C、酸式滴定管在盛装0.100 0 mol·L−1 HCl溶液前要用该溶液润洗2~3次 D、用酚酞作指示剂,溶液颜色从粉红色刚好变为无色,且半分钟内不褪色,即达到滴定终点
-
9、一定条件下的密闭容器中发生反应:C2H6(g) C2H4 (g) +H2(g) ΔH > 0。达到平衡后升高反应温度,下列叙述不正确的是( )A、正、逆反应速率都增大 B、平衡向逆反应方向移动 C、C2H6的转化率增大 D、化学平衡常数增大
-
10、下图表示的是元素的某种性质(X)随原子序数的变化关系,则X可能是( )
 A、元素原子的价电子数 B、元素的原子半径 C、元素的电负性 D、元素的第一电离能
A、元素原子的价电子数 B、元素的原子半径 C、元素的电负性 D、元素的第一电离能 -
11、下列离子方程式与所给事实不相符的是( )A、Cl2制备84消毒液(主要成分是NaClO):Cl2 + 2OH- = Cl- + ClO- + H2O B、食醋去除水垢中的CaCO3:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑ C、利用覆铜板制作印刷电路板:2Fe3+ + Cu = 2Fe2+ + Cu2+ D、Na2S去除废水中的Hg2+:Hg2+ += HgS↓
-
12、融雪剂可以降低冰雪融化的温度,利于道路通畅,通常分为氯盐类的无机融雪剂和非氯盐类的有机融雪剂两类。氯化钠、醋酸钾两种融雪剂相同条件下融冰量和对碳钢(铁碳合金)腐蚀速率图像如下所示。回答问题。
图1 不同融雪剂融冰量比较
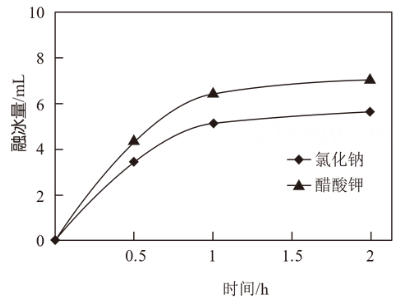 图2 不同盐溶液对碳钢腐蚀比较
图2 不同盐溶液对碳钢腐蚀比较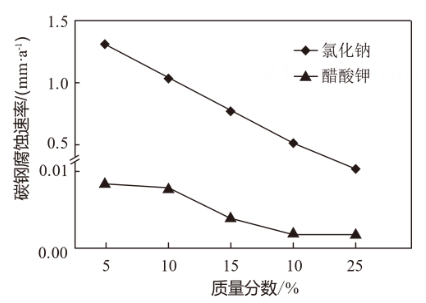 (1)、下列关于醋酸钾(CH3COOK)的说法中,不正确的是( )A、是强电解质 B、电离方程式为CH3COOK=CH3COO-+K+ C、使用CH3COOK融雪后,附近水土酸碱性不受影响 D、由图1可知,与氯化钠相比醋酸钾融冰量高,是更加高效的融雪剂(2)、结合图2分析下列关于碳钢(铁碳合金)腐蚀的说法中,不正确的是( )A、盐类融雪剂能够造成碳钢的腐蚀 B、碳钢腐蚀的负极反应为Fe-2e-=Fe2+ C、融雪剂浓度越大,碳钢腐蚀速率越快 D、寻找环保、高效的融雪剂是新型融雪剂的研究方向
(1)、下列关于醋酸钾(CH3COOK)的说法中,不正确的是( )A、是强电解质 B、电离方程式为CH3COOK=CH3COO-+K+ C、使用CH3COOK融雪后,附近水土酸碱性不受影响 D、由图1可知,与氯化钠相比醋酸钾融冰量高,是更加高效的融雪剂(2)、结合图2分析下列关于碳钢(铁碳合金)腐蚀的说法中,不正确的是( )A、盐类融雪剂能够造成碳钢的腐蚀 B、碳钢腐蚀的负极反应为Fe-2e-=Fe2+ C、融雪剂浓度越大,碳钢腐蚀速率越快 D、寻找环保、高效的融雪剂是新型融雪剂的研究方向 -
13、下列措施是为了增大化学反应速率的是( )A、用锌粒代替镁粉制备氢气 B、将食物放进冰箱避免变质 C、自行车车架镀漆避免生锈 D、工业合成氨时加入催化剂
-
14、下列化学用语书写不正确的是( )A、F的原子结构示意图:
 B、NaCl的电子式:
B、NaCl的电子式: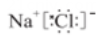 C、基态铬原子(24Cr)的价层电子排布式:3d44s2
D、基态氧原子的轨道表示式:
C、基态铬原子(24Cr)的价层电子排布式:3d44s2
D、基态氧原子的轨道表示式: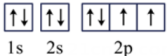
-
15、关于下列现象的分析不合理的是( )

醋酸溶液能导电

氧炔焰切割金属

五彩缤纷的烟花

铸钢模具须提前干燥
A.与盐类水解有关
B.与乙炔和氧气反应放热有关
C.与核外电子的跃迁有关
D.与铁与水能发生反应有关
A、A B、B C、C D、D -
16、载人航天工程对科学研究及太空资源开发具有重要意义,其发展水平是衡量一个国家综合国力的重要指标。中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次正式踏上飞向浩渺星辰的征途。(1)、氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的极,OH-向(填“正”或“负”)极作定向移动,Y极的电极反应式为。
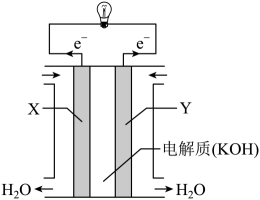 (2)、“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
(2)、“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。①飞船在光照区运行时,太阳能电池帆板将能转化为能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为:Cd+2NiOOH+2H2OCd(OH)2+2Ni(OH)2 , 充电时,阳极的电极反应式为;当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性(填“增强”“减弱”或“不变”)。
②紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O2Ag+Zn(OH)2 , 其负极的电极反应式为。
-
17、中科院天津工业生物技术研究所的科学家在国际上首次突破二氧化碳人工合成淀粉,对减少CO2在大气中累积及实现可再生能源的有效利用具有重要意义。CO2和H2在一定条件下能发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH。回答下列问题:(1)、该反应中反应物与生成物的能量与活化能的关系如图所示,该反应的ΔH=kJ·mol-1(用含Ea1和Ea2的代数式表示)。
 (2)、恒温恒容条件下,下列不能说明该反应达到平衡状态的是____(填标号)。A、ʋ(CO2)正=ʋ(CH3OH)逆 B、CH3OH(g)的体积分数与H2O(g)的体积分数相等 C、混合气体的密度不再变化 D、混合气体的压强不再变化(3)、一定温度下,向一体积为3L的刚性密闭容器中充入3molCO2和6molH2 , 此时容器内的压强为45kPa,发生上述反应,进行5min时达到平衡,此时容器内的压强为30kPa,则0~5min内用H2表示的化学反应速率为mol·L-1·min-1。该温度下,该反应的平衡常数K=L2·mol-2。(4)、以CO2、H2为原料合成CH3OH时,还发生了副反应:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41.5kJ·mol-1。其化学平衡常数(K)和温度(t)的关系如表所示:
(2)、恒温恒容条件下,下列不能说明该反应达到平衡状态的是____(填标号)。A、ʋ(CO2)正=ʋ(CH3OH)逆 B、CH3OH(g)的体积分数与H2O(g)的体积分数相等 C、混合气体的密度不再变化 D、混合气体的压强不再变化(3)、一定温度下,向一体积为3L的刚性密闭容器中充入3molCO2和6molH2 , 此时容器内的压强为45kPa,发生上述反应,进行5min时达到平衡,此时容器内的压强为30kPa,则0~5min内用H2表示的化学反应速率为mol·L-1·min-1。该温度下,该反应的平衡常数K=L2·mol-2。(4)、以CO2、H2为原料合成CH3OH时,还发生了副反应:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41.5kJ·mol-1。其化学平衡常数(K)和温度(t)的关系如表所示:t/℃
700
800
830
1000
1200
K
0.6
0.9
1.0
1.7
2.6
回答下列问题:
①该反应的化学平衡常数表达式为K=。
②该反应为(填“吸热”或“放热”)反应。
③某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),则此时的温度为℃。
-
18、反应热及数据广泛应用于科学研究和工业生产方面。(1)、若1g石墨完全燃烧放出的热量为akJ,则石墨完全燃烧的热化学方程式为。(2)、“长征2F”运载火箭使用N2O4和C2H8N2作推进剂。12.0g液态C2H8N2在液态N2O4中燃烧生成CO2、N2、H2O三种气体,放出510kJ热量。该反应的热化学方程式为。(3)、键能指气态分子解离为气态原子所需的能量。已知 , 其中H—H、O=O、O—H的键能依次为、、 , 又知 , 则氢气的燃烧热。(4)、测定中和反应的反应热的实验步骤如下:①用量筒量取盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取溶液,测出溶液温度;③将溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。上述实验步骤中一处不合理的操作应改成。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热(“偏大”“偏小”或“相等”)。(5)、理论研究表明,在101kPa和298K下,异构化反应的能量变化如图。

①稳定性:HCNHNC(填“>”、“<”或“=”)。
②该异构化反应的ΔH=。
(6)、科学家用氮气和氢气制备肼,过程如下:则 ΔH=kJ/mol(用含a、b、c的计算式表示)。
-
19、已知A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素
B元素原子的核外p电子数比s电子数少1
C原子的第一至第四电离能分别是:I1=738kJ/molI2=1451kJ/mol
I3=7733kJ/molI4=10540kJ/mol
D元素简单离子半径是该周期中最小的
E元素是该周期电负性最大的元素
F所在族的元素种类是周期表中最多的
G在周期表的第十一列
(1)、写出BA3的电子式。(2)、B基态原子中能量最高的电子,其电子云在空间有个方向,原子轨道呈形。(3)、实验室制备E的单质的离子反应方程式为。(4)、B和A中非金属性较强的是(填元素的符号)。(5)、C与D的第一电离能大小为。(6)、G价电子排布图为 , 位于区。(7)、F元素的原子结构示意图为 , 前四周期中未成对电子数最多的元素在周期表中位置为。 -
20、只改变一个条件,化学反应aA(g)+B(g)cC(g)的变化图象如下,其中表示平衡转化率,下列说法正确的是( )
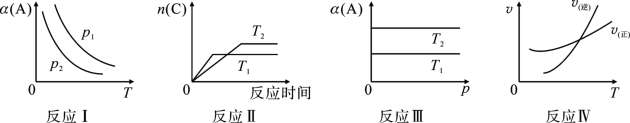 A、反应Ⅰ中,若p1>p2 , 则此反应的ΔS>0 B、反应Ⅱ中,T1温度下B的转化率高于T2温度下B的转化率 C、反应Ⅲ中,若T1>T2 , 则该反应在一定条件下能自发进行 D、反应Ⅳ中,该反应正反应为吸热反应
A、反应Ⅰ中,若p1>p2 , 则此反应的ΔS>0 B、反应Ⅱ中,T1温度下B的转化率高于T2温度下B的转化率 C、反应Ⅲ中,若T1>T2 , 则该反应在一定条件下能自发进行 D、反应Ⅳ中,该反应正反应为吸热反应