相关试卷
-
1、(1)、一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸,用字母填写下列空格:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是。
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是。
(2)、常温下,0.1 mol·L-1的HCl溶液中,由水电离出来的H+浓度为mol·L-1。(3)、在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(A-)=c(M+),而乙同学认为c(A-)和c(M+)是否相等,要看一元酸HA是强酸还是弱酸。你认为同学(填“甲”或“乙”)的说法正确,理由为。(4)、明矾[KAl(SO4)2·12H2O]常用作净水剂,其原理是(用离子方程式表示)。(5)、将FeCl3溶液蒸干并灼烧,最终得到的固体物质是(填写化学式)。 -
2、Ⅰ.以下是关于合成氨的有关问题,请回答:(1)、若在容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在--定条件下发生反应:N2+3H22NH3 △H<0,若5min反应达到平衡,此时测得NH3的物质的量为0.2mol。则0-5min内,用H2表示的化学反应速率为。(2)、平衡后,若提高H2的转化率,可以采取的措施有____。A、加催化剂 B、增大容器体积 C、降低反应体系的温度 D、加入一定量N2(3)、若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)2NH3(g) △H<0,其化学平衡常数K与温度t的关系如表所示:
t℃
200
300
400
K
K1
K2
0.5
请完成下列问题:
①试比较K1、K2的大小,K1K2(填">”、“<”或“=”);
②400℃时,反应2NH3(g)N2(g)+ 3H2(g)的化学平衡常数为。当测得NH3、N2和H2物质的量分别为3mol、2mol和2mol时,则该反应的v(N2)正 v(N2)逆(填“>” “<”或“=”)。
(4)、Ⅱ.肼(N2H4)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-544kJ/mol,键能数据如下表:
化学键
N-N
N-H
O=O
O-H
键能/(kJ/mol)
193
391
497
463
则氮氮三键的键能为kJ/mol。
(5)、已知:N2(g)+2O2(g)=2NO2(g) △H= + 68kJ/mol,则肼和二氧化氮反应生成氮气和水蒸气的热化学方程式为。 -
3、25 ℃时,将一定浓度的盐酸和一定浓度的氨水按2∶1的体积比混合,若混合溶液中c()=c(Cl-),则溶液的pH ( )A、大于7 B、小于7 C、等于7 D、无法确定
-
4、将V1mL 1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )
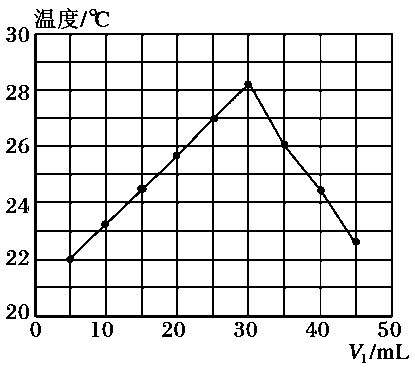 A、做该实验时环境温度为22℃ B、该实验表明有水生成的反应都是放热反应 C、NaOH溶液的浓度约为1.0mol/L D、该实验表明化学能可能转化为热能
A、做该实验时环境温度为22℃ B、该实验表明有水生成的反应都是放热反应 C、NaOH溶液的浓度约为1.0mol/L D、该实验表明化学能可能转化为热能 -
5、在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是 ( )
 A、向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CH3COO-) B、25 ℃时,加入CH3COONa可能引起由b向a的变化,升温可能引起由a向c的变化 C、T℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液呈中性 D、b点对应的溶液中大量存在:K+、Ba2+、NO3-、I-
A、向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CH3COO-) B、25 ℃时,加入CH3COONa可能引起由b向a的变化,升温可能引起由a向c的变化 C、T℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液呈中性 D、b点对应的溶液中大量存在:K+、Ba2+、NO3-、I- -
6、常温下1mol化学键分解成气态原子所需要的能量用E表示,结合表中信息下列说法不正确的是( )
共价键
H-H
F-F
H-F
H-Cl
H-I
E(kJ/mol)
436
157
568
432
298
A、表中最稳定的共价键是H-F B、1mol H2(g)与1 mol F2(g)生成2 mol HF(g)放出25 kJ的能量 C、432kJ/mol> E(H-Br)> 298kJ/mol D、1mol H2(g)分解成2 mol H(g)需放出436 kJ的能量 -
7、下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是 ( )
选项
A
B
C
D
强电解质
HNO3
NaCl
BaSO4
盐酸
弱电解质
CH3COOH
NH3
H3PO4
Fe(OH)3
非电解质
C6H12O6(葡萄糖)
CO2
C2H5OH
H2O
A、A B、B C、C D、D -
8、下列反应中,反应速率最大的是( )A、25 ℃时,镁条与0.1 mol·L-1盐酸反应 B、25 ℃时,镁条与0.2 mol·L-1盐酸反应 C、35 ℃时,镁条与0.2 mol·L-1盐酸反应 D、35 ℃时,镁条与0.3 mol·L-1盐酸反应
-
9、一定温度下,将2 mol A和2 mol B两种气体混合放入体积为2 L的密闭刚性容器中,发生反应3A(g)+B(g) = xC(g)+2D(g),2 min 末反应达到平衡,生成0.8 mol D,并测得C的物质的量浓度为0.4 mol/L,下列说法正确的是 ( )A、此温度下该反应的平衡常数K等于0.5 B、A的平衡转化率为40% C、x的值为1 D、A和B的平衡转化率相等
-
10、如图所示是298K时,A2与B2反应过程中能量变化的曲线图,下列叙述正确的是 ( )
 A、每生成2 molAB吸收b kJ热量 B、加入催化剂,反应的活化能和反应热都改变 C、该反应的热化学方程式为A2(g)+B2(g)=2AB(g) △H= + (a-b) kJ/mol D、断裂1 mol A-A和1 mol B-B键,放出a kJ能量
A、每生成2 molAB吸收b kJ热量 B、加入催化剂,反应的活化能和反应热都改变 C、该反应的热化学方程式为A2(g)+B2(g)=2AB(g) △H= + (a-b) kJ/mol D、断裂1 mol A-A和1 mol B-B键,放出a kJ能量 -
11、反应2NO2(g)N2O4(g) △H=-57 kJ/mor, 在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ( )
 A、T1>T2 B、X、Y两点的反应速率:X>Y C、X、Z两点气体的颜色:X深,Z浅 D、X、Z两点气体的平均相对分子质量:X>Z
A、T1>T2 B、X、Y两点的反应速率:X>Y C、X、Z两点气体的颜色:X深,Z浅 D、X、Z两点气体的平均相对分子质量:X>Z -
12、如图是向100 mL pH=1的盐酸中逐渐加入NaOH溶液时,溶液pH的变化图像,根据如图所得结论正确的是( )
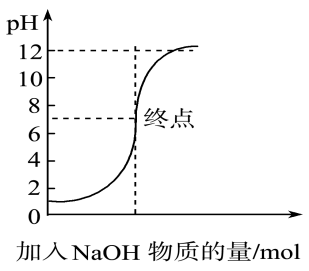 A、原来盐酸的物质的量浓度为0.1 mol·L-1 B、NaOH溶液的物质的量浓度为0.1 mol·L-1 C、原来盐酸的物质的量浓度为1 mol·L-1 D、NaOH溶液的物质的量浓度为0.01 mol·L-1
A、原来盐酸的物质的量浓度为0.1 mol·L-1 B、NaOH溶液的物质的量浓度为0.1 mol·L-1 C、原来盐酸的物质的量浓度为1 mol·L-1 D、NaOH溶液的物质的量浓度为0.01 mol·L-1 -
13、下列有关化学平衡常数的描述中正确的是 ( )A、化学平衡常数的大小取决于化学反应本身,与其他外界条件无关 B、相同温度下,反应与反应的化学平衡常数相同 C、反应的化学平衡常数随温度升高而增大 D、反应的平衡常数达式为
-
14、反应4A(s)+3B(g)2C(g)+D(g),经2 min 后B的浓度减少0.6 mol·L-1。下列说法正确的是 ( )A、用A表示的反应速率是0.4 mol·L-1·min-1 B、在2 min末的反应速率,用B表示是0.3 mol·L-1·min-1 C、分别用B、C、D表示的反应速率,其比值是3∶2∶1 D、在这2 min内B和C两物质浓度是逐渐减小的
-
15、在一密闭容器中发生反应:2A(g)+2B(g)C(s)+3D(g)ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是 ( )A、移走少量C B、选择良好的催化剂 C、缩小容积,增大压强 D、容积不变,充入1molN2(N2不参加反应)
-
16、在反应2HIH2+I2中,有关反应条件改变使反应速率增大的原因分析中,不正确的是 ( )A、加入适宜的催化剂,可降低反应的活化能 B、增大 , 单位体积内活化分子数增大 C、升高温度,单位时间内有效碰撞次数增加 D、增大压强,活化分子的百分数增大
-
17、下列离子方程式表示的是盐类的水解且正确的是 ( )A、 B、 C、 D、
-
18、下列热化学方程式中,正确的是( )A、甲烷的燃烧热 , 则甲烷燃烧热的热化学方程式可表示为: B、在时,完全燃烧生成液态水,放出热量,燃烧的热化学方程式表示为 C、HCl和NaOH反应的中和热 , 则和反应的中和热 D、、下,已知热化学方程式: , 将和置于密闭容器中充分反应生成 , 放热
-
19、某天然氨基酸M是人体必需的氨基酸之一,其合成路线如下:

已知:①


②

 (1)、A→B的反应条件和试剂是;化合物F的名称为;(2)、I→J的反应类型是;(3)、写出D→E反应的化学方程式;(4)、I与乙二醇反应可生成能降解的高分子化合物N,写出该反应的化学方程式;(5)、符合下列条件的化合物M的同分异构体共有种(不考虑立体异构);
(1)、A→B的反应条件和试剂是;化合物F的名称为;(2)、I→J的反应类型是;(3)、写出D→E反应的化学方程式;(4)、I与乙二醇反应可生成能降解的高分子化合物N,写出该反应的化学方程式;(5)、符合下列条件的化合物M的同分异构体共有种(不考虑立体异构);①含有苯甲酸结构 ②含有一个甲基 ③苯环上只有两个取代基
其中核磁共振氢谱峰面积比为1:1:2:2:2:3的分子的结构简式(任写一种);
(6)、请结合以上合成路线,写出以丙酸和上述流程中出现的物质为原料经三步合成丙氨酸( )的路线。
)的路线。 -
20、A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子的2p能级有3个电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。回答下列问题:(1)、写出基态E+的价电子排布式:。基态A原子的第一电离能比B的大,其原因是。(2)、A5+由美国空军研究实验室推进科学与先进概念部Karl .O.Christed 于1999年成功合成,其结构呈‘V'形且该离子中各原子均达到8电子稳定结构,则A5+的结构式为。(3)、B3分子的空间构型为 , 其中B原子的杂化类型是 , 与B3分子互为等电子体的微粒有(写一种离子)。(4)、向E的硫酸盐溶液中通入A的气态氢化物至过量,产生蓝色沉淀,随后沉淀溶解得到深蓝色溶液,向溶液中加入适量乙醇,析出蓝色晶体。加入乙醇的目的。 写出该配合物中配离子的结构简式。(5)、由长周期元素组成的镧镍合金、铜钙合金有相同类型的晶体结构XYn , 它们有很强的储氢能力,其中铜钙合金的晶体的部分结构如图所示。

已知镧镍合金(LaNin)晶体中的重复结构单元如图一所示,该结构单元的体积为9.0×10-23cm3 , 储氢后形成LaNinH4.5的合金(氢进入晶体空隙,体积不变),则LaNin中n=(填数值);氢在合金中的密度为g/L。