相关试卷
-
1、已知:NaClO能与水缓慢反应生成NaOH、HClO。某小组探究“84消毒液”的性质,请你参与他们的探究活动。
[观察]“84消毒液”是一种透明的液体。
[预测]NaClO中Cl显+1价,可能具有漂白性;它是弱酸盐,能与较强酸反应。
[实验]在相同条件下进行实验,测得“84消毒液”的漂白效率与温度的关系如图所示。
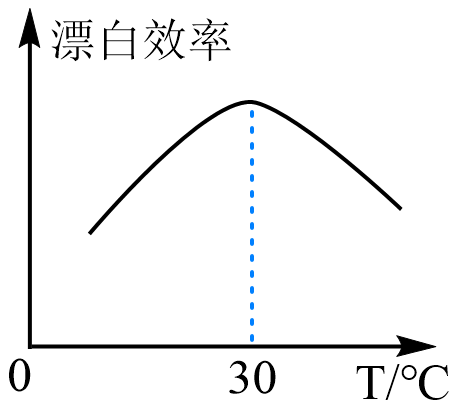
下列判断正确的是( )
A、上述探究活动中只用到了观察法、实验法 B、可用pH试纸测定“84消毒液”的pH值 C、“84消毒液”需密封保存,使用时可用沸水稀释 D、温度大于30℃时,漂白效率降低的原因可能是HClO分解加快 -
2、一定温度下,向饱和的烧碱溶液中加入一定量的金属钠,充分反应后恢复到原温度,下列叙述正确的是( )A、溶液中数目减少,有放出 B、溶液中溶质的质量分数增大,有放出 C、溶液中溶质的质量分数不变,有放出 D、溶液中数目增大,有放出
-
3、某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,并测得溶液的导电能力随时间的变化曲线如图所示。下列说法错误的是(不考虑水的电离)( )
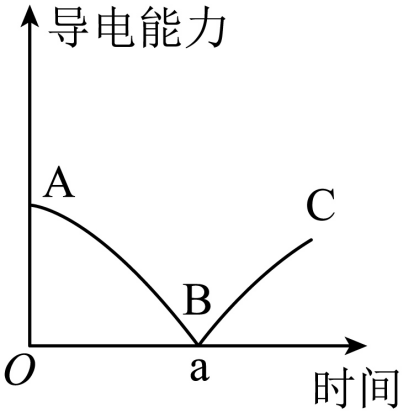 A、A点溶液中的微粒只有Ba2+和OH- B、B点表示Ba(OH)2溶液与稀硫酸恰好完全中和 C、B—C的过程中。溶液的导电能力逐渐增强的原因之一是溶液中能够自由移动的离子数目增多(单位体积内) D、A—C的过程中。仅发生一种属于基本反应类型的反应
A、A点溶液中的微粒只有Ba2+和OH- B、B点表示Ba(OH)2溶液与稀硫酸恰好完全中和 C、B—C的过程中。溶液的导电能力逐渐增强的原因之一是溶液中能够自由移动的离子数目增多(单位体积内) D、A—C的过程中。仅发生一种属于基本反应类型的反应 -
4、已知由二氧化碳和氧气组成的混合气体,其平均相对分子质量为38,则该混合气体中二氧化碳和氧气的质量比为( )A、1∶1 B、1∶2 C、11∶8 D、8∶11
-
5、电视剧中《三生三世十里桃花》中的仙境美轮美奂,其中所需的烟雾是在放于温热石棉网上的和Zn粉的混合物中滴几滴水后产生的白烟: , 下列说法中正确的是( )A、该反应中仅是还原产物 B、常温下每消耗1.3gZn粉,即可产生 C、该反应中作氧化剂,Zn作还原剂 D、每生成1molZnO共转移5mol电子
-
6、对于相同质量的二氧化硫和三氧化硫来说,下列关系正确的是( )A、气体分子数之比为1:1 B、原子个数之比为3:4 C、气体体积之比为5:4 D、含硫原子的个数比为5:4
-
7、下列对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断均正确的是( )
选项
陈述Ⅰ
陈述Ⅱ
判断
A
氯气能使湿润的红色布条褪色
氯气具有漂白性
Ⅰ对;Ⅱ对;有
B
可作潜水艇的供氧剂
能和、反应生成
Ⅰ对;Ⅱ对;有关系
C
金属钠在空气中很容易变质
金属钠具有强还原性
Ⅰ错;Ⅱ对;有关系
C
中
 少量杂质可将气体通入饱和溶液除去
少量杂质可将气体通入饱和溶液除去可与反应
Ⅰ对,Ⅱ对,有去
A、A B、B C、C D、D -
8、下列溶液中,能大量共存的离子组是( )A、含大量的溶液:、、、 B、含大量溶液:、、、 C、某强碱性溶液:、、、 D、含大量的溶液:、、、
-
9、有两个无标签的试剂瓶,分别盛有Na2CO3、NaHCO3固体,有四位同学为鉴别它们采用了以下不同方法,其中不可行的是( )A、分别将它们配制成溶液,再加入澄清石灰水 B、分别将它们配制成溶液,再加入CaCl2溶液 C、分别将它们配制成溶液,再逐滴滴加稀盐酸 D、分别加热,再用澄清石灰水检验是否有气体产生
-
10、下列说法正确的是( )A、的摩尔质量是 B、标准状况下,水中约含个分子 C、常温常压下,中所含氧原子数约为 D、常温常压下,的体积是
-
11、下列物质不可由对应的两种单质直接化合制备的是( )A、 B、HCl C、 D、
-
12、英国化学家汉弗里·戴维在十九世纪初通过电解的方式获得金属钠的单质,下列有关金属钠的性质描述,错误的是( )A、金属钠性质活泼,一般保存在煤油中 B、Na的金属性强,可从硫酸铜溶液中置换出铜 C、金属钠可用刀切割,说明其硬度较小 D、使用后多余的金属钠应放回试剂瓶中
-
13、下列反应中,属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )A、2Na+2H2O=2NaOH+H2↑ B、Cl2+H2O=HCl+HClO C、SO2+H2O=H2SO3 D、C+H2OCO↑+H2↑
-
14、下列生活中的化学现象与氧化还原知识无关的是( )A、菜刀洗过后如果没擦干,放置一段时间就会出现斑点 B、用盐酸可以除去铁锈 C、用天然气做饭烧菜 D、月饼盒中放置硫酸亚铁粉末包
-
15、下列反应的离子方程式书写正确的是( )A、大理石与盐酸反应: B、铜与硝酸银溶液反应: C、稀硝酸与氢氧化钾溶液反应: D、二氧化碳与氢氧化钠溶液反应:
-
16、下列属于非电解质的是( )A、酒精溶液 B、Cu C、熔融 D、
-
17、溶液和胶体这两种分散系的根本区别是( )A、是否能通过半透膜 B、分散质粒子直径的大小 C、是否存在丁达尔效应 D、是否均一、透明、稳定
-
18、某自热火锅发热包的成分为生石灰、苛性钠、铝粉、活性炭、还原铁粉、纯碱。下列关于发热包成分的物质分类正确的是( )
选项
A
B
C
D
物质
苛性钠、纯碱
铝粉、铁粉
生石灰
活性炭、纯碱
类别
碱
单质
酸性氧化物
含碳化合物
A、A B、B C、C D、D -
19、某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在250 mL容量瓶中配制250 mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
请完成下列问题:
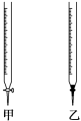 (1)、正确的操作步骤是(填写字母)→→→D→;(2)、 若用标准浓度的H2SO4溶液测定NaOH溶液的浓度,参看图示从下表中选出正确选项( )
(1)、正确的操作步骤是(填写字母)→→→D→;(2)、 若用标准浓度的H2SO4溶液测定NaOH溶液的浓度,参看图示从下表中选出正确选项( )锥形瓶中溶液
滴定管中溶液
选用指示剂
选用滴定管
A
碱
酸
石蕊
乙
B
酸
碱
酚酞
甲
C
碱
酸
甲基橙
甲
D
酸
碱
石蕊
乙
(3)、 操作D中液面应调整到 , 尖嘴部分应;(4)、 滴定终点时的颜色变化是;(5)、若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响(填“偏高”、“偏低”或“无影响”,其他操作均正确);(6)、该烧碱样品的纯度计算式是。 -
20、已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示:
酸
电离平衡常数
醋酸
碳酸
亚硫酸
(1)、根据上表可知,试比较同浓度Na2CO3、Na2SO3溶液的pH:Na2CO3Na2SO3。(填“>” “<”或 “=”,下同)(2)、向0.1 mol∙L−1的CH3COONa溶液中加入少量下列物质,其水解程度增大的是____。A、NaCl溶液 B、Na2CO3固体 C、NH4Cl溶液 D、CH3COONa固体(3)、已知常温下NH3∙H2O的电离常数 ,则常温下CH3COONH4溶液的pH7。(4)、将pH=4的溶液稀释100倍后溶液的pH范围是 , 图中的纵坐标可以是。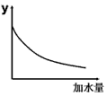
a.溶液的pH b.醋酸的电离平衡常数
c.溶液的导电能力 d.醋酸的电离程度
(5)、NaHSO3是中学化学常见的物质。在水溶液中存在如下两个平衡Ka2
Kh2(水解平衡常数,表示水解程度)
已知25 ℃时,Ka2 > Kh2 , 则0.1 mol∙L−1 NaHSO3溶液呈(填“酸性”“碱性”或“中性”);其中c(Na+)c()(填“>”“<”或“=”);其电荷守恒表达式可写为。