相关试卷
-
1、指出下列氧化还原反应中的氧化剂和还原剂:(1)、在Fe2O3+3CO2Fe+3CO2反应中 , 氧化剂是 ;还原剂是(2)、在Zn+H2SO4= ZnSO4+H2↑ 反应中 , 氧化剂是 ;还原剂是(3)、在4Na+O2= 2Na2O反应中 , 氧化剂是 ;还原剂是(4)、在CuO+H2Cu+H2O 反应中 , 氧化剂是 ;还原剂是
-
2、认识氧化还原反应,根据所学知识填空:(1)、氧化还原反应的特征是;氧化还原反应的本质是; 对于反应MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O (2)、MnO2中的Mn元素化合价(填“升高”或“降低”),在反应中电子(填“得到”或“失去”),发生反应(填“氧化”或“还原”)。(3)、HCl中的Cl元素化合价(填“升高”或“降低”),在反应中电子(填“得到”或“失去”),发生反应(填“氧化”或“还原”)。
MnCl2+Cl2↑+2H2O (2)、MnO2中的Mn元素化合价(填“升高”或“降低”),在反应中电子(填“得到”或“失去”),发生反应(填“氧化”或“还原”)。(3)、HCl中的Cl元素化合价(填“升高”或“降低”),在反应中电子(填“得到”或“失去”),发生反应(填“氧化”或“还原”)。 -
3、写出下列反应的离子反应方程式:(1)、NaOH溶液和HCl溶液:;(2)、NaCl溶液和AgNO3溶液:;(3)、Ba(OH)2溶液和H2SO4溶液:;(4)、Fe与CuSO4溶液反应:;
-
4、按要求用序号填空:(1)、现有下列几种物质:①H2O ②空气 ③Mg ④CaO ⑤H2SO4 ⑥Ca(OH)2⑦CuSO4 ⑧碘酒 ⑨葡萄糖 ⑩NaHCO3。
其中属于混合物的是(填序号,下同);属于单质的是;属于酸的是;属于盐的是 ;属于有机物的是 。
(2)、现有以下几种物质:①NaHCO3晶体 ②液态HCl ③铁 ④蔗糖⑤酒精 ⑥熔融的K2SO4 ⑦干冰 ⑧石墨
其中能导电的是;(填序号,下同)
属于非电解质的是;属于电解质的是。
-
5、写出下列物质在水溶液中电离的电离方程式(1)、写出KOH 的电离方程式:(2)、写出(NH4)2CO3的电离方程式:(3)、写出K2SO4 的电离方程式:
-
6、写出下列物质的化学式:(1)、硝酸钡;(2)、硫酸铝;(3)、硫酸钠;(4)、氢氧化铜 ;(5)、碳酸钙;(6)、氯化铵。
-
7、火药的爆炸反应为 , 其中被还原的元素是( )A、N B、C C、N和S D、N和C
-
8、有关右边的基本化学反应类型与氧化还原反应关系图,解读错误的是( )
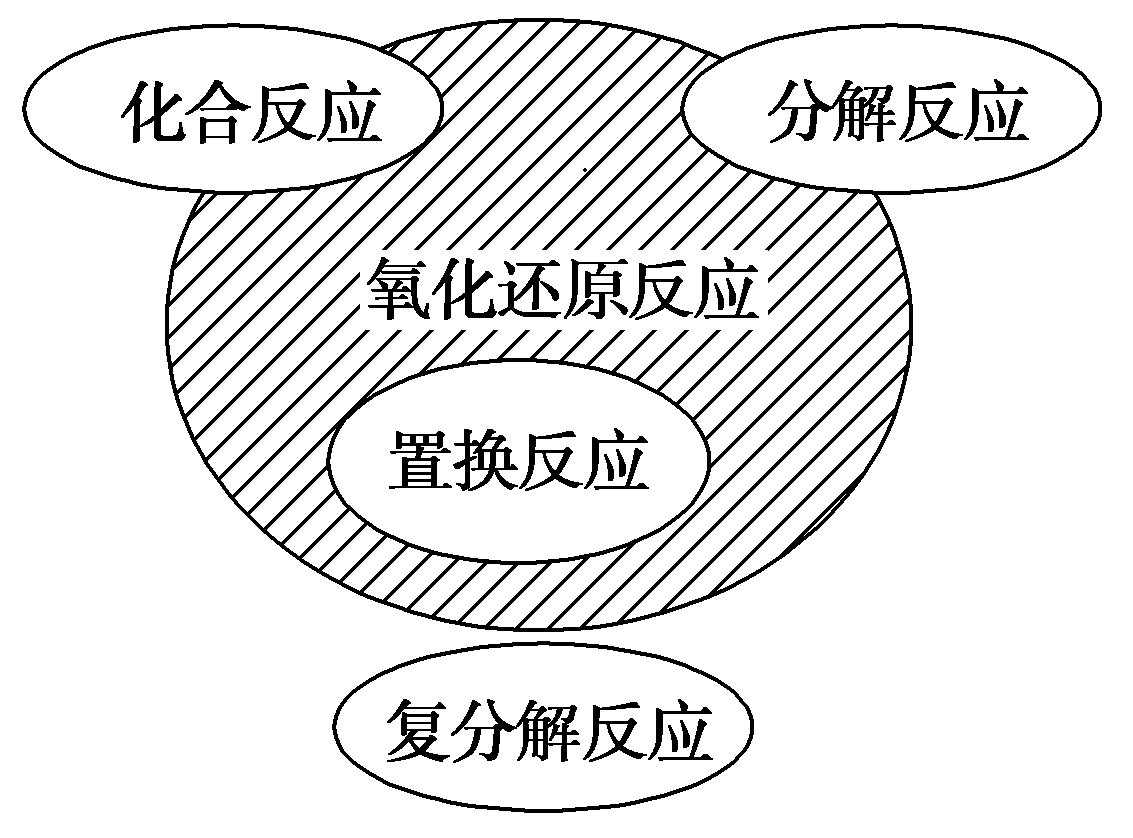 A、置换反应一定是氧化还原反应 B、复分解反应可能是氧化还原反应 C、分解反应不一定是氧化还原反应 D、有单质参加的化合反应一定是氧化还原反应
A、置换反应一定是氧化还原反应 B、复分解反应可能是氧化还原反应 C、分解反应不一定是氧化还原反应 D、有单质参加的化合反应一定是氧化还原反应 -
9、下列电离方程式正确的是( )A、H2SO4=H2++SO42- B、Ca(OH)2=Ca2++(OH)2- C、AlCl3=Al+3+3Cl-1 D、Al2(SO4)3=2Al3++3SO42-
-
10、化学兴趣小组在家中进行化学实验,按左图连接好线路发现灯泡不亮,按照右图连接好线路发现灯泡亮,由此得出的结论正确的是( )
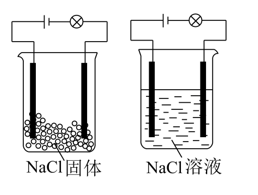 A、NaCl是非电解质 B、NaCl溶液是电解质 C、NaCl在水溶液中电离出了可以自由移动的离子 D、NaCl固体能导电
A、NaCl是非电解质 B、NaCl溶液是电解质 C、NaCl在水溶液中电离出了可以自由移动的离子 D、NaCl固体能导电 -
11、下列物质属于电解质的是( )A、熔融的NaOH B、铁丝 C、CO2 D、KCl溶液
-
12、下列说法正确的是( )A、不能导电物质就是非电解质 B、其水溶液能导电的化合物就是电解质 C、电解质任何状态下都能导电 D、酸、碱、盐都是电解质
-
13、下列分散系不能发生丁达尔现象的是( )A、稀豆浆 B、硫酸铜溶液 C、血液 D、雾
-
14、科学家发现了一种纯碳新材料“碳纳米泡沫”,每个碳纳米泡沫含有约4000个碳原子,直径约6~9nm,则这种“碳纳米泡沫”分散到空气中属于( )A、溶液 B、悬浊液 C、乳浊液 D、胶体
-
15、下列有关概念说法正确的是( )A、盐酸、冰水混合物、空气都属于混合物 B、金属氧化物均为碱性氧化物 C、只由一种元素组成的物质一定是单质 D、CuSO4∙5H2O属于纯净物
-
16、下列各组物质不互为同素异形体的是( )A、H2O和H2O2 B、O2和O3 C、金刚石和石墨 D、红磷和白磷
-
17、1942年,我国化工专家侯德榜以NaCl、NH3(氨气)、CO2等为原料先制得NaHCO3 , 进而生产出纯碱,他的“侯氏制碱法”为世界制碱工业做出了突出贡献。
某同学模拟工艺流程,制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)。
已知:NH3极易溶于水,溶液呈碱性。

请回答:
(1)、写出甲中发生反应的离子方程式。(2)、乙装置中的试剂是。(3)、实验结束后,分离出NaHCO3晶体的操作是(填分离操作的名称)。(4)、装置丙中析出NaHCO3的原因是a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(5)、请写出从NaHCO3晶体获得纯碱的化学方程式。(6)、检验产品碳酸钠中含有氯化钠,请你把以下实验方案补充完整:操作:取少量试样溶于水中,再滴加。
现象:。
-
18、“化学我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”道理。请填空:(1)、工业上可以利用氯气制漂白粉,其化学方程式为:。(2)、研究小组用下图装置制取:

仪器A的名称为;A中反应的离子方程式为;
(3)、下列收集的正确装置是 。A、 B、
B、 C、
C、 D、
D、 (4)、某同学设计了如图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:
(4)、某同学设计了如图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:
①浓的作用是;
②与研究目的直接相关的实验现象是 , 并解释产生上述现象的原因;
③该实验设计存在事故隐患,应在D处增加一装置,该装置的作用是。
-
19、填空:(1)、某金属氯化物 , 含有 , 则该化合物的摩尔质量为;(2)、含有个水分子;(用表示,代表阿伏加德罗常数的值)(3)、(标况)约含mol氢原子;(4)、个含有电子的物质的量为;(5)、含 , R的相对原子质量为。
-
20、回答下列问题:(1)、下列物质能导电的是 , 属于电解质的是 , 属于非电解质的是。
①NaCl晶体,②液态 , ③液态醋酸,④铜,⑤固体,⑥蔗糖(),⑦氨水
(2)、和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:①请配平上述化学方程式:;
②浓盐酸在反应中显示出来的性质是(填编号)
A.还原性 B.酸性 C.氧化性
③氧化剂是 , 氧化产物是;
④每产生 , 则转移的电子的物质的量为mol。