相关试卷
-
1、钙钛矿类杂化材料在太阳能电池领域具有重要的应用价值,其晶胞参数如图1所示,代表 , 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如的原子分数坐标为 , B的原子分数坐标为。设为阿伏加德罗常数的值,晶体的密度为。下列说法中错误的是( )
 A、该晶胞含有3个 B、粒子与粒子之间最近距离为 C、为 D、若沿轴向平面投影,则其投影图如图2所示
A、该晶胞含有3个 B、粒子与粒子之间最近距离为 C、为 D、若沿轴向平面投影,则其投影图如图2所示 -
2、下列各组离子能大量共存,且加入相应试剂后发生反应的离子方程式正确的是( )
选项
离子组
加入试剂
加入试剂后发生的离子反应
A
溶液
B
溶液
C
气体
D
酸性溶液
A、A B、B C、C D、D -
3、一种可充电锌—空气电池放电时的工作原理如下图所示。已知:Ⅰ室溶液中,锌主要以的形式存在,并存在电离平衡。下列说法错误的是( )
 A、放电时,Ⅰ室溶液中浓度增大 B、放电时,Ⅱ室中的通过阴离子交换膜进入Ⅰ室 C、充电时,电极的电极反应为 D、充电时,每生成 , Ⅲ室溶液质量理论上减少
A、放电时,Ⅰ室溶液中浓度增大 B、放电时,Ⅱ室中的通过阴离子交换膜进入Ⅰ室 C、充电时,电极的电极反应为 D、充电时,每生成 , Ⅲ室溶液质量理论上减少 -
4、下列实验操作、现象、实验结论均正确的是( )
选项
实验操作
现象
结论
A
向两支盛有等浓度等体积的试管中分别加入等浓度等体积的溶液和溶液
前者产生气泡速率快
的催化效果比好
B
取于试管中,加入溶液,充分反应后滴入5滴15%的溶液
溶液变红
与的反应有一定限度
C
取A、B两试管,各加入的 , 向A中加酸性高锰酸钾溶液,同时向B中加入酸性高锰酸钾溶液
B试管先褪为无色
其他条件不变时,增大反应物的浓度,反应速率加快
D
向溶液中滴加2滴等浓度的出现白色沉淀,过滤后取上层清 液又加入2滴溶液
有黄色沉淀生成
A、A B、B C、C D、D -
5、为除去粗盐水中含有的杂质、和 , 得到精制食盐,设计了如下实验流程

下列说法不正确的是( )
A、NaOH溶液的作用是除去 B、步骤i、ii的顺序可以互换 C、滤液2中有四种离子:、、、 D、步骤iv中发生的离子反应为:、 -
6、实验室中可通过香草胺与8-甲基壬酸为原料合成二氢辣椒素,下列有关说法正确的是( )
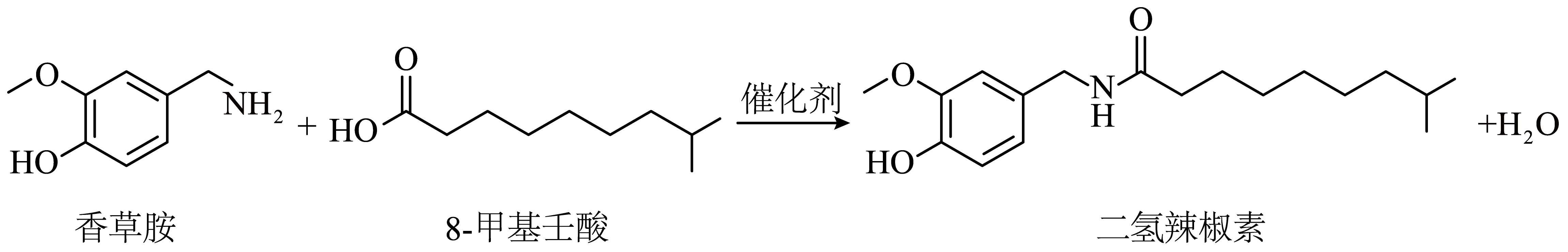 A、香草胺中含有两种官能团 B、二氢辣椒素结构中具有一个手性碳原子 C、1 mol二氢辣椒素与过量NaOH溶液作用,最多可消耗3 mol NaOH D、产物提纯后,可通过红外光谱检测酰胺基的存在,初步确定此合成是否成功
A、香草胺中含有两种官能团 B、二氢辣椒素结构中具有一个手性碳原子 C、1 mol二氢辣椒素与过量NaOH溶液作用,最多可消耗3 mol NaOH D、产物提纯后,可通过红外光谱检测酰胺基的存在,初步确定此合成是否成功 -
7、物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,实验室中常用洗涤残留在试管壁上的N单质。下列说法错误的是( )
 A、X、Z形成的化合物与M、N形成的化合物可以发生氧化还原反应 B、实验室中用洗涤残留在试管壁上的N单质,利用了N单质的还原性 C、Z的氢化物的沸点不一定大于Y的氢化物的沸点 D、化合物W常用作氧化剂,不宜在高温下使用
A、X、Z形成的化合物与M、N形成的化合物可以发生氧化还原反应 B、实验室中用洗涤残留在试管壁上的N单质,利用了N单质的还原性 C、Z的氢化物的沸点不一定大于Y的氢化物的沸点 D、化合物W常用作氧化剂,不宜在高温下使用 -
8、检验黑木耳中铁离子的步骤为:灼烧黑木耳→加酸溶解→过滤→取滤液检验,所选择的装置(夹持装置已略去)或操作不正确的是( )




A.灼烧黑木耳
B.加酸后搅拌溶解
C.过滤得滤液
D.检验铁离子
A、A B、B C、C D、D -
9、化学既神奇又美丽。下列说法正确的是( )A、冬天飞舞的雪花,水分子之间通过O-H键结合形成晶体 B、金刚石中碳原子之间通过C-C键形成空间网状结构 C、CuSO4溶液中加入过量浓氨水得到深蓝色溶液,Cu(OH)2溶液为深蓝色 D、碘升华得到紫色碘蒸气,升华过程破坏了碘分子之间的氢键
-
10、利用反应可制备化工试剂 . 下列说法正确的是( )A、的电子式为 B、基态原子的价电子排布图为
 C、为共价化合物
D、的VSEPR模型为平面三角形
C、为共价化合物
D、的VSEPR模型为平面三角形
-
11、中华文明源远流长,化学与文化传承密不可分。下列物质主要由合金材料制成的是( )




A.裴李岗文化骨笛
B.走马楼简牍
C.商朝后期陶埙
D.曾侯乙青铜编钟
A、A B、B C、C D、D -
12、比哌立登是一种抗震颤麻痹药,可用于轻型帕金森综合症的治疗。其合成路线如图:

回答下列问题:
(1)、C中官能团的名称为。(2)、A→C的化学反应方程式为。(3)、D与G合成H的反应类型为。(4)、根据物质结构知识判断沸点:
 (填“>”或“<”)。 (5)、J是C的同分异构体,J能与FeCl3发生显色反应,符合条件的J有种,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:3:6的结构简式为(写一种即可)。(6)、参照上述合成路线,以1,3-丁二烯和
(填“>”或“<”)。 (5)、J是C的同分异构体,J能与FeCl3发生显色反应,符合条件的J有种,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:3:6的结构简式为(写一种即可)。(6)、参照上述合成路线,以1,3-丁二烯和 主要原料,设计
主要原料,设计 的合成路线(无机试剂和含有三个碳原子以下的有机试剂任选)。
的合成路线(无机试剂和含有三个碳原子以下的有机试剂任选)。 -
13、低碳烯烃是基础有机化工原料,工业上可利用合成气直接或间接制取。主要反应方程式如下。
间接制取低碳烯烃:CO(g)+2H2(g)CH3OH(l) △H1=-116kJ•mol-1
2CH3OH(l) C2H4(g)+2H2O(l) △H2=-35kJ•mol-1
直接制取低碳烯烃:2CO(g)+4H2(g) C2H4(g)+2H2O(g) △H3
回答下列问题:
(1)、已知H2O(g) H2O(l) △H=-44kJ•mol-1 , 则△H3=kJ/mol。(2)、将N2、CO和H2以体积比为1:1:2充入密闭容器中直接制取乙烯,CO的平衡转化率与温度的关系如图1所示,则P1P2(填“>”“<”或“=”),M点的正反应速率N点的逆反应速率(填“>”“<”或“=”)。在500K,压强为P1的条件下,该反应的Kp=(列出计算式)。 (3)、已知反应空速是指一定条件下,单位时间单位体积(或质量)催化剂处理的气体量。在常压、450℃,n(CO):n(H2)为1:2的条件下,利用合成气直接制取乙烯。反应空速对CO转化率和乙烯选择性[选择性=×100%]的影响如图2所示。随着反应空速的增加,乙烯的选择性先升高后降低的原因是。
(3)、已知反应空速是指一定条件下,单位时间单位体积(或质量)催化剂处理的气体量。在常压、450℃,n(CO):n(H2)为1:2的条件下,利用合成气直接制取乙烯。反应空速对CO转化率和乙烯选择性[选择性=×100%]的影响如图2所示。随着反应空速的增加,乙烯的选择性先升高后降低的原因是。 (4)、利用合成气制取低碳烯烃时,需使合成气吸附在催化剂表面的活性位点上。研究发现催化剂晶体的颗粒越小,催化效果越好,其理由是。(5)、Ga2O3是工业上利用合成气制低碳烯烃的催化剂,其晶体结构单元如图3所示(O2-之间紧密堆积,Ga3+位于O2-形成的空隙中且未画出),其中O2-半径为anm,晶体结构单元的高为bnm。已知阿伏加德罗常数的值为NA , 则Ga2O3晶体的摩尔体积Vm=m3/mol。
(4)、利用合成气制取低碳烯烃时,需使合成气吸附在催化剂表面的活性位点上。研究发现催化剂晶体的颗粒越小,催化效果越好,其理由是。(5)、Ga2O3是工业上利用合成气制低碳烯烃的催化剂,其晶体结构单元如图3所示(O2-之间紧密堆积,Ga3+位于O2-形成的空隙中且未画出),其中O2-半径为anm,晶体结构单元的高为bnm。已知阿伏加德罗常数的值为NA , 则Ga2O3晶体的摩尔体积Vm=m3/mol。
-
14、苯胺是一种无色油状液体,主要用于制造染料、药物和树脂等。利用水蒸气蒸馏法分离提纯粗苯胺(杂质为难以气化的物质)的装置如图所示。

实验操作:将粗苯胺加入仪器B中,向仪器A中加水,打开F,加热仪器A使水沸腾。同时对仪器B进行预热,关闭F,让水蒸气导入蒸馏装置,通入冷凝水,开始蒸馏。
回答下列问题:
(1)、仪器C的名称是;仪器E的作用是。(2)、如果加热A一段时间后发现漏加沸石,应该采用的补救操作是。(3)、水蒸气冷凝放热较多,为了提高冷凝效果可采取的措施是。(4)、蒸馏至时可停止蒸馏。(5)、将D中苯胺分离出来,需要用到的玻璃仪器有。(6)、已知混合物的蒸气总压等于外界大气压时,混合物开始沸腾。混合气体的总压等于各气体的分压之和,各气体的分压之比等于它们的物质的量之比。苯胺与水共沸时,苯胺的分压为5.6kPa,水蒸气的分压为95.7kPa,理论上每蒸出1g水同时蒸出苯胺的质量为g(计算结果保留2位有效数字);苯胺微溶于水,使水的蒸气压降低,则实际蒸出苯胺的质量(“偏大”“偏小”或“不变”)。 -
15、高锰酸钾在化工生产和环境保护等领域应用十分广泛。以软锰矿(主要成分是MnO2 , 含有Fe2O3和SiO2等杂质)为原料制备高锰酸钾的工艺流程如图:

回答下列问题:
(1)、基态Mn原子的价电子轨道表示式为。(2)、“焙烧”中有K2MnO4生成,该步骤主要反应的化学方程式为。(3)、若“焙烧”时未加入KClO3 , “水浸”后所得溶液中也含有K2MnO4 , 原因可能是。(4)、“水浸”时需要加热,其目的是。(5)、“滤渣2”含有MnO2和 , “歧化”过程中主要反应的离子方程式为。(6)、KMnO4可通过电解K2MnO4溶液的方法直接制得,相比“歧化法”,电解法的优点是。 -
16、实验测得0.1mol/LNaHCO3溶液的pH随温度升高的变化如图所示。

下列说法正确的是( )
A、由a点可知Ka1(H2CO3)•Ka2(H2CO3)>Kw B、a→b,HCO的水解程度减小 C、b→c,可能发生反应:2HCOCO+CO2↑+H2O D、a点溶液和d点溶液的c(OH-)相同 -
17、一水硫酸四氨合铜[Cu(NH3)4SO4•H2O]是一种易溶于水的晶体,可作高效安全的广谱杀菌剂,实验室制备流程如图:

下列说法错误的是( )
A、铜屑表面的油污可通过“碱煮水洗”去除 B、过程③中蓝色沉淀溶解,溶液变为绿色 C、过程④中加入的“溶剂X”可以是乙醇 D、玻璃棒摩擦的目的是加快结晶速率 -
18、已知反应S2O(aq)+2I-(aq)2SO(aq)+I2(aq),若起始向反应体系中加入含Fe3+的溶液,反应机理如图所示。下列说法正确的是( )
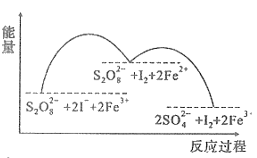 A、S2O中硫元素显+7价 B、反应速率与Fe3+浓度无关 C、由图可知氧化性:Fe3+>S2O D、若不加Fe3+ , 正反应的活化能比逆反应的小
A、S2O中硫元素显+7价 B、反应速率与Fe3+浓度无关 C、由图可知氧化性:Fe3+>S2O D、若不加Fe3+ , 正反应的活化能比逆反应的小 -
19、科学家近年发明了一种新型光电催化装置,它能将葡萄糖和CO2转化为甲酸盐,如图所示。光照时,光催化电极a产生电子(e-)和空穴(h+),图中的双极膜中间层中的H2O会解离产生H+和OH-。

下列说法错误的是( )
A、光催化电极a的反应为C6H12O6+12h++18OH-=6HCOO-+12H2O B、双极膜中间层中的H+在外电场作用下向催化电极b移动 C、理论上电路中转移4mole-时可生成2molHCOO- D、阳极区和阴极区的pH均减小 -
20、下列实验方案能达到实验目的的是( )
选项
实验目的
实验方案
A
探究葡萄糖的还原性
在一支试管中先加入2mL10%NaOH溶液,滴入5滴5%CuSO4溶液,再加入2mL10%葡萄糖溶液,加热。观察实验现象
B
检验苯中是否含有苯酚
在盛有苯和苯酚混合溶液的试管中滴加少量溴水。观察实验现象
C
探究不同盐的水解程度
用pH试纸分别测量等体积、等浓度的NaClO溶液和CH3COONa溶液的pH。比较大小
D
检验乙烯的还原性
在圆底烧瓶中加入乙醇和浓硫酸的混合溶液,并加入碎瓷片,迅速升温到170℃,将生成的气体通入高锰酸钾溶液中。观察实验现象
A、A B、B C、C D、D