相关试卷
-
1、氟锑酸(HSbF6)是石油重整中常用的催化剂,酸性比纯硫酸要强2×1019倍,被称为超强酸。实验室可通过SbCl5+6HF=HSbF6+5HCl制得,且HSbF6在HF中容易生成[H2F]+[SbF6]-。下列说法错误的是( )A、HF的电子式为
 B、[H2F]+的空间结构为V形
C、基态氯原子核外电子的运动状态有9种
D、基态Sb和F原子中电子占据能量最高的轨道形状相同
B、[H2F]+的空间结构为V形
C、基态氯原子核外电子的运动状态有9种
D、基态Sb和F原子中电子占据能量最高的轨道形状相同
-
2、对下列劳动项目的解释错误的是( )
选项
劳动项目
解释
A
用SO2漂白纸浆
SO2具有还原性
B
用铝制容器贮运浓硝酸
铝遇浓硝酸钝化
C
模具注入熔融钢水之前必须干燥
铁与H2O在高温下会反应
D
用固体管道疏通剂(主要成分为NaOH和铝粉)疏通管道
与铝粉和NaOH溶液反应产生气体有关
A、A B、B C、C D、D -
3、一种用氢气制备双氧水的反应原理如图所示,已知钯(Pd)常以正二价形式存在。下列有关说法正确的是( )
 A、H2、O2和H2O2都是非极性分子 B、反应①②③均为氧化还原反应 C、反应②中每产生1mol[PbCl2O2]2- , 转移2mol电子 D、[PbCl4]2-和HCl均为该反应的催化剂
A、H2、O2和H2O2都是非极性分子 B、反应①②③均为氧化还原反应 C、反应②中每产生1mol[PbCl2O2]2- , 转移2mol电子 D、[PbCl4]2-和HCl均为该反应的催化剂 -
4、金属M在潮湿的空气中会形成一层致密稳定的3M(XY)2•MZX3。X、Y、Z为短周期主族元素,X的原子序数是Y的8倍,基态X和Z的未成对电子数相同,M是人体的必需微量元素之一。1molMZX3含有60mol质子。下列说法正确的是( )A、3M(XY)2•MZX3中Z原子采用sp3杂化 B、同周期元素中第一电离能比X大的有3种 C、基态M原子核外电子排布式为[Ar]4s2 D、氢化物的沸点:X>Z
-
5、设NA为阿伏加德罗常数的值。下列说法正确的是( )A、9g羟基所含电子数目为10NA B、pH=13的NaOH溶液中含有的Na+数目为NA C、在含4molSi-O键的SiO2晶体中,氧原子数目为2NA D、0.5molNF3中孤电子对的数目为0.5NA
-
6、茶多酚是茶叶中多酚类物质的总称,具有抗癌、抗衰老等功能。茶叶的手工制作过程非常复杂:“采回的鲜茶叶,要及时、均匀地薄摊在洁净的竹匾上……要用火力均匀的木炭火在锅内手工翻炒、烘焙……”。下列有关说法正确的是( )A、“翻炒”时,木炭火的温度越高越好 B、用开水刚泡制的茶水pH=7 C、瓷器茶杯属于新型的无机非金属材料 D、茶多酚能有效清除人体的活性氧自由基,起到抗衰老作用
-
7、奥司他韦是目前治疗甲流的常用药物之一,其结构如图所示。下列有关该物质的说法错误的是( )
 A、该物质具有碱性 B、该物质在碱性条件下的水解产物有2种 C、该物质能使酸性高锰酸钾、溶液褪色 D、该物质可形成分子内氢键和分子间氢键
A、该物质具有碱性 B、该物质在碱性条件下的水解产物有2种 C、该物质能使酸性高锰酸钾、溶液褪色 D、该物质可形成分子内氢键和分子间氢键 -
8、下列化学用语表示正确的是( )A、中子数为16的磷原子: B、乙烯的空间填充模型
 C、氧原子核外电子轨道表示式:
C、氧原子核外电子轨道表示式: D、乙醇的键线式:
D、乙醇的键线式:
-
9、化学与人类生产、生活密切相关。下列有关物质用途的说法错误的是( )A、三聚氰胺可用作食品添加剂 B、使用聚四氟乙烯活塞的滴定管可以装碱性溶液 C、可以向牙膏中添加Na2PO3F、NaF和SrF2等预防龋齿 D、运输水果的过程中,可以在包装盒内加入浸泡过高锰酸钾溶液的硅藻土
-
10、空气中含量的控制和资源利用具有重要意义。(1)、利用高炉炼铁尾气中的制取有机物的过程如下:

相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率随电解电压的变化如图1所示:

图1
, 选择性。
“电解”在质子交换膜电解池中进行,生成的电极反应式为 , 当电解电压为时,生成和的选择性之比为。
(2)、利用铟氧化物催化制取的可能机理如图2所示,无催化活性,形成氧空位后具有较强催化活性,将固定比例的混合气体以不同流速通过装有催化剂的反应管,选择性、转化率随气体流速变化曲线如图3所示,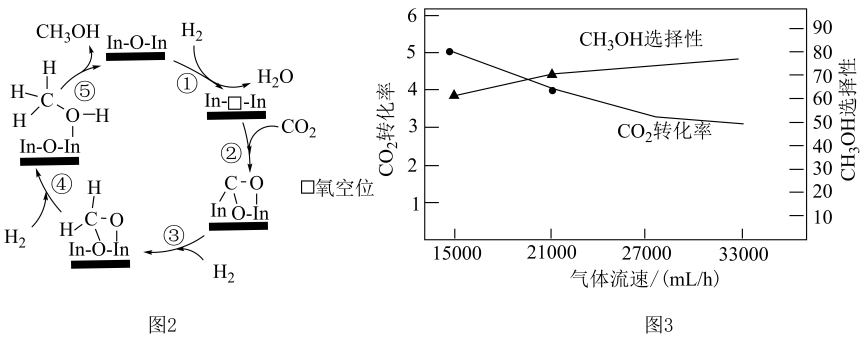
①图2中的反应每生成放出的热量,其热化学方程式为。
②若原料气中比例过低、过高均会减弱催化剂活性,原因是。
③制取时,同时发生反应 , 气体流速分别为和 , 相同时间内生成的质量,前者后者(选填“>”、“="或“<”);保持气体流速不变,反应管内温度从升高到 , 测得出口处和的物质的量均减小,可能的原因是。
-
11、以方铅矿(主要成分 , 含少量)和软锰矿(主要成分)为原料制备电池材料和 , 过程可表示为

已知:①
②
(1)、时,“协同浸取”生成和的离子方程式为;“协同浸取”时加入可避免生成沉积在矿石表面,其原因是。(2)、“沉降分铅”的目的是将滤液中的沉降为沉淀。沉降反应的平衡常数。(3)、络合萃取剂全氟聚醚-二(甲基吡啶)胺通过氮原子与形成配位键的方式萃取铅。已知氮原子的电子云密度越大配位能力越强,全氟聚醚-二(甲基吡啶)胺中氮原子和含氟基团相连使得配位能力下降,若在氮原子和含氟基团间引入基团配位能力会增强,其原因分别是。(4)、制备。(难溶于水的黑色晶体)可通过空气氧化制得,制备时溶液的温度和对的产率影响如图所示。请补充完整由净化后的含的滤液制备较纯净的的实验方案:取一定量的含的滤液于三颈烧瓶中, , 真空40干燥得产品。(必须使用的试剂:空气、蒸馏水、氨水、稀硝酸、溶液。)
-
12、化合物H是治疗胃癌的小分子靶向抗肿瘤药物,其合成路线如下:
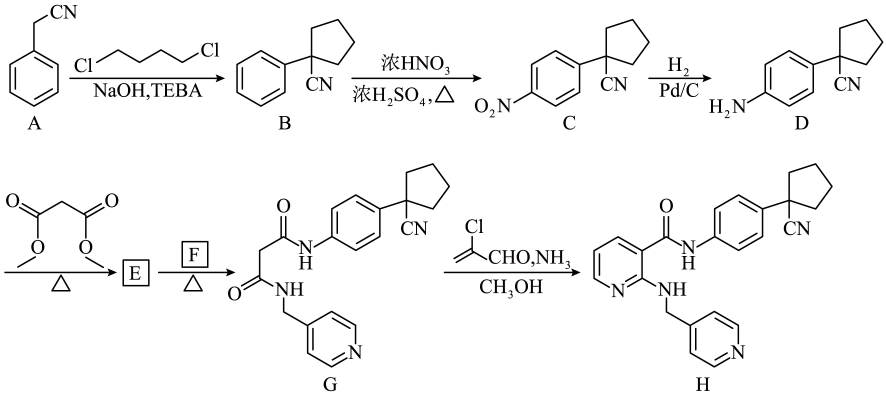 (1)、A分子中碳原子的杂化轨道类型有种。(2)、写出同时满足下列条件的C的一种同分异构体的结构简式:。
(1)、A分子中碳原子的杂化轨道类型有种。(2)、写出同时满足下列条件的C的一种同分异构体的结构简式:。①苯环上有4个取代基,能与溶液发生显色反应;
②核磁共振氢谱图中有3个峰。
(3)、的反应中均有生成,则的结构简式为。(4)、的反应中有一种与互为同分异构体的副产物生成,其结构简式为。(5)、写出以 、
、 、
、 和为原料,制备
和为原料,制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。 -
13、广泛用于冶金、化工行业,可制取多种含钒化合物。(1)、实验室制备氧钒(Ⅳ)碱式碳酸铵晶体,过程如下:

“还原”步骤中生成 , 反应的化学方程式为;若不加 , HCl也能还原生成和 , 分析反应中不生成的原因。
(2)、对制得的晶体进行含钒量的测定:称取样品,经过系列处理后将钒(Ⅳ)完全氧化,定容为溶液;量取溶液,加入指示剂,用的标准溶液滴定至终点,滴定过程中反应为;平行滴定4次,消耗标准溶液的体积分别为 , 则样品中钒元素的质量分数为(写出计算过程,结果保留两位小数)。(3)、时,将氧钒碱式碳酸铵晶体与反应制备共价晶体 , 一段时间后,固体质量不再变化,经检测仍有氧钒碱式碳酸铵剩余,可能的原因是。(4)、可溶于强酸强碱,不同、不同钒元素浓度时,价存在形态如题图所示:
①将溶解在烧碱溶液中,剩余溶液的 , 反应的离子方程式为。
②具有对称结构,其结构式可表示为。
-
14、二甲醚和水蒸气制氢气可作为燃料电池的氢能源,发生的主要反应如下:
反应Ⅰ
反应Ⅱ
反应Ⅲ
在恒压下,将一定比例的二甲醚和水蒸气混合后,以一定流速通过装有催化剂的反应器,反应相同时间测得的实际转化率、实际选择性与平衡选择性随温度的变化如图所示.的选择性 . 下列说法不正确的是( )
 A、曲线表示实际转化率随温度的变化 B、时,反应Ⅱ的速率大于反应Ⅲ的速率 C、适当增加 , 有利于提高的产率 D、一定温度下,若增大压强,的平衡产量不变
A、曲线表示实际转化率随温度的变化 B、时,反应Ⅱ的速率大于反应Ⅲ的速率 C、适当增加 , 有利于提高的产率 D、一定温度下,若增大压强,的平衡产量不变 -
15、室温下,体系中各含碳微粒的物质的量分数与的关系如图1所示.在的体系中,研究在不同时的可能产物,与的关系如图2所示,曲线Ⅰ的离子浓度关系符合 , 曲线Ⅱ的离子浓度关系符合。

下列说法正确的是( )
A、由点可求得 B、的体系中: C、点的体系中,发生反应 D、点的体系中, -
16、利用碳氮化反应 , 可将转化为 , 再进一步还原得到金属钛,下列说法正确的是( )A、碳氯化反应在高温下不能自发进行 B、加压、降温均可增大生成的速率 C、反应中每消耗 , 转移电子的数目约为 D、将与粉碎并混合均匀后反应可提高的平衡转化率
-
17、室温下,下列实验探究方案能够边到探究目的的是( )
选项
探究方案
探究目的
A
将溴丁烷与的乙醇溶液混合后加热,生成的气体通入的溶液中,观察现象
溴丁烷能否发生消去反应生成烯烃
B
将气体通入紫色石蕊溶液中,观察溶液颜色变化
是否具有漂白性
C
向饱和溶液中通入足量气体,观察现象
比较与在水中溶解度的大小
D
向溶液中滴加淀粉,再通入气体,观察现象
比较与氧化性的强弱
A、A B、B C、C D、D -
18、药物沃塞洛托的重要中间体的合成路线如图所示.下列说法不正确的是( )

A 最多能与反应
A、分子中所有原子有可能共平面 B、的分子组成相差 C、用红外光谱可确证存在不同的官能团 -
19、在指定条件下,下列选项所示的物质间转化能实现的是( )A、 B、 C、 D、
-
20、下列物质的结构、性质、用途具有对应关系的是( )A、浓硫酸具有脱水性,可用于干燥 B、具有强氧化性,可用作火箭助燃剂 C、冰晶石微溶于水,可用作电解铝工业的助熔剂 D、分子之间形成氢键,的热稳定性比的高