相关试卷
-
1、日本福岛核废水排海引起舆论风波,核废水中不只含有放射性氚,真正具有伤害性的,还有6种放射性元素,分别是碘、铯和铯、碳、钴和锶。下列叙述正确的是( )A、原子所含中子数与质子数之差为25 B、和互称为同素异形体 C、铯的核外电子数为65 D、和的核外电子数之差为4
-
2、下列化学用语正确的是( )A、的电子式
 B、次氯酸的结构式:
C、的电子式
B、次氯酸的结构式:
C、的电子式 D、的结构示意图
D、的结构示意图
-
3、中华文化源远流长、博大精深。下列说法不正确的是( )A、先秦文献《考工记》记录了六类青铜器物的合金成分配比,合金的熔点一般比纯金属的低 B、《本草经集注》中记载了区分硝石()和朴硝()的方法:“以火烧之,紫青烟起,乃真硝石也”,二者可以利用“焰色试验”区分 C、《神农本草经》中提到“白青[]得铁化为铜”,其中白青属于碱 D、“蜡炬成灰泪始干”、“爆竹声中一岁除”中均涉及氧化还原反应
-
4、规范、科学处置废旧锂离子电池具有重要的环保意义和经济价值。废旧锂离子电池的正极材料主要含有及少量Al、Fe等,处理该废料的一种工艺流程如图所示。

已知:①难溶于水。
②相关金属离子形成氢氧化物沉淀的pH如下表所示。
开始沉淀的pH
2.7
7.6
7.0
完全沉淀的pH
3.7
9.6
9.0
③的溶解度(S)随温度(T)的变化曲线如下图所示。
 (1)、化合物中钴元素的化合价为价。(2)、“放电处理”有助于锂元素在正极的回收,电池放电时的总反应为 , 则此时正极的电极反应式为。(3)、“碱溶”过程主要发生的离子方程式为。(4)、为提高“酸溶”的速率,可采取的措施有(任写一条)。(5)、“调pH”时,用氨水调节pH的范围为。(6)、“沉钴”过程中对产生的沉淀洗涤的实验操作为。(7)、“沉锂”后,洗涤所得沉淀要使用(填“热水”或“冷水”)。
(1)、化合物中钴元素的化合价为价。(2)、“放电处理”有助于锂元素在正极的回收,电池放电时的总反应为 , 则此时正极的电极反应式为。(3)、“碱溶”过程主要发生的离子方程式为。(4)、为提高“酸溶”的速率,可采取的措施有(任写一条)。(5)、“调pH”时,用氨水调节pH的范围为。(6)、“沉钴”过程中对产生的沉淀洗涤的实验操作为。(7)、“沉锂”后,洗涤所得沉淀要使用(填“热水”或“冷水”)。 -
5、甲烷在日常生活及有机合成中用途广泛,某实验小组研究甲烷在高温下气相裂解反应的原理及其应用。
已知:①
②
(1)、裂解反应的。(2)、在某密闭容器中投入 , 在不同条件下发生反应:。实验测得平衡时的物质的量随温度、压强的变化如图所示。
①M点时,的转化率为;温度:(填“>”、“<”或“=”)。
②M、N、Q三点的平衡常数由大到小的顺序为。
③M点对应的压强平衡常数(以分压表示,分压=总压×物质的量分数,整理出含的最简表达式)。
④若向M点对应平衡体系中再充入、和 , 此时平衡向(填“正反应”或“逆反应”)方向移动。
(3)、在恒温恒容条件下,充入一定量 , 发生反应。下列能判断该反应达到平衡状态的是(填字母)。a.
b.的体积分数不再改变
c.混合气体的密度不再改变
d.同一时间内,消耗 , 生成
-
6、是高中化学中常见铵盐,试运用所学相关的化学知识解答下列问题。
已知:ⅰ.25℃时,的
ⅱ.氯化铵的抗碱容量是指用溶液滴定溶液至时,单位质量的所消耗的物质的量,即
(1)、的电子式。(2)、溶液呈性(填“酸”或“碱”),现有溶液,则该溶液在25℃时的pH为。(3)、某化学小组测定固体抗碱容量 , 实验步骤如下:a.配置溶液;
b.称取固体,溶于水中,用上述溶液滴定至。
①步骤a需要称量固体为g。
②步骤b需要用到下图所示仪器中的(填名称)。
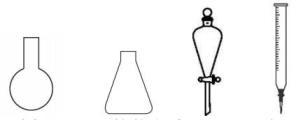
③步骤b消耗的体积为ymL,则。
(4)、混合溶液具有抗碱能力。向该溶液中加入少量 , 溶液的pH变化不大。现有混合溶液(物质的量之比为),对于该混合溶液的下列叙述中正确的是____。A、常温下,该混合溶液呈酸性 B、溶液中离子浓度大小关系为: C、溶液中离子浓度存在恒等式: D、溶液中微粒间满足: -
7、滴定实验是化学学科中最重要的定量实验之一。常见的滴定实验有酸碱中和滴定、氧化还原反应滴定、沉淀滴定等等。
Ⅰ.用的NaOH溶液分别滴定的盐酸和醋酸溶液各。滴定过程中溶液pH随溶液体积变化的两条滴定曲线如图所示:
 (1)、滴定醋酸的曲线是(填“Ⅰ”或“Ⅱ”)。(2)、和的关系:(填“>”、“=”或“<”)。(3)、Ⅱ.获取安全的饮用水一直以来都是人们关注的重要问题,自来水厂经常用氯气进行杀菌,某化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量,实验步骤如下:
(1)、滴定醋酸的曲线是(填“Ⅰ”或“Ⅱ”)。(2)、和的关系:(填“>”、“=”或“<”)。(3)、Ⅱ.获取安全的饮用水一直以来都是人们关注的重要问题,自来水厂经常用氯气进行杀菌,某化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量,实验步骤如下:①取水样于锥形瓶中,加入溶液(足量),滴入2~3滴淀粉溶液。
②将自己配制的标准溶液(显碱性)装入滴定管中,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:
试回答下列问题:
①滴定前装有标准液的滴定管排气泡时,应选择下图中的(填标号,下同)。
A.
 B.
B. C.
C. D.
D.
②若用滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积。
A. B. C. D.
(4)、步骤①发生反应的离子方程式为。(5)、达到滴定终点的现象是。(6)、实验测得游离态氯的浓度比实际浓度偏大,造成误差的原因可能是____。A、锥形瓶水洗后直接装待测水样 B、配制标准溶液定容时,加水超过刻度线 C、装标准溶液的滴定管水洗后没有润洗 D、滴定到达终点时,俯视读出滴定管读数 -
8、下列实验操作能达到实验目的的是( )。
选项
实验目的
实验操作
A
比较和溶度积大小
向的硝酸银溶液中先滴加2~3滴浓度为的溶液,再滴加2~3滴相同浓度的KI溶液,观察生成沉淀的颜色
B
探究化学反应是否可逆
向的KI溶液中滴加2滴的溶液,充分反应后,滴入2滴的溶液,观察现象
C
探究浓度对盐类水解平衡的影响
向滴有酚酞的碳酸钠溶液中加入等体积蒸馏水,观察现象
D
比较和酸性强弱
用pH试纸测定溶液和溶液的pH
A、A B、B C、C D、D -
9、对于下列反应,其反应过程的能量变化如图所示:

编号
反应
平衡常数
反应热
反应①
反应②
反应③
下列说法不正确的是( )。
A、 B、 C、增大压强,反应①②③的反应速率均加快 D、升高温度,增大,减小、不变 -
10、某反应可有效降低汽车尾气污染物的排放,其反应热。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法不正确的是( )。
 A、三个基元反应中只有①是吸热反应 B、
A、三个基元反应中只有①是吸热反应 B、 是该反应的中间产物
C、该过程的总反应为
D、
是该反应的中间产物
C、该过程的总反应为
D、
-
11、利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的是( )。
 A、b电极为电池正极 B、电池工作时,海水中的向a电极移动 C、电池工作时,紧邻a电极区域的海水呈强碱性 D、每消耗 , 就有的溶解氧(已换算标准状况)参与反应
A、b电极为电池正极 B、电池工作时,海水中的向a电极移动 C、电池工作时,紧邻a电极区域的海水呈强碱性 D、每消耗 , 就有的溶解氧(已换算标准状况)参与反应 -
12、下列各离子组在指定的溶液中能够大量共存的是( )。A、无色溶液中:、、、 B、含有的溶液中:、、、 C、的溶液中:、、、 D、由水电离出的的溶液中:、、、
-
13、设为阿伏加德罗常数的值,下列说法正确的是( )。A、一定条件下,与足量反应生成数目为 B、将溶于水,溶液中与数目之和为 C、室温下,的溶液中数目为 D、室温下,的溶液中水电离产生的数目为
-
14、常温下,下列事实不能说明某一元酸HX是弱酸的是( )。A、溶液 B、和反应,生成HX C、溶液比硝酸导电能力弱 D、溶液与溶液恰好中和
-
15、下列关于焓判据和熵判据的说法中,正确的是( )。A、吸热的自发过程一定为熵增加的过程 B、的反应均是自发进行的反应 C、碳酸钙分解为吸热反应,该反应在任何温度下都不能自发进行 D、大于0的反应一定不能发生
-
16、下列四组物质的溶液加热蒸干、灼烧、所得固体的成分不相同的是( )。
①、 ②、 ③、 ④、
A、①② B、②③ C、③④ D、①④ -
17、考古学家在江苏建湖发现一处钱币窖藏遗存,出土钱币约1.5吨。除少量的唐代开元通宝钱币外,大部分为宋代钱币。钱币主要成分是铜合金。下列叙述错误的是( )。A、钱币表面绿色物质的主要成分是 B、钱币中铜在地下主要发生析氢腐蚀 C、钱币在窖藏中发生电化学腐蚀时铜被氧化 D、保护钱币措施有保持干燥、涂保护层等
-
18、劳动有利于“知行合一”,下列劳动项目与所述的化学知识没有关联的是( )。
选项
劳动项目
化学知识
A
环保行动:用除去废水中的
溶度积:
B
学农活动:用小苏打作发泡剂烘焙面包
受热易分解产生气体
C
家务劳动:用食醋清洗水壶内的水垢
醋酸的酸性比碳酸强
D
帮厨活动:用热的纯碱溶液去除厨房的油污
油脂直接与纯碱发生化学反应
A、A B、B C、C D、D -
19、某温度下,A和B以物质的量之比为充入某密闭容器中,发生的反应。C的物质的浓度随反应时间(t)的变化如下表。下列说法中正确的是( )。
2
4
6
8
10
12
C的浓度/
0.22
0.36
0.42
0.46
0.46
0.46
A、在内,平均反应速率为 B、前正反应速率小于逆反应速率 C、后反应物消耗完,反应停止 D、在反应过程中转化率均有 -
20、下列依据热化学方程式得出的结论正确的是( )。A、已知 ; , 则 B、已知 , 则氢气的燃烧热为 C、已知 , 则含的稀溶液与稀醋酸完全中和,放出的热量小于 D、已知P(白磷,s)=P(红磷,s) , 则白磷比红磷稳定