相关试卷
-
1、下列实验装置使用不正确的是 ( )
 A、图①装置用于标准酸溶液滴定未知碱溶液 B、图②操作可排出盛有AgNO3溶液滴定管尖嘴内的气泡 C、图③装置用于测定中和反应的反应热 D、④装置盐桥中阳离子向CuSO4溶液中迁移
A、图①装置用于标准酸溶液滴定未知碱溶液 B、图②操作可排出盛有AgNO3溶液滴定管尖嘴内的气泡 C、图③装置用于测定中和反应的反应热 D、④装置盐桥中阳离子向CuSO4溶液中迁移 -
2、氯化铁是一种重要的盐,下列说法不正确的是( )A、铁元素位于d区 B、氯化铁溶液呈酸性 C、氯化铁可用于净水 D、铁离子价层电子排布图为3d5
-
3、下列物质属于强电解质的是( )A、CO2 B、盐酸 C、冰醋酸 D、BaSO4
-
4、卤沙唑仑W是一种抗失眠药物,在医药工业中的一种合成方法如图:

已知:ⅰ.

ⅱ.
 (1)、A的化学名称是。(2)、B含有的官能团名称为。(3)、反应②的反应类型是。(4)、反应③中NaOH的作用是。写出反应③的化学方程式:。(5)、Y的结构简式为。(6)、写出W的结构简式:。(7)、C同分异构体中,含有苯环并能发生银镜反应的共有种。(不考虑立体异构)
(1)、A的化学名称是。(2)、B含有的官能团名称为。(3)、反应②的反应类型是。(4)、反应③中NaOH的作用是。写出反应③的化学方程式:。(5)、Y的结构简式为。(6)、写出W的结构简式:。(7)、C同分异构体中,含有苯环并能发生银镜反应的共有种。(不考虑立体异构) -
5、全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:(1)、5G芯片主要材质是高纯硅。基态Si原子核外电子的空间运动状态有种,若其电子排布式表示为违背了。(2)、高纯硅制备过程中会有等中间产物生成。沸点:(填“>”或“<”)。(3)、复兴号高铁车体材质用到等元素。
①的一种配合物化学式为 , 下列说法正确的是(填字母标号)。
A.与原子配位时,提供孤电子对的是原子
B.Mn原子的配位数为6
C.中键与键数目之比为
D.中C原子的杂化类型为
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测比的分解温度(填“高”或“低”),解释原因
(4)、时速600公里的磁浮列车需用到超导材料。超导材料TiN具有型结构(如图),晶胞参数(晶胞边长)为 , 其中阴离子采用面心立方最密堆积方式,则为D,该氮化钛的密度(列出计算式即可)。
-
6、二氧化碳资源化利用是科研的热点,甲烷化技术是重要途径之一,其相关反应如下:
ⅰ.
ⅱ.;
ⅲ.积炭反应: ;
ⅳ.。
 (1)、CO歧化积炭反应在低温下能自发进行,则0(填“>”或“<”)。(2)、研究表明三种双金属合金团簇均可用于催化反应ⅰ,在催化剂表面涉及多个基元反应,其中在不同催化剂作用下裂解的反应历程如图甲所示。
(1)、CO歧化积炭反应在低温下能自发进行,则0(填“>”或“<”)。(2)、研究表明三种双金属合金团簇均可用于催化反应ⅰ,在催化剂表面涉及多个基元反应,其中在不同催化剂作用下裂解的反应历程如图甲所示。①该历程分步进行,甲烷逐步脱氢过程中活化能最大的反应步骤是:(用化学方程式表示)。
②双金属合金团簇具有良好的抗积碳作用,有效抑制碳积沉对催化剂造成的不良影响,请结合图甲解释原因:。
(3)、加氢制甲醇也是资源化利用的重要途径之一,其反应原理为。投料比时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 , 在时随压强变化关系及在时随温度()的曲线变化如图乙所示:①图中对应等温过程的曲线为。
②图中两点的速率(填“>”、“<”或“=”)
③当时,的平衡转化率为;为210℃时,各物质的平衡分压表示反应的平衡常数(列出计算式)。
-
7、绿矾是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为 , 此外还含有少量 , 表面有少量油脂)制取绿矾,并分离出铜,并测定绿砜中的结晶水含量,他们的实验过程如下:
Ⅰ.制备绿矾并分离出铜
 (1)、加入热碳酸钠溶液的目的是。(2)、针对上述实验过程,某同学提出了以下几种观点,其中错误的是(填序号)。
(1)、加入热碳酸钠溶液的目的是。(2)、针对上述实验过程,某同学提出了以下几种观点,其中错误的是(填序号)。a.溶液A中至少含有3种溶质
b.由于接触空气,混合物C中可能含有
c.操作X用到的仪器可能有玻璃棒、烧杯、分液漏斗等
(3)、操作Y包括加热浓缩、冷却结晶、抽滤(减压过滤)等,不采用蒸发结晶的主要原因是 , 抽滤的优点是。(4)、Ⅱ.测定制得绿矾中结晶水含量将石英玻璃管(带两端开关和)(设为装置)称重,记为 , 将样品装入石英玻璃管中,再次将装置称重,记为 , 按如图连接好装置进行实验。

仪器B的名称为。
(5)、将下列实验操作步骤正确排序(填标号);重复上述操作步骤,直至A恒重,记为。①启动电加热器,加热②关闭电加热器③冷却到室温④关闭和 , 称量⑤打开和 , 缓缓通入
(6)、根据实验所得数据计算,(列式表示)。(7)、若加热时,石英管A中产生红色固体,会使的值(填“偏大”、“偏小”或“无影响”,下同);若通过测量加热前后B管的质量变化确定 , 会使其值。 -
8、金属镓被称为“电子工业脊梁”,GaN凭借其出色的功率性能、频率性能以及散热性能,应用于技术中以及充电行业。让高功率、更快速充电由渴望变为现实。一种以粉煤灰(主要含有等杂质)为原料,制备高纯三甲基镓的工艺流程如下:

已知:①镓性质与铝相似,金属活动性介于锌和铁之间;②常温下,相关元素可溶性组分物质的量浓度与的关系如下图所示。当溶液中可溶组分浓度时,可认为已除尽。
 (1)、“焙烧”过程中,将转化为(填化学式)。(2)、“碱浸”操作时,为加快浸取速率可采取的方法是(任写一种即可)。“滤渣1”主要成分为。(3)、与过量发生反应的离子方程式为。(4)、常温下,反应的平衡常数的值为。(5)、“电解”可得金属 , 写出阴极电极反应式。(6)、工业上以机化合物与作为原料,在高温下反应生成 , 该反应的化学方程式为。
(1)、“焙烧”过程中,将转化为(填化学式)。(2)、“碱浸”操作时,为加快浸取速率可采取的方法是(任写一种即可)。“滤渣1”主要成分为。(3)、与过量发生反应的离子方程式为。(4)、常温下,反应的平衡常数的值为。(5)、“电解”可得金属 , 写出阴极电极反应式。(6)、工业上以机化合物与作为原料,在高温下反应生成 , 该反应的化学方程式为。 -
9、在悬浊液中滴加氨水[浓度以计],存在平衡关系:
;
;
,
平衡常数分别为与的关系如图所示(其中代表或)。下列说法错误的是( )
 A、时,溶液中 B、加入少量固体后,X点坐标下移 C、随浓度增大,也增大 D、X点对应的
A、时,溶液中 B、加入少量固体后,X点坐标下移 C、随浓度增大,也增大 D、X点对应的 -
10、某实验小组依据反应:设计如图原电池,探究对氧化性的影响。测得电压与pH的关系如图,下列有关叙述错误的是( )
 A、时,氧化性 B、时盐桥中向右移 C、调节可以改变反应的方向 D、时,正极的电极反应为
A、时,氧化性 B、时盐桥中向右移 C、调节可以改变反应的方向 D、时,正极的电极反应为 -
11、实验装置不能达到实验目的的是( )




A.验证浓硫酸的吸水性
B.提纯乙酸乙酯
C.制取少量碳酸钙
D.制取少量
A、A B、B C、C D、D -
12、为短周期主族元素,的一种同位素具有放射性,可用来断定古生物体死亡的年代。X、Y的某种同位素之间的转化如下:。由组成的双原子分子和Y常见单质分子所含电子数相同。下列说法错误的是( )A、元素非金属性 B、M与其它三种元素均可形成两种或两种以上的二元化合物 C、能组成离子化合物 D、简单氢化物的热稳定性
-
13、催化作用下,发生反应的历程如图所示。下列说法正确的是( )
 A、改变反应途径,提高了单位时间原料转化率 B、反应过程中Mo形成的共价键数目始终保持不变 C、总反应为 D、如果原料为乙二醇,则主要有机产物是乙醛和乙烯
A、改变反应途径,提高了单位时间原料转化率 B、反应过程中Mo形成的共价键数目始终保持不变 C、总反应为 D、如果原料为乙二醇,则主要有机产物是乙醛和乙烯 -
14、碳酸甘油酯为生物基化学品,具有无污染可降解等特性,应用广泛,其中一种合成方法如图所示。下列说法正确的是( )
 A、碳酸丙烯酯分子中碳原子一定共面 B、环氧丙烷生成碳酸丙烯酯的反应是取代反应 C、碳酸甘油酯在水中的溶解性比碳酸丙烯酯强 D、可采用1,2-丙二醇与浓硫酸共热得到纯净的丙烯
A、碳酸丙烯酯分子中碳原子一定共面 B、环氧丙烷生成碳酸丙烯酯的反应是取代反应 C、碳酸甘油酯在水中的溶解性比碳酸丙烯酯强 D、可采用1,2-丙二醇与浓硫酸共热得到纯净的丙烯 -
15、《中国诗词大会》不仅弘扬了中国传统文化,还蕴含着许多化学知识,下列分析正确的是( )A、“爆竹声中一岁除,春风送暖入屠苏”,爆竹的燃放不涉及氧化还原反应 B、绘制“山水画”所用的纸和墨的主要成分都是有机物 C、“日照香炉生紫烟,遥看瀑布挂前川”,“紫烟”指“香炉”中碘升华现象 D、“朝坛雾卷,曙岭烟沉”,雾产生丁达尔效应是胶体粒子对光的散射
-
16、被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,回答下列问题:
 (1)、进入的电极为极。(2)、电池工作时:溶液中的向(填“正极”或“负极”)迁移,通(填“”或“”)一极的电势较低。(3)、写出电池工作时的负极反应式:。(4)、若电池工作时转移0.01mol电子,理论上消耗标准状态下。(5)、该电池在工作过程中,电解液的pH将(填“不变”、“变大”或“变小”),用该电池电解水,其阴极的电极反应式。(6)、若将此燃料电池改成以和为原料进行工作时,正极极反应式为:。
(1)、进入的电极为极。(2)、电池工作时:溶液中的向(填“正极”或“负极”)迁移,通(填“”或“”)一极的电势较低。(3)、写出电池工作时的负极反应式:。(4)、若电池工作时转移0.01mol电子,理论上消耗标准状态下。(5)、该电池在工作过程中,电解液的pH将(填“不变”、“变大”或“变小”),用该电池电解水,其阴极的电极反应式。(6)、若将此燃料电池改成以和为原料进行工作时,正极极反应式为:。 -
17、水是生命的源泉、工业的血液、城市的命脉。河水是主要的饮用水源,污染物通过饮用水可宵接毒害人体,也可通过食物链和灌溉农田间接危及健康。请回答下列问题:(1)、纯水在100℃时,pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=mol·L-1。(2)、25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为。(3)、体积均为100mLpH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则相同温度时,HX的电离平衡常数(填“大于”或“小于”或“等于”)CH3COOH的电离平衡常数,理由是。
 (4)、电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
(4)、电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:化学式
电离常数(25℃)
HCN
K=4.9×10-10
CH3COOH
K=1.8×10-5
H2CO3
K1=4.3×10-7、K2=5.6×10-11
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三种溶液的pH由大到小的顺序为。
②向NaCN溶液中通入少量的CO2 , 发生反应的化学方程式为。
(5)、25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=mol·L-1(填精确值)。 -
18、甲醇是重要的化工原料,发展前景广阔。研究表明,二氧化碳与氢气反应可以合成甲醇,反应如下:(1)、反应的平衡常数表达式为K=。(2)、有利于提高平衡时转化率的措施有(填字母)。
a.使用催化剂
b.加压
c.增大和的初始投料比
(3)、研究温度对甲醇产率的影响时发现,在210~290℃,保持原料气中和的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的∆H0(填“>”“=”或“<”),依据是。 (4)、电子式 , 分子空间构型 , 属于分子(填极性或非极性)。
(4)、电子式 , 分子空间构型 , 属于分子(填极性或非极性)。 -
19、乙酸俗称醋酸,因是醋的主要成分而得名,是一种重要的化工原料。(1)、纯的无水乙酸常温下是无色液体,低于16.6℃凝结为类似冰一样的晶体,又称为冰醋酸。一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,加水前导电能力接近零的原因是;a、b、c三点对应的溶液中,由大到小的顺序是。
 (2)、t℃时,的 , 0.010mol/L的醋酸溶液中 , pH=。(lg2=0.3)(3)、为了测定某醋酸中的浓度,某学习小组进行了如下实验:取20.00mL待测溶液,用0.1000mol/LNaOH标准溶液滴定。
(2)、t℃时,的 , 0.010mol/L的醋酸溶液中 , pH=。(lg2=0.3)(3)、为了测定某醋酸中的浓度,某学习小组进行了如下实验:取20.00mL待测溶液,用0.1000mol/LNaOH标准溶液滴定。①滴定加入的指示剂应是(选填“甲基橙”或“酚酞”)。滴定终点的颜色变化为。
②滴定操作测得数据记录如下:
测定次数
滴定前读数/mL
滴定后读数/mL
第1次
0.20
20.14
第2次
0.12
19.98
第3次
0.00
18.30
第4次
0.00

的读数如上图所示,则mL,根据以上实验数据,所测醋酸的浓度是mol/L。
③上述实验中,当其它操作正确时,下列操作一定会造成测定结果偏高的是(填字母)。
A.待装NaOH标准溶液的滴定管用蒸馏水洗净后,未用标准溶液润洗
B.锥形瓶用蒸馏水洗净后,直接盛装待测液
C.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛NaOH标准溶液的滴定管,滴定前尖嘴部分有气泡,滴定后无气泡
④25℃下,用酸式滴定管量取25.00mL未知浓度的醋酸溶液,放入烧杯中,并放入磁力搅拌子,开启磁力搅拌器,往滴数传感器的滴定管中注入一定量的1.00mol/LNaOH溶液,通过数字化实验,计算机绘制出溶液pH随NaOH溶液体积变化的曲线如图。酸碱刚好完全反应时对应曲线上的点。

-
20、下列装置中能构成原电池产生电流的是( )A、
 B、
B、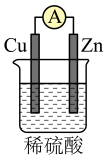 C、
C、 D、
D、