相关试卷
-
1、下列表示不正确的是( )A、质子数为92、中子数为146的U原子: B、HClO的电子式:
 C、
C、 的名称:2,2,4-三甲基己烷
D、H2S的价层电子对互斥(VSEPR)模型:
的名称:2,2,4-三甲基己烷
D、H2S的价层电子对互斥(VSEPR)模型:
-
2、工业上常用NaOH溶液吸收NO2 , 发生反应: , 下列说法不正确的是( )A、NaNO3是强电解质 B、NaNO2有毒,不可用于食品添加剂 C、N元素位于元素周期表p区 D、NaNO2溶液中通入O2 , 溶液pH降低
-
3、材料是人类赖以生存和发展的物质基础,下列材料主要成分不属于新型无机非金属材料的是( )A、水泥 B、石英光导纤维 C、氮化铝陶瓷 D、石墨烯
-
4、M为治疗偏头痛的药物主要成分,其合成路线如下:

已知:
I. II.
 (1)、有机物A的官能团名称为。(2)、有机物D的结构简式为。(3)、下列说法正确的是____。A、化合物C可以发生加成,取代反应 B、D到E的过程中KOH的作用是做催化剂 C、化合物M的分子式是 D、化合物G与氢气完全加成后有两个手性碳原子(4)、写出E→F的化学方程式。(5)、结合上述信息,写出以苯甲醇为原料,选择合适的试剂制备
(1)、有机物A的官能团名称为。(2)、有机物D的结构简式为。(3)、下列说法正确的是____。A、化合物C可以发生加成,取代反应 B、D到E的过程中KOH的作用是做催化剂 C、化合物M的分子式是 D、化合物G与氢气完全加成后有两个手性碳原子(4)、写出E→F的化学方程式。(5)、结合上述信息,写出以苯甲醇为原料,选择合适的试剂制备 的合成路线。(无机试剂任选) (6)、写出化合物C同时符合下列条件的同分异构体的结构简式
的合成路线。(无机试剂任选) (6)、写出化合物C同时符合下列条件的同分异构体的结构简式①分子中含有一个苯环;②核磁共振氢谱和红外光谱表明,分子中共有4种不同化学环境的氢原子,且峰面积比为6:2:2:2,只有一个-NO2。
-
5、清凉茶酸乙酯()是一种消毒杀菌剂,对细菌霉菌等有灭活作用。通过酯化反应制备清凉茶酸乙酯的方法如下,实验装置(部分夹持装置省略)如图所示。
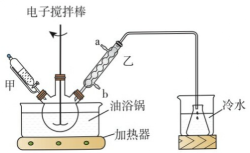
Ⅰ.在三颈烧瓶中加入5.6g清凉茶酸,4.6g乙醇,环己烷,少量浓硫酸等。
Ⅱ.油浴加热,控制温度为110℃,并不断搅拌,一段时间之后停止加热和搅拌。
Ⅲ.反应混合物冷却至室温,进行操作X
Ⅳ.在滤液中加入5%的小苏打溶液,洗涤,至混合液pH=7左右,再用蒸馏水洗涤。
V.将洗涤后混合液加入分液漏斗,进行分液。
Ⅵ.在分液后的有机层加入干燥剂,振荡,静置,过滤。
Ⅶ.对滤液进行蒸馏,收集一定温度的馏分,得到5.4mL纯净的清凉茶酸乙酯。
已知部分物质的性质如下:
沸点/℃
密度/(g·cm-3)
水溶性
备注
乙醇
78
0.789
混溶
清凉茶酸
228
1.204
易溶
清凉茶酸乙酯
195
0.926
难溶
环己烷
80.7
0.780
难溶
挥发过程中可带出较多的水
(1)、仪器甲的名称为(2)、写出实验中三颈烧瓶中发生的主要反应 , 其中环己烷的作用是。(3)、加热搅拌过程中忘加沸石,正确的操作是。(4)、下列有关该实验过程,正确的是____。A、乙中的进水口为a B、操作X使用的玻璃仪器有玻璃棒,漏斗,烧杯 C、加入小苏打是为了中和混合物中的酸性物质 D、分液后的有机层加入碱石灰干燥(5)、计算该制备实验的产率:(保留三位有效数字)。 -
6、NOx是大气主要污染物。有效去除大气中的NOx是环境保护的重要课题。
已知:的反应过程分为两步:
第一步:
第二步:
(1)、一定温度下,反应的平衡常数表达式是(用 , , , 表示)。(2)、将H2、NO、O2按体积之比为3:2:1充入恒温恒压(200℃,100Kpa)容器中,发生反应。达到平衡时,N2的体积分数为0.1。①平衡时,NO的转化率为 , 平衡常数=(以平衡分压表示,平衡分压=平衡时总压×平衡时的物质的量分数)。
②已知该反应ΔH<0,初始温度、压强和反应物的用量均相同,下列四种容器中NO的转化率最高的是。( )
A.恒温恒容容器 B.恒温恒压容器
C.恒容绝热容器 D.恒压绝热容器
③该反应需选择合适的催化剂进行,分别选用A,B,C三种不同的催化剂进行实验,所得结果如图所示(其它条件相同),则实际生产中适宜选择的催化剂是 , 理由为。
 (3)、用稀硝酸可以吸收NOx得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的反应式。
(3)、用稀硝酸可以吸收NOx得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的反应式。 -
7、氨气的用途非常广泛,下列是氨气的部分转化关系图。
 (1)、混合物A的成分为(用化学式表示)。(2)、N2H4又称联氨,为二元弱碱,不如氨气稳定。
(1)、混合物A的成分为(用化学式表示)。(2)、N2H4又称联氨,为二元弱碱,不如氨气稳定。①从分子结构角度分析,N2H4不如氨气稳定的原因是。
②N2H4在水中的电离与氨相似;25℃时,N2H4第一步电离平衡常数的值为。
(已知: )
(3)、NH3在无水环境下与CO2反应生成化合物B(不稳定),继续与NH3反应生成C。已知化合物C中含有铵根离子,可完全水解,其水解产物有NH4HCO3 , 下列说法正确的是____。A、化合物B的化学式为NH2COOH B、化合物B属于氨基酸 C、化合物C水解生成两种盐 D、化合物C可用于制备尿素(4)、实验中在加热条件下,通入过量的NH3与CuO反应,请设计实验验证尾气中比较活泼的两种气体。 -
8、硫及其化合物在生活、生产中有着广泛的应用。

图1
(1)、基态硫原子的价层电子轨道表示式是。(2)、S单质的常见形式为S8 , 其环状结构如图1所示,其中S原子的杂化方式是。(3)、下列说法正确的是____A、H2S分子的空间构形是直线型 B、六氟化硫(SF6)中心原子的杂化方式为sp3d2 C、第一电离能大小顺序F>O>S D、工业生产硫酸时用水吸收SO3(4)、大π键可用符号π表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则SO3中的大π键可表示为。(5)、黄铜矿为含硫矿石,这种矿石浑身都是宝。黄铜矿的晶胞如图2所示,原子1的坐标为与Cu(0,0,0)最近的Fe原子的坐标为;若阿伏加德罗常数的值为NA , 则黄铜矿晶体的密度是g⋅cm-3。
图2
-
9、下列实验操作及其现象、结论都正确的是( )
实验操作
现象
结论
A
将少量乙二醇滴入酸性KMnO4溶液中
溶液紫色变浅
乙二醇被氧化成乙二酸
B
用电导仪测定碱性条件下乙酸乙酯水解反应中导电能力的变化(溶液温度不变)
随着反应进行,
溶液的导电能力逐渐下降
相同浓度的OH-导电能力强于CH3COO-
C
用洁净的玻璃棒蘸取某无色溶液,在酒精灯上灼烧
火焰出现黄色
溶液中含有Na元素
D
用pH计测定浓度为0.1mol·L-1的NaHCO3溶液与CH3COOH溶液
NaHCO3的pH值小于CH3COOH的pH值
A、A B、B C、C D、D -
10、水体中的重金属离子,如Cu2+ , Sn2+可通过转化为CuS,SnS除去。已知室温下Kₐₗ(H2S)=9×10-8 , Kₐ2(H2S)=1×10-12 , 下列说法正确的是( )A、0.1mol·的Na2S溶液中: B、0.1mol·的NaHS溶液中: C、向10mL0.001mol·的CuSO4溶液中加入10mL0.001mol·的Na2S溶液,有沉淀析出。忽略混合时溶液体积的变化,则说明. D、室温时,向0.001molSnS粉末中加入10mL0.1mol·L-1的CuSO4溶液,充分浸出后所得溶液中则
-
11、铁酸锌(ZnFe2O4)是效果较好的脱硫剂,脱硫反应为 ΔH,经实验测定在不同的投料比x1、x2、x3[投料比]时H2S的平衡转化率与温度的关系如图。现向5L的恒容密闭容器中,投入3molH2S、2molH2与足量ZnFe2O4 , 初始压强为p0 , 平衡时H2O(g)的体积分数是H2的两倍,则下列说法正确的是( )
 A、△H>O B、x1>x2>x3 C、该温度下该反应的 D、恒温恒容条件下,若混合气体压强不变,则说明反应已到达平衡
A、△H>O B、x1>x2>x3 C、该温度下该反应的 D、恒温恒容条件下,若混合气体压强不变,则说明反应已到达平衡 -
12、工业废水中常含有氮、氯元素,可用电解原理对含有高浓度氯离子的工业废水中的氮进行脱除。用NH4NO3和NaCl分别模拟工业废水中的氮和氯,电化学处理装置如图1所示;在电解过程中,模拟工业废水中ClO-的浓度随时间变化的曲线如图2所示。

图1 图2
下列说法不正确的是( )
A、该方法能脱除废水中的NO3 , 无法脱除NH4+ B、A电极接电源的正极,B电极接电源的负极 C、B电级的反应式为: D、电解过程中,A电极附近的溶液pH值降低 -
13、K3[Fe(C2O4)3]⋅3H2O为草绿色晶体,易溶于水,难溶于乙醇,可用FeC2O4制备,流程如下已知:FeC2O4+3H2O2+6K2C2O4=4K3[Fe(C2O4)3]+2Fe(OH)3↓

下列说法不正确的是( )
A、步骤Ⅰ中不可用酸性KMnO4溶液替代H2O2 B、步骤Ⅱ中加热煮沸是为了除去多余的H2O2 C、步骤Ⅲ中加入无水乙醇是为了降低三草酸合铁酸钾的溶解度 D、可用亚铁氰化钾溶液来检验翠绿色溶液中是否还有 未被氧化 -
14、BAS是一种可定向移动的“分子机器”,其合成路线如下:

下列说法正确的是( )
A、 存在顺反异构
B、
存在顺反异构
B、 既有酸性又有碱性
C、中间产物结构简式:
既有酸性又有碱性
C、中间产物结构简式: D、①为加成反应,②为消去反应
D、①为加成反应,②为消去反应
-
15、W、X、Y、Z四种短周期主族元素的原子序数依次增大,WY为10电子分子,X与Y、Z在元素周期表中相邻,下列说法不正确的是( )A、简单原子半径Z>X>Y>W B、ZX3Y-中Z原子采取sp3杂化 C、W2X和WY两种分子间可以形成四种氢键 D、四种元素形成的化合物WZX3Y为强酸
-
16、当新鲜的牛奶被加热后,其表面会凝结成一层奶皮,这层奶皮富含多种营养物质,包括蛋白质、脂肪和糖类等,下列说法不正确的是( )A、蛋白质、脂肪和糖类等物质是以碳链为骨架的有机高分子化合物 B、蛋白质分子内含有氢键 C、可以通过红外光谱分析来识别葡萄糖分子中的官能团 D、灼烧蛋白质时会散发出类似烧焦羽毛的气味
-
17、粗盐提纯实验是初中阶段的一项基础实验内容,下列关于该实验的说法不正确的是( )A、溶解时加热的主要目的是增加食盐的溶解度 B、该实验过滤通常要进行2~3次,若跳过首次过滤,则应控制后续添加的Na2CO3的用量 C、第二次过滤的滤渣主要为碱式盐和复盐 D、若粗盐中含有钾离子,则加热时不能用余热蒸干
-
18、NA为阿伏加德罗常数的值,下列说法正确的是( )A、3.2gCaC2中含有的离子数是0.15NA B、17gNH3通入水中,溶液中含有的质子数为10NA C、50g质量分数为60%的丙醇水溶液中含有的σ键数目为5.5NA D、标准状况下,11.2L甲烷和乙烯混合物中含氢原子数为2NA
-
19、已知反应:2LiCoO2+3H2SO4+H2O2=Li2SO4+2CoSO4+O2↑+4H2O下列说法正确的是,( )A、H2O2作氧化剂 B、H2O2的空间结构为三角锥形 C、消耗1molLiCoO2转移电子的数目为2mol D、氧化剂和还原剂的比值为2:1
-
20、在溶液中能大量共存的离子组是( )A、H+、Fe3+、ClO-、Cl- B、K+ 、Na+ 、 、 C、H+、K+、F-、Cl- D、、、、