相关试卷
-
1、农用工具的发明与使用体现了中国智慧。下列农具中最可能含有硅酸盐的是( )




A.旧石器石铲
B.河姆渡骨耜(sì)
C.春秋青铜铲
D.汉铁铲
A、A B、B C、C D、D -
2、某研究小组通过下列路线合成药物西地那非。

已知:Mc为甲基(—CH3),Et为乙基(—CH2CH3),Pr为正丙基(—CH2CH2CH3);化合物I中不存在一个氮原子与两个羰基直接和连的结构。
请回答:
(1)、化合物A的含氧官能团的名称是。(2)、试剂Y的结构简式是。(3)、下列说法正确的是____。A、D→E的反应条件X为浓硝酸、浓硫酸并适当加热 B、化合物I→J的反应主要经历了加成和消去的过程 C、保持其它条件不变,若将B→C中的CH3I改为CH3Cl,则该反应速率将变快 D、可通过测定K的质谱图来确定J→K中ClSO3H参与反应的是Cl原子还是OH基团(4)、写出F与过量NH3反应生成G的化学方程式。(5)、有机玻璃是一种重要的塑料( ),可通过化合物W(
),可通过化合物W( ),聚合得到。设计以丙酮和甲醇为原料合成W的路线(用流程图表示,无机试剂任选)。 (6)、写出同时符合下列条件的化合物C的同分异构体的结构简式。
),聚合得到。设计以丙酮和甲醇为原料合成W的路线(用流程图表示,无机试剂任选)。 (6)、写出同时符合下列条件的化合物C的同分异构体的结构简式。①分子中含有苯环;
②1H-NMR谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,有氮氧键,无氧氢键和氧氧键;
③分子中没有两个甲基连在同一个碳原子上。
-
3、某兴趣小组用下图的装置制取ICl,并用ICl的冰醋酸溶液来测定某油脂的不饱和度。油脂的不饱和度是指一个油脂分子最多可加成的氢分子数。
已知:①ICl的熔点为13.9℃,沸点为97.4℃,化学性质与氯气相似易水解;
② , ICl3的熔点为111℃.

请回答:
(1)、:写出第一个装置中发生反应的化学方程式:。(2)、虚线框内应选用的装置是(填“甲”或“乙”)。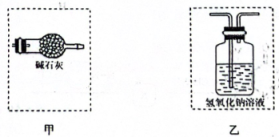 (3)、上述制备ICl的实验中,根据气流方向各装置的连接顺序为;
(3)、上述制备ICl的实验中,根据气流方向各装置的连接顺序为;a→ →→→→→(用接口的字母表示)
(4)、下列有关说法正确的是____A、上述实验装置中的KMnO4固体也可用MnO2代替 B、恒压滴液漏斗使用时应打开上面的玻璃塞 C、ICl与NaOH溶液反应的方程式为: D、若所制得的ICl中溶有少量ICl3杂质,可以采用蒸馏法进行提纯(5)、用ICl的冰醋酸溶液测定某油脂的不饱和度,进行如下实验,实验过程中有关反应为:①
 ;②;③
;②;③实验步骤:
将含有0.05mol某油脂的样品溶于CCl4后形成100mL溶液;从中取出10mL,加入20mL含有ICl物质的量为n mol的冰醋酸溶液(过量);充分反应后,加入足量KI溶液;生成的碘单质用a 的标准溶液滴定;重复上述实验两次,测得滴定所需NazS2O3的平均值为V mL.
①滴定前,需要将装有标准液的滴定管中的气泡排尽,应选择图中。
A.
 B.
B. C.
C. D.
D.
②该油脂的不饱和度为(用含a、n、V的表达式表示)。
-
4、一种燃煤烟气中CO2的捕集和资源再利用技术可通过图1转化过程实现。
 (1)、以过渡金属作催化剂,利用图2所示装置可实现“转化”。写出阴极表面的电极反应方程式。(2)、CO2可以被NaOH溶液捕获.若所得溶液 , 则溶液中含碳微粒(①H2CO3、②、③)的浓度由大到小的顺序为(填序号)。(室温下,的;)(3)、在催化剂下,CO2氧化C2H6可获得C2H4。其主要化学反应为:
(1)、以过渡金属作催化剂,利用图2所示装置可实现“转化”。写出阴极表面的电极反应方程式。(2)、CO2可以被NaOH溶液捕获.若所得溶液 , 则溶液中含碳微粒(①H2CO3、②、③)的浓度由大到小的顺序为(填序号)。(室温下,的;)(3)、在催化剂下,CO2氧化C2H6可获得C2H4。其主要化学反应为:反应I.
反应II.
反应III.
将4 mol C2H6和6 mol CO2的混合气体置于1.0L恒容密闭容器中反应,乙烷的平衡转化率、乙烯的选择性与温度关系如图3所示(C2H4的选择性。

②M点反应I的平衡常数为(保留两位有效数字)。
③C2H4选择性随温度升高而下降的原因可能是。
(4)、用Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯,所得产物含C3H6、C4H8等副产物,反应过程如图4。
催化剂中添加Na、K、Cu助剂后可改变反应的选择性。在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如表所示:
助剂
CO2转化率/%
各产物在所有产物中的占比/%
C2H4
C3H6
其他
Na
42.5
35.9
39.6
24.5
K
27.2
75.6
22.8
1.6
Cu
9.8
80.7
12.5
6.8
下列说法正确的是____。
A、催化剂助剂主要在第Ⅰ步起作用 B、在Fe3(CO)12/ZSM-5中添加K助剂时,合成乙烯的效果最好 C、添加助剂不同,CO2加氢合成乙烯的平衡常数不同 D、Fe3(CO)12为簇状超分子,可活化CO -
5、光盘金属层含有Ag(其它金属微量忽略不计),可以进行资源回收利用。下图为从光盘中提取Ag的工业流程;

已知:①气体A、气体D是空气的主要组成气体。
②配离子的形成是分步进行的:
③AgCl的
请回答:
(1)、已知Ag位于周期表的第五周期、IB族,Ag的原子序数为。气体A的化学式为。写出溶液C中所有的阳离子。
(2)、反应III的离子方程式为。(3)、是一个可逆反应。①结合相关数据说明上述反应是可逆反应;
②设计实验验证上述反应是可逆反应。
-
6、氮、碳、硼元素形成的化合物具有独特的结构。请回答:(1)、固态的N2O5为离子晶体(阴阳离子中所含原子个数均不超过4个),其阳离子的空间结构名称为 , 阴离子中氮原子的杂化方式为。(2)、比较酸性强弱:(填“>”、“<”),请说明理由。(3)、当石墨被过量的K处理后(未反应的金属被汞洗出),K+离子在石墨层间嵌入,K+层在石墨层的投影如图1所示。该钾石墨晶体的化学式是 , 晶体类型是。
 (4)、石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x , 该物质仍具润滑性,其单层局部结构如图2所示。下列关于该化合物的说法不正确的是( )A、与石墨相比,(CF)x导电性增强 B、与石墨相比,(CF)x抗氧化性增强 C、(CF)x中C—F的键长比C—C短 D、1mol(CF)x中含有2x mol共价单键(5)、硼砂与NaOH的混合溶液中加入H2O2可以制备 , 已知X的阴离子只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式。
(4)、石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x , 该物质仍具润滑性,其单层局部结构如图2所示。下列关于该化合物的说法不正确的是( )A、与石墨相比,(CF)x导电性增强 B、与石墨相比,(CF)x抗氧化性增强 C、(CF)x中C—F的键长比C—C短 D、1mol(CF)x中含有2x mol共价单键(5)、硼砂与NaOH的混合溶液中加入H2O2可以制备 , 已知X的阴离子只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式。 -
7、根据下列有关实验方案设计和现象,所得结论不正确的是( )
选项
实验方案
现象
结论
A
将打磨过的铁铜合金放在氨水中一段时间
溶液变为深蓝色
可能是铜在氨水中发生吸氧腐蚀
B
向FeCl3溶液中滴加KSCN溶液,再加入少量Cu粉
溶液先变成血红色,加入Cu粉后,血红色变浅
与SCN-的配位能力:
C
将和NH4NO3固体混合并用玻璃棒快速搅拌
有刺激性气味的气体产生,并伴随降温
该反应能发生的主要原因是嫡增
D
用精密pH试纸测定溶液的pH值
测得pH为7.8
A、A B、B C、C D、D -
8、常温常压下,H2S气体在水中的饱和浓度约为。已知: , ;。下列说法不正确的是( )A、饱和H2S溶液中存在 B、向溶液中加几滴浓盐酸,使其浓度达到, , 此时溶液中约为 C、向溶液中通入H2S气体直至饱和,溶液中有FeS沉淀生成 D、的平衡常数为
-
9、在葡萄糖水溶液中,链状结构与环状结构的平衡关系及百分含量如下:

下列说法不正确的是( )
A、链状葡萄糖成环是-OH与-CHO发生加成反应的结果 B、链状葡萄糖成环反应的 , C、链状葡萄糖成环后,分子中多了一个手性碳原子 D、水溶液中,吡喃葡萄糖比吡喃葡萄糖稳定 -
10、如图所示装置中,C1、C2是石墨电极。A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液。当连接开关K,并向B中滴加浓盐酸时,发现灵敏电流计G的指针向右偏转。一段时间后,当电流计指针回到中间“0”位置时,再向B中滴加过量浓NaOH溶液,可观察到电流计指针向左偏转。下列说法正确的是( )
 A、电流计G的指针向右偏转时,化学能转变为电能;向左偏转时,电能转变为化学能 B、电流计G的指针向右偏转时,C1电极反应为: C、电流计G的指针向左偏转时,C2电极反应为: D、由上述实验现象可知,氧化性:
A、电流计G的指针向右偏转时,化学能转变为电能;向左偏转时,电能转变为化学能 B、电流计G的指针向右偏转时,C1电极反应为: C、电流计G的指针向左偏转时,C2电极反应为: D、由上述实验现象可知,氧化性: -
11、短周期元素X、Y、Z、W、Q原子序数依次增大。W简单离子在同周期离子中半径最小;基态X、Z、Q原子均有两个单电子,Q与Z同主族。下列说法不正确的是( )A、第一电离能: B、电负性: C、Z与Q形成的化合物可能是非极性分子 D、Z的氢化物沸点不可能低于X的氢化物沸点
-
12、姜黄素X(
 )的合成路线如下:
)的合成路线如下:
下列说法不正确的是( )
A、A的键线式为 B、B有5种化学环境不同的氢原子
C、有机物C能发生银镜反应
D、X分子中有4种官能团
B、B有5种化学环境不同的氢原子
C、有机物C能发生银镜反应
D、X分子中有4种官能团
-
13、下列化学反应与方程式不相符的是( )A、少量FeCl3固体加入到KI浓溶液中: B、Cu和浓HNO3反应: C、Al2(SO4)3溶液与Na[Al(OH)4]溶液反应: D、少量甲醛与新制Cu(OH)2反应:
-
14、下列说法正确的是( )A、用酸性KMnO4溶液可鉴别汽油、煤油和柴油 B、用NaOH溶液、硝酸银溶液可鉴别氯乙烷、溴乙烷和碘乙烷 C、用溴水可鉴别酒精、苯酚、己烯和甲苯 D、用饱和Na2CO3溶液可鉴别乙醇、乙醛、乙酸和乙酸乙酯
-
15、下列装置能达到实验目的的是( )A、熔化Na2CO3:
 B、验证SO2氧化性:
B、验证SO2氧化性: C、实验室制CO2:
C、实验室制CO2: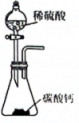 D、实验室保存液溴:
D、实验室保存液溴:
-
16、根据材料的组成和结构变化可推测其性能变化,下列推测不合理的是( )
材料
组成和结构变化
性能变化
A
聚乙烯
低压法聚乙烯转变为高压法聚乙烯
软化温度和密度增大
B
纯铝
加入少量Mn等其它金属
硬度增大
C
钢铁
钢铁表面进行发蓝处理
抗腐蚀性增强
D
液态植物油
与氢气加成,提高其饱和程度
熔化温度提高
A、A B、B C、C D、D -
17、明矾常用作净水剂,下列关于明矾大晶体制备实验的说法不正确的是( )A、配制明矾饱和溶液的温度要控制在比室温高10~15℃ B、明矾小晶核要悬挂在饱和溶液中央,可避免形成形状不规整的晶体 C、形成大晶体的过程中,需要敞开玻璃杯静置较长时间 D、本实验中所用仪器都要用蒸馏水洗净
-
18、在溶液中能大量共存的离子组是( )A、Na+、Pb2+、、 B、K+、CN-、Cl-、[Fe(SCN)6]3- C、K+、H+、Cl-、 D、OH-、K+、、
-
19、我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为: , 下列说法不正确的是(NA为阿伏加德罗常数的值)( )A、该反应在任何温度下都可以自发进行 B、生成28gN2转移电子的数目为10NA C、KNO3是氧化剂 D、K2S和N2都是还原产物
-
20、下列表示不正确的是( )A、苯甲酰胺的分子式:C7H7NO B、油酸甘油酯的结构简式:
 C、基态Ti2+离子的电子排布式:
D、Cl-Cl的p-p键电子云图形:
C、基态Ti2+离子的电子排布式:
D、Cl-Cl的p-p键电子云图形: