相关试卷
-
1、下列各组离子中能大量共存的是A、Cl-、OH-、SO、NH B、H+、Fe2+、SO、Cl- C、K+、Ba2+、NO、SO D、H+、Cl-、MnO、Fe2+
-
2、维生素C是重要的营养素,其分子结构如图。下列关于维生素C的叙述不正确的是
 A、维生素C的分子式为C6H8O6 B、分子中含有3种官能团 C、1mol该物质最多能与2mol H2加成 D、该物质能发生氧化反应、取代反应、消去反应
A、维生素C的分子式为C6H8O6 B、分子中含有3种官能团 C、1mol该物质最多能与2mol H2加成 D、该物质能发生氧化反应、取代反应、消去反应 -
3、实验室为配制0.10mol/L的稀硫酸,不需要用到的仪器是A、
 B、
B、 C、
C、 D、
D、
-
4、下列仪器与名称对应不正确的是A、坩埚
 B、圆底烧瓶
B、圆底烧瓶 C、长颈漏斗
C、长颈漏斗 D、容量瓶
D、容量瓶
-
5、已知 , 25℃时,的 , 。用溶液滴定溶液,溶液中、、的分布分数随pH变化曲线及滴定曲线如下图(忽略滴定过程中温度的变化)。下列说法错误的是[如分布分数:]
 A、两次突变,应选用不同的指示剂 B、pH=8时: C、b点溶液的pH约为4.54 D、
A、两次突变,应选用不同的指示剂 B、pH=8时: C、b点溶液的pH约为4.54 D、 -
6、新型化学电池Zn-、能量密度大、体积小、重量轻、寿命长、无污染。下列关于其放电时的说法错误的是A、负极发生失电子的氧化反应 B、将化学能转化为电能 C、在正极得电子 D、阳离子向负极移动
-
7、下列说法中不正确的是




A.该实验用于观察Fe(OH)2
的颜色
B.比较Na2CO3和NaHCO3稳定性,甲物质为Na2CO3
C.光照过程中氯水中氯离子的浓度变化的主要原因是HClO见光分解
D.实验员看到钾元素的焰色为紫色
A、A B、B C、C D、D -
8、设NA为阿伏加德罗常数,下列说法正确的是A、0.1 mol Na2O2中阴离子的数目为0.2 NA B、0.1 mol Na2O2与足量的水反应,转移电子的数目为0.2 NA C、0.1 mol Fe和0.1 mol Cl2在点燃条件下反应时转移电子数目为0.2 NA D、1 L 0.4 mol·L-1的浓盐酸与足量的MnO2加热充分反应,产生Cl2的数目等于0.1 NA
-
9、某容器中发生一个化学反应,反应过程中存在Fe2+、、Fe3+、、H+和水六种粒子,在反应过程中测得Fe3+、的含量随时间变化的曲线如图所示,下列判断错误的是
 A、被还原,发生还原反应 B、还原性:Fe2+> C、该反应中Fe2+被氧化为Fe3+ D、还原剂与氧化剂的个数之比为6∶1
A、被还原,发生还原反应 B、还原性:Fe2+> C、该反应中Fe2+被氧化为Fe3+ D、还原剂与氧化剂的个数之比为6∶1 -
10、下列有关钠的化合物说法正确的是A、将NaOH浓溶液滴加到饱和FeCl3溶液中制备Fe(OH)3胶体 B、将过氧化钠加入到硫酸亚铁溶液中,可以观察到有红褐色沉淀生成 C、过氧化钠与水反应生成NaOH,过氧化钠属于碱性氧化物 D、大量的Na2O2粉末加入到酚酞溶液中,可以观察到酚酞最终变红
-
11、无放射性的同位素被称之为“稳定同位素”,在陆地生态系统研究中,2H、13C、15N、18O、34S等常作环境分析指示物。下列有关一些“稳定同位素”的说法正确的是A、34S原子核内中子数为16 B、2H、3H属于同种核素 C、16O与18O最外层电子数相同 D、13C和15N原子核内的质子数相差2
-
12、干冰升华过程中,其焓变和熵变正确的是A、 , B、 , C、 , D、 ,
-
13、某溶液中含有Na+、CO、HCO、Cl- , 在加入Na2O2后浓度不发生变化的是A、Na+、CO B、Cl- C、CO、Cl- D、HCO
-
14、实验室用和浓盐酸反应生成后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
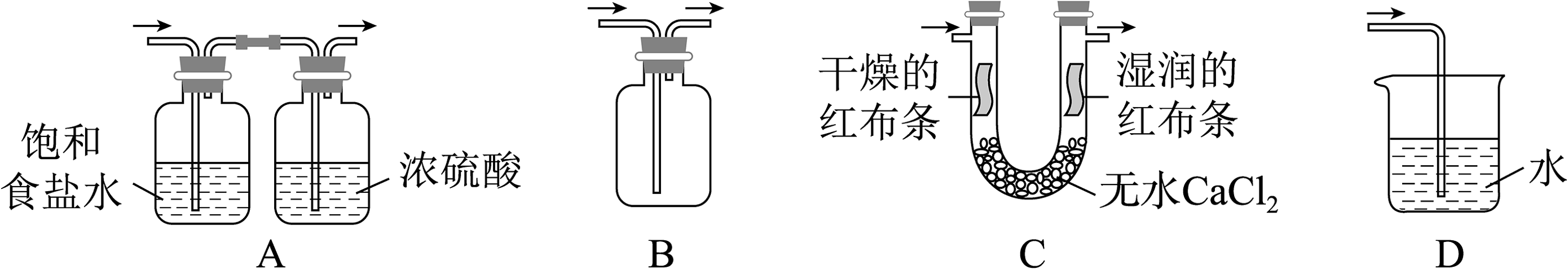 A、A B、B C、C D、D
A、A B、B C、C D、D -
15、下列关于化合物
 的说法正确的是 A、与苯互为同系物 B、可以发生取代、加成、加聚反应 C、分子中所有原子可能共平面 D、一氯代物有4种(不考虑立体异构)
的说法正确的是 A、与苯互为同系物 B、可以发生取代、加成、加聚反应 C、分子中所有原子可能共平面 D、一氯代物有4种(不考虑立体异构) -
16、下述实验中均有红棕色气体产生,对比分析所得结论正确的是



①
②
③
A、由①中的红棕色气体,推断产生的气体一定都是氮的氧化物 B、②中产生红棕色气体说明②中木炭与浓硝酸产生了反应 C、由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 D、③的气体产物中检测出由此说明木炭一定与浓硝酸发生了反应 -
17、部分含或含物质的分类与相应化合价关系如图所示。下列推断不合理的是
 A、可存在c→d→e的转化 B、能与反应生成c的物质只有b C、新制的d可用于检验葡萄糖中的醛基 D、若b能与反应生成 , 则b中含共价键
A、可存在c→d→e的转化 B、能与反应生成c的物质只有b C、新制的d可用于检验葡萄糖中的醛基 D、若b能与反应生成 , 则b中含共价键 -
18、常温下,将体积均为的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随的变化如图所示。已知 , 下列说法正确的是
 A、电离常数: B、水的电离程度:b>d C、升温,a点溶液中增大 D、等浓度HA和BOH溶液等体积混合,溶液的pH<7
A、电离常数: B、水的电离程度:b>d C、升温,a点溶液中增大 D、等浓度HA和BOH溶液等体积混合,溶液的pH<7 -
19、氮氧化物、二氧化硫能引发酸雨、雾霾等。回答下列问题:(1)、汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的化学方程式为。(2)、目前工业上烟气脱硫脱硝的工艺流程如下:

已知:烟气中含尘、、。
“催化氧化”的目的是;图中产品中含硫成分为(填化学式)。该物质中含有键(填化学键类型),写出该物质的一种用途。
(3)、为探究某种催化剂在有氧条件下用还原的最佳温度,将一定比例的、和混合,以一定的流速通过催化还原反应器[如图(a)],反应相同时间后测得的去除率随反应温度的变化曲线如图(b)所示。
①写出催化反应器中与反应的化学方程式:。
②当反应温度高于380℃时,的去除率迅速下降的原因可能是。
-
20、将NaCl固体溶于水后,溶液中存在多种微粒,如图所示的微粒是
 A、聚合水分子 B、水合钠离子 C、水合氯离子 D、水合氢离子
A、聚合水分子 B、水合钠离子 C、水合氯离子 D、水合氢离子