相关试卷
-
1、活性炭吸附法是工业提碘的主要方法之一。其流程如图:下列有关叙述正确的是( )
 A、反应①的离子方程式为2NO2-+2H2O+2I-=2NO↑+I2+4OH- B、实验室从反应②所得溶液提取碘可采用蒸馏法 C、流程中I2碘经过吸附,转化为I-、IO3-再转化为I2的过程是为了增大I2的浓度 D、反应②所得溶液呈紫色
A、反应①的离子方程式为2NO2-+2H2O+2I-=2NO↑+I2+4OH- B、实验室从反应②所得溶液提取碘可采用蒸馏法 C、流程中I2碘经过吸附,转化为I-、IO3-再转化为I2的过程是为了增大I2的浓度 D、反应②所得溶液呈紫色 -
2、下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )A、H2+CuO=Cu+H2O B、2Na2O2+2H2O=4NaOH+O2↑ C、H2+Cl2=2HCl D、2NaOH+Cl2=NaCl+NaClO+H2O
-
3、下列装置应用于实验室进行相关实验,能达到实验目的的是
 A、用装置甲在强光照条件下制取一氯甲烷 B、用装置乙分离乙酸乙酯和水 C、用装置丙蒸馏石油并收集60~150℃馏分 D、用装置丁制取并收集乙酸乙酯
A、用装置甲在强光照条件下制取一氯甲烷 B、用装置乙分离乙酸乙酯和水 C、用装置丙蒸馏石油并收集60~150℃馏分 D、用装置丁制取并收集乙酸乙酯 -
4、下列有关晶体的叙述中,正确的是
 A、氯化钠晶胞中含有4个NaCl分子 B、金刚石结构中最小的环上有6个碳原子 C、干冰晶体中,每个分子周围距离相等且最近的分子共有8个 D、金属Zn晶体中的晶胞如图所示,这种堆积方式称为体心立方堆积
A、氯化钠晶胞中含有4个NaCl分子 B、金刚石结构中最小的环上有6个碳原子 C、干冰晶体中,每个分子周围距离相等且最近的分子共有8个 D、金属Zn晶体中的晶胞如图所示,这种堆积方式称为体心立方堆积 -
5、下列说法正确的是:A、其它条件不变时,升高温度,可以提高反应物的活化分子百分数 B、其它条件不变时,增大反应物的浓度,可以提高反应物的活化分子百分数 C、保持温度不变,化学平衡正向移动时,化学平衡常数增大,逆向移动时则减小 D、其它条件不变时,加入高效催化剂,可以增大化学反应速率和反应物的转化率
-
6、LED系列产品是被看好的一类节能新产品,下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是
 A、a处通入氢气,发生了还原反应:H2-2e-+2OH-=2H2O B、b处通入氧气,为电池的正极 C、该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替 D、P-型半导体连接的是电池负极.
A、a处通入氢气,发生了还原反应:H2-2e-+2OH-=2H2O B、b处通入氧气,为电池的正极 C、该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替 D、P-型半导体连接的是电池负极. -
7、短周期主族元素W、X、Y、Z 的原子序数依次增加。K、L、 M、N 均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是固体,乙是气体,K 是主要的大气污染物之一,0.05mol·L-1丙溶液的pH为1,上述物质的转化关系如下图所示。下列说法正确的是
 A、原子半径: W<X<Y<Z B、元素的非金属性: Y>Z>X C、原子最外层电子数: W<X<Y<Z D、K、L、M、N 四种物质中沸点最高的是N
A、原子半径: W<X<Y<Z B、元素的非金属性: Y>Z>X C、原子最外层电子数: W<X<Y<Z D、K、L、M、N 四种物质中沸点最高的是N -
8、下列离子方程式正确的是A、AlCl3溶液中加入足量的氨水:Al3++ 3OH- = Al(OH)3↓ B、将一小块金属钠投入到硫酸铜溶液中:2Na+Cu2+=Cu+2Na+ C、氢氧化钡溶液与硫酸反应:2H+ + SO42-+Ba2+ + 2OH-= BaSO4↓+2H2O D、将Cl2通入FeCl2溶液中:Fe2++Cl2=Fe3++2Cl-
-
9、工业上合成
 的反应为
的反应为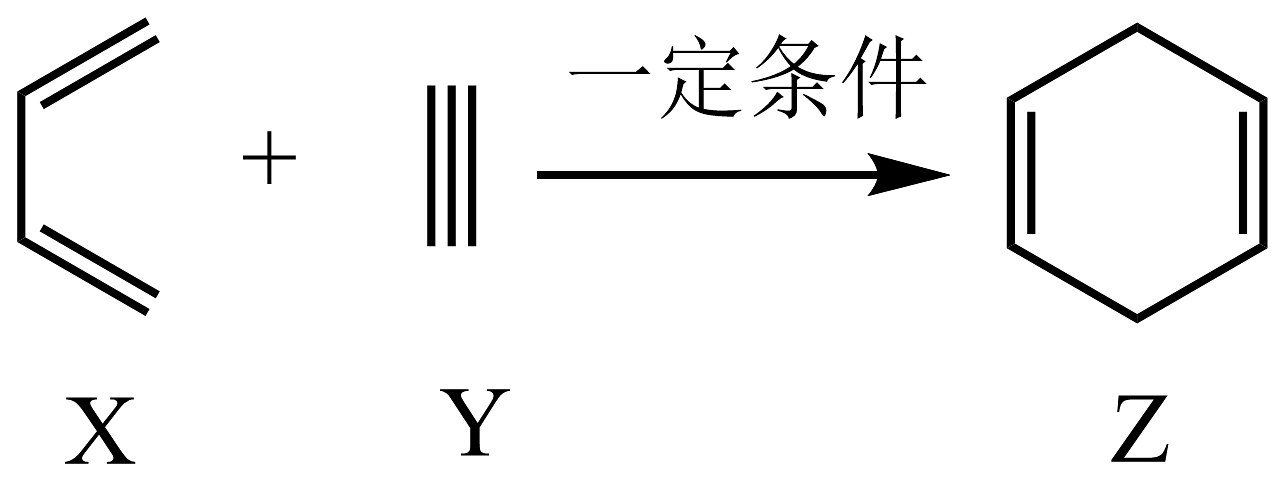 , 下列有关说法不正确的是 A、、、三种有机物均易发生加成反应 B、、、三种有机物分子中所有原子均有可能共平面 C、、、三种有机物使酸性高锰酸钾溶液褪色的原理相同 D、的二氯代物有种不考虑立体异构
, 下列有关说法不正确的是 A、、、三种有机物均易发生加成反应 B、、、三种有机物分子中所有原子均有可能共平面 C、、、三种有机物使酸性高锰酸钾溶液褪色的原理相同 D、的二氯代物有种不考虑立体异构 -
10、下列关于有机化合物的说法正确的是A、乙烯能使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同 B、葡萄糖和果糖的分子式都是 , 二者互为同分异构体 C、不含其他杂质的油脂属于纯净物 D、石油裂解和油脂皂化都是化学变化,而石油的分馏和煤的干馏都是物理变化
-
11、下列反应属于氧化还原反应的是A、 B、 C、 D、
-
12、下列物质中,工业上常用电解法冶炼的是A、Fe B、Na C、Cu D、Ag
-
13、下列各项叙述中,正确的是A、、、的电负性随原子序数的增大而增大 B、价电子排布为的元素位于第周期第Ⅴ族,是区元素 C、和轨道形状均为哑铃形,能量也相等 D、原子的价电子表示式不符合洪特规则
-
14、能源可划分为一次能源和二次能源,直接来自于自然界的能源称为一次能源;需依靠其他能源的能量间接制取的能源称为二次能源。下列叙述正确的是( )A、水煤气是二次能源 B、水力是二次能源 C、天然气是二次能源 D、电能是一次能源
-
15、下列关于常见有机物的说法正确的是A、乙烯和苯都能和溴水发生化学反应而使溴水褪色 B、乙烷可使酸性高锰酸钾溶液褪色 C、糖类和蛋白质都是高分子化合物 D、乙酸和油脂都能与氢氧化钠溶液反应
-
16、浓盐酸是一种化学实验室常用的试剂。实验用浓盐酸一般质量分数为37.0%。(1)、用浓盐酸配制100mL浓度为0.100 mol/L的稀盐酸,下列操作错误的有
________。




A.浓盐酸稀释
B.上下颠倒摇匀
C.定容
D.用蒸馏水洗涤烧杯和玻璃棒
A、A B、B C、C D、D(2)、写出浓盐酸与MnO2混合加热生成MnCl2和Cl2的离子反应方程式。
(3)、在用浓盐酸与MnO2混合加热制氯气过程中,发现氯气不再逸出时,固液混合物中仍存在盐酸和MnO2。①关于MnO2剩余的原因,该小组提出如下猜想:
猜想ⅰ.随着反应进行,c(H+)降低,Cl-的还原性减弱,不能被MnO2氧化
猜想ⅱ.随着反应进行,c(H+)降低,MnO2的氧化性减弱,不能氧化Cl-。
猜想ⅱi.随着反应进行,c(Cl-)降低,Cl-的还原性减弱,不能被MnO2氧化。
猜想iv.随着反应进行,c(Mn2+)升高,MnO2的氧化性减弱,不能氧化Cl-。
该小组设计原电池装置验证上述猜想。
恒温装置未画出。每组实验前都将电池装置放电至无明显现象且电流表归零为止。

组别
实验步骤
实验现象
实验结论
实验反思与评价
i
向右侧烧杯中滴入几滴浓盐酸
该操作不能验证猜想i,理由是①。
ii
将实验步骤补充完整:②。
预测现象:③。
猜想ii成立
正极的电极反应方程式为④。
……
iv
在验证了猜想i不成立、猜想ii和iii均成立以后,向左侧烧杯中加入⑤ , (填化学式)向右侧烧杯中加入⑥。(填化学式)
电流表几乎无示数
猜想iv成立
-
17、LiOH是生产航空航天润滑剂的原料。清华大学首创三室膜电解法制备氢氧化锂,其模拟装置如图所示。下列有关说法正确的是
 A、a极为电源的负极,Y极上发生氧化反应 B、X极的电极反应式为2H2O-4e-=4H++O2↑ C、膜1为阳离子交换膜,膜2为阴离子交换膜 D、每转移2mol电子,理论上生成24g LiOH
A、a极为电源的负极,Y极上发生氧化反应 B、X极的电极反应式为2H2O-4e-=4H++O2↑ C、膜1为阳离子交换膜,膜2为阴离子交换膜 D、每转移2mol电子,理论上生成24g LiOH -
18、关于化合物M:
 下列说法正确的是 A、M分子中处于同一直线上的原子数最多为9个 B、M分子中仅含有1个手性碳原子 C、1mol M可以消耗1mol NaOH D、M不能使酸性KMnO4稀溶液褪色
下列说法正确的是 A、M分子中处于同一直线上的原子数最多为9个 B、M分子中仅含有1个手性碳原子 C、1mol M可以消耗1mol NaOH D、M不能使酸性KMnO4稀溶液褪色 -
19、下列实验装置或操作不正确的是


A.测定锌与稀硫酸反应速率
B.测定中和反应的反应热


C.制备乙烯
D.探究铁的吸氧腐蚀
A、A B、B C、C D、D -
20、下列过程中,颜色变化与氧化还原反应无关的是A、湿润的淀粉KI试纸遇氯气变蓝色 B、放置时间较长的苯酚固体变为粉红色 C、氯化铁溶液滴入KSCN溶液变红色 D、酸性K2Cr2O7溶液滴入乙醇变绿色