相关试卷
-
1、常温下,假设1L水溶液中Co2+和C2O42-初始物质的量浓度均为0.01mol·L-1。平衡条件下,体系中全部四种含碳物种的摩尔分数随pH的变化关系如图所示(忽略溶液体积变化)。
已知:体系中含钴物种的存在形式为Co2+ , CoC2O4(s)和Co(OH)2(s);Ksp (CoC2O4)= 6.0x10°,Ksp[Co(OH)2]=5.9x10-15。
下列说法正确的是( )
 A、甲线所示物种为HC2O4- B、H2C2O4的电离平衡常数Ka2=10-8 C、pH =a时,Co2+物质的量浓度为1.6x10-3mol·L' D、pH=b时,物质的量浓度: c(OH-)<c(C2O42-)
A、甲线所示物种为HC2O4- B、H2C2O4的电离平衡常数Ka2=10-8 C、pH =a时,Co2+物质的量浓度为1.6x10-3mol·L' D、pH=b时,物质的量浓度: c(OH-)<c(C2O42-) -
2、以异丁醛(M)为原料制备化合物Q的合成路线如下,下列说法错误的是( )
 A、M系统命名为2-甲基丙醛 B、若M+X→N原子利用率为100%,则X是甲醛 C、用酸性KMnO4溶液可鉴别N 和Q D、P→Q过程中有CH3COOH生成
A、M系统命名为2-甲基丙醛 B、若M+X→N原子利用率为100%,则X是甲醛 C、用酸性KMnO4溶液可鉴别N 和Q D、P→Q过程中有CH3COOH生成 -
3、 钢渣中富含CaO,SiO2 , FeO,Fe2O3等氧化物,实验室利用酸碱协同法分离钢渣中的Ca,Si,Fe元素,流程如下。已知:Fe2(C2O4),能溶于水; Ksp(CaC2O4)=2.3x10-9 , Kp(FeC2O4)=3.2x10-7。
下列说法错误的是( )
 A、试剂X可选用Fe粉 B、试剂Y可选用盐酸 C、“分离”后Fe元素主要存在于滤液Ⅱ中 D、“酸浸”后滤液Ⅰ的pH过小会导致滤渣Ⅱ质量减少
A、试剂X可选用Fe粉 B、试剂Y可选用盐酸 C、“分离”后Fe元素主要存在于滤液Ⅱ中 D、“酸浸”后滤液Ⅰ的pH过小会导致滤渣Ⅱ质量减少 -
4、全铁液流电池工作原理如图所示,两电极分别为石墨电极和负载铁的石墨电极。下列说法正确的是( )
 A、隔膜为阳离子交换膜 B、放电时,a极为负极 C、充电时,隔膜两侧溶液Fe2浓度均减小 D、理论上,Fe3+每减少1mol,Fe2+总量相应增加2mol
A、隔膜为阳离子交换膜 B、放电时,a极为负极 C、充电时,隔膜两侧溶液Fe2浓度均减小 D、理论上,Fe3+每减少1mol,Fe2+总量相应增加2mol -
5、完成下列实验所用部分仪器或材料选择正确的是( )
实验内容
仪器或材料
A
灼烧海带
坩埚、泥三角
B
加热浓缩NaCl溶液
表面皿、玻璃棒
C
称量5.0gNaOH 固体
电子天平、称量纸
D
量取25.00mL稀H2SO4
25mL移液管、锥形瓶
A、A B、B C、C D、D -
6、在恒容密闭容器中,Na2SiF6(s)热解反应所得固相产物和气相产物均为含氟化合物。平衡体系中各组分物质的量随温度的变化关系(实线部分)如图所示。已知:T2温度时,Na2SiF6(s)完全分解;体系中气相产物在T1T3温度时的分压分别为p1 , p3。下列说法错误的是( )
 A、a线所示物种为固相产物 B、T1温度时,向容器中通入N2 , 气相产物分压仍为p1 C、p3小于T3温度时热解反应的平衡常数Kp。 D、T1温度时、向容器中加入b线所示物种,重新达平衡时逆反应速率增大
A、a线所示物种为固相产物 B、T1温度时,向容器中通入N2 , 气相产物分压仍为p1 C、p3小于T3温度时热解反应的平衡常数Kp。 D、T1温度时、向容器中加入b线所示物种,重新达平衡时逆反应速率增大 -
7、用肼(N2H4)的水溶液处理核冷却系统内壁上的铁氧化物时,通常加入少量CuSO4 , 反应原理如图所示。下列说法正确的是( )
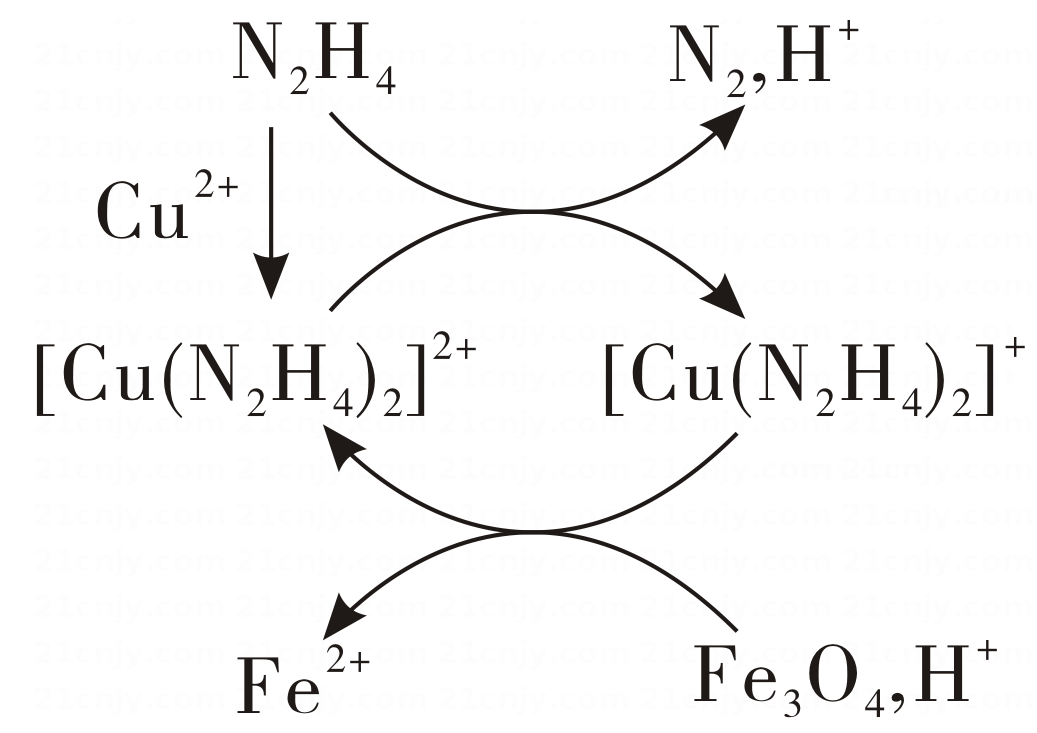 A、N2是还原反应的产物 B、还原性:N2H4<Fe2+ C、处理后溶液的pH增大 D、图示反应过程中起催化作用的是Cu2+
A、N2是还原反应的产物 B、还原性:N2H4<Fe2+ C、处理后溶液的pH增大 D、图示反应过程中起催化作用的是Cu2+ -
8、物质性质与组成元素的性质有关,下列对物质性质差异解释错误的是( )
性质差异
主要原因
A
沸点:H2O>H2S
电离能:O>S
B
酸性:HClO>HBrO
电负性:Cl>Br
C
硬度:金刚石>晶体硅
原子半径:Si>C
D
熔点:MgO>NaF
离子电荷: Mg2+ >Na+ , O2- >F-
A、A B、B C、C D、D -
9、用硫酸和NaN3可制备一元弱酸HN3。下列说法错误的是( )A、NaN3的水溶液显碱性 B、N3-的空间构型为V形 C、NaN3为含有共价键的离子化合物 D、N3-的中心N原子所有价电子均参与成键
-
10、 第70号元素镱(Yb)的基态原子价电子排布式为4f146s2。下列说法正确的是( )A、Yb的中子数与质子数之差为 104 B、Yb与°Yb是同一种核素 C、基态Yb原子核外共有10个d电子 D、Yb位于元素周期表中第6周期
-
11、下列实验涉及反应的离子方程式书写正确的是( )A、用NaOH 溶液吸收少量SO2:SO2+ OH" = HSO3- B、用Na2O2和水制备少量O2: Na2O2+H2O =2Na++2O2↑ C、用MnO2和浓盐酸制备Cl2: D、用稀硝酸溶解少量Cu粉:3Cu+8H++8NO3-= 3Cu(NO3)2+2NO↑+4H2O
-
12、 称取1.6g 固体 NaOH 配制400mL浓度约为0.1mol·L-1的NaOH 溶液,下列仪器中不需要使用的是( )A、100mL烧杯 B、500mL容量瓶 C、500mL量筒 D、500mL细口试剂瓶(具橡胶塞)
-
13、实验室中,下列试剂保存方法正确的是( )A、液溴加水封保存在广口试剂瓶中 B、硝酸银溶液保存在棕色细口试剂瓶中 C、高锰酸钾与苯酚存放在同一药品柜中 D、金属锂保存在盛有煤油的广口试剂瓶中
-
14、化学应用体现在生活的方方面面,下列用法不合理的是( )A、用明矾净化黄河水 B、用漂白粉漂白蚕丝制品 C、用食醋去除水壶中水垢 D、用小苏打作烘焙糕点膨松剂
-
15、下列在化学史上产生重要影响的成果中,不涉及氧化还原反应的是( )A、侯德榜发明了以NH3CO2和NaCl为原料的联合制碱法 B、戴维电解盐酸得到H2和CI2 , 从而提出了酸的含氢学说 C、拉瓦锡基于金属和O2的反应提出了燃烧的氧化学说 D、哈伯发明了以N2和H2为原料合成氨的方法
-
16、 化合物I具有杀虫和杀真菌活性,以下为其合成路线之一(部分反应条件已简化)。

回答下列问题:
(1)、I中含氧官能团的名称是。(2)、A的结构简式为。(3)、由B生成C的化学方程式为。反应时,在加热搅拌下向液体B中滴加异丙醇;若改为向异丙醇中滴加B则会导致更多副产物的生成,副产物可能的结构简式为(写出一种即可)。(4)、由D生成E的反应类型为。(5)、由F生成H的反应中可能生成中间体J,已知J的分子式为 , 则J的结构简式为(写出一种即可)。(6)、G的同分异构体中,含有碳氧双键的还有种(不考虑立体异构);其中,能发生银镜反应,且核磁共振氢谱显示为两组峰的同分异构体的结构简式为。 -
17、 的热分解与催化的重整结合,可生产高纯度合成气 , 实现碳资源的二次利用。主要反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
回答下列问题:
(1)、位于元素周期表中区;基态的价电子排布式为。(2)、水分子的模型与其空间结构模型不同,原因是。(3)、的晶胞如图1所示(晶胞参数),该物质的化学式为。 (4)、恒压条件下,重整反应可以促进分解,原因是。(5)、在温度分别为和下,的平衡转化率与压强的关系如图2所示,反应温度最高的是(填“”“”或“”),原因是。
(4)、恒压条件下,重整反应可以促进分解,原因是。(5)、在温度分别为和下,的平衡转化率与压强的关系如图2所示,反应温度最高的是(填“”“”或“”),原因是。 (6)、一定温度、下,向体系中加入和 , 假设此条件下其他副反应可忽略,恒压反应至平衡时,体系中转化率为 , 转化率为 , 物质的量为 , 反应Ⅲ的平衡常数(保留小数点后一位),此时原位利用率为。
(6)、一定温度、下,向体系中加入和 , 假设此条件下其他副反应可忽略,恒压反应至平衡时,体系中转化率为 , 转化率为 , 物质的量为 , 反应Ⅲ的平衡常数(保留小数点后一位),此时原位利用率为。已知:原位利用率
-
18、 某研究小组设计了如下实验测定某药用硫黄中硫的含量,其中硫转化的总反应为。
主要实验步骤如下:
Ⅰ.如图所示,准确称取细粉状药用硫黄于①中,并准确加入乙醇溶液(过量),加入适量蒸馏水,搅拌,加热回流。待样品完全溶解后,蒸馏除去乙醇。

Ⅱ.室温下向①中加入适量蒸馏水,搅拌下缓慢滴加足量溶液,加热至 , 保持 , 冷却至室温。
Ⅲ.将①中溶液全部转移至锥形瓶中,加入2滴甲基橙指示剂,用标准溶液滴定至终点,消耗溶液体积为。
Ⅳ.不加入硫黄,重复步骤Ⅰ、Ⅱ、Ⅲ做空白实验,消耗标准溶液体积为。计算样品中硫的质量分数。
Ⅴ.平行测定三次,计算硫含量的平均值。
回答下列问题:
(1)、仪器①的名称是:;②的名称是。(2)、步骤Ⅰ中,乙醇的作用是。(3)、步骤Ⅰ中,样品完全溶解后,必须蒸馏除去乙醇的原因是。(4)、步骤Ⅱ中不宜采用水浴加热的原因是。步骤Ⅱ结束后,若要检验反应后溶液中的 , 实验操作是。(5)、步Ⅲ中,判断滴定达到终点的现象为。(6)、单次样品测定中硫的质量分数可表示为(写出计算式)。 -
19、 一种从预处理得到的贵金属合金粉[主要成分为、(铑)、 , 含有少量]中尽可能回收铑的工艺流程如下:

回答下列问题:
(1)、“酸溶1”的目的是。(2)、已知“酸溶2”中转化为 , 则生成该物质的化学方程式为;“滤渣”的主要成分是(填化学式)。(3)、“沉铑”中得到的沉淀经“灼烧”后分解成铑单质,但夹杂少量和 , 则“高温还原”中发生反应的化学方程式为。(4)、若“活化还原”在室温下进行,初始浓度为 , 为避免生成沉淀,溶液适宜的为____(填标号)[已知的]。A、2.0 B、4.0 C、6.0(5)、“活化还原”中,必须过量,其与(III)反应可生成 , 提升了的还原速率,该配离子中的化合价为;反应中同时生成 , (III)以计,则理论上和(III)反应的物质的量之比为。(6)、“酸溶3”的目的是。 -
20、 乙二胺( , 简写为Y)可结合转化为(简写为)(简写为)。与Y可形成和两种配离子。室温下向溶液中加入Y,通过调节混合溶液的改变Y的浓度,从而调控不同配离子的浓度(忽略体积变化)。混合溶液中和Y的初始浓度分别为和。与的变化关系如图1所示(其中M代表、或),分布系数与的变化关系如图2所示(其中N代表Y、或)。比如。

下列说法错误的是( )
A、曲线I对应的离子是 B、最大时对应的 C、反应的平衡常数 D、时,