相关试卷
- 广东省惠州市2016-2017学年高一上学期化学期末考试试卷
- 山东省淄博七中2016-2017学年高一上学期化学期中考试试卷
- 河南省焦作市2016-2017学年高一上学期化学期中考试试卷
- 山东省淄博市淄川一中2016-2017学年高一上学期化学期中考试试卷
- 山东省德州市陵城一中2016-2017学年高一上学期化学期中考试试卷
- 山东省淄博六中2016-2017学年高二上学期化学期中考试试卷
- 山东省临沂市蒙阴一中2016-2017学年高二上学期化学期中考试试卷
- 2016-2017学年山东省烟台市高一下学期期中化学试卷
- 2016-2017学年山东省德州市夏津一中高一下学期期中化学试卷
- 2016-2017学年山东省德州市武城二中高一下学期期中化学试卷(普通班)
-
1、根据实验目的设计方案并进行实验,观察到相关现象,下列方案设计、结论均正确的是( )
实验目的
方案设计
现象
结论
A
探究金属、的金属性强弱
将金属、分别切成体积相等的颗粒,投入蒸馏水中
金属与水反应更加剧烈
的金属性强于
B
判断的化学键类型
将固体溶于水,进行导电性实验
溶液可导电
中含有离子键
C
探究浓硝酸与炭在加热条件下能否反应
将红热的木炭投入浓硝酸中
产生红棕色气体
炭与浓硝酸在加热条件下反应生成
D
探究有机物中官能团之间的影响
分别向丙烯酸乙酯()和α-氰基丙烯酸乙酯[]中滴入水
前者无明显现象,后者快速固化
氰基活化双键,使其更易发生加聚反应
A、A B、B C、C D、D -
2、常温下,往0.35mol/L溶液中通入。
已知: , , ,
下列说法不正确的是( )
A、通入一定量后溶液 , 未出现沉淀 B、往溶液中加盐酸酸化,将有生成 C、通入一定量后溶液中 , 滴入酚酞试剂,溶液一直呈无色 D、已知自然条件下,饱和碳酸溶液的 , 则自然条件下饱和碳酸溶液中存在 -
3、乙醛与氢氰酸( , 弱酸)能发生加成反应,生成2-羟基丙腈,历程如下:

下列说法不正确的是( )
A、因氧原子的电负性较大,醛基中的碳原子带部分正电荷,与作用 B、易挥发且有剧毒,是该反应不在酸性条件下进行的原因之一 C、往丙酮与反应体系中加入一滴溶液,反应速率明显加快,因此碱性越强,上述反应越容易进行 D、与加成的反应速率: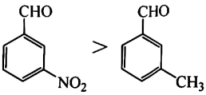
-
4、高氯酸在化工生产中有广泛应用,工业上以为原料制备高氯酸的原理如图所示。下列说法正确的是( )
 A、上述装置中,f极为光伏电池的正极 B、a、b处均通入溶液 C、d处得到较浓的溶液,c处得到HClO4溶液 D、若转移2mol电子,理论上生成100.5gHClO4
A、上述装置中,f极为光伏电池的正极 B、a、b处均通入溶液 C、d处得到较浓的溶液,c处得到HClO4溶液 D、若转移2mol电子,理论上生成100.5gHClO4 -
5、有机金属氯化物由原子序数依次增大的短周期主族元素X、Y、Z、M、N组成,部分结构如图所示,基态原子M核外电子所占据原子轨道全充满,N元素的价层电子排布式为。下列说法不正确的是( )
 A、Z与N可形成化合物、 B、最简单氢化物的沸点: C、M元素的第一电离能比同周期相邻元素的大 D、离子中Y发生杂化
A、Z与N可形成化合物、 B、最简单氢化物的沸点: C、M元素的第一电离能比同周期相邻元素的大 D、离子中Y发生杂化 -
6、有机物L的合成路线(反应条件和其他产物已经略去)如下图所示,下列说法不正确的是( )
 A、1molX最多能与2mol(水溶液)发生反应 B、在Z→M的过程中,发生还原反应,M的结构简式为 C、Y能使溴水和酸性高锰酸钾溶液褪色,但褪色原理不同 D、N和L均难溶于水
A、1molX最多能与2mol(水溶液)发生反应 B、在Z→M的过程中,发生还原反应,M的结构简式为 C、Y能使溴水和酸性高锰酸钾溶液褪色,但褪色原理不同 D、N和L均难溶于水 -
7、下列指定反应与方程式不相符的是( )A、淀粉碘化钾溶液在空气中变蓝: B、用惰性电极电解溶液,阴极的电极反应式: C、甘油与硝酸发生酯化反应:
 D、在酸催化下,苯酚与甲醛反应生成羟甲基苯酚:
D、在酸催化下,苯酚与甲醛反应生成羟甲基苯酚:
-
8、关于有机物检测,下列说法正确的是( )A、分子式为的有机物不能使酸性溶液褪色,则该有机物一定不是醇 B、可用溴水鉴别甲酸水溶液、甲醛水溶液和甲苯 C、与的核磁共振氢谱谱图是完全相同的 D、淀粉水解液碱化后,加入新制氢氧化铜并加热,出现砖红色沉淀,说明淀粉水解生成了还原性糖
-
9、某实验小组为制备1-氯-2-甲基丙烷(沸点69℃),将2-甲基-1-丙醇和溶于中,加热回流(伴有气体产生)。反应完全后倒入冰水中分解残余的 , 分液收集层,再用无水干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的部分装置(夹持及加热装置略)如下图,下列说法不正确的是( )
 A、装置①在加热回流时,需加入沸石或碎瓷片 B、装置②与装置①的冷凝管上端相连,因气体极易溶于水,需将尾气处理装置设计成防倒吸 C、装置③在分液前无法区分水层与有机层时,可向分液漏斗中滴水,若上层无水滴通过轨迹,则上层为水层 D、沸点为39.8℃,为增强冷凝效果,可使用装置④的蒸馏装置,对圆底烧瓶进行控制温度的温水浴加热
A、装置①在加热回流时,需加入沸石或碎瓷片 B、装置②与装置①的冷凝管上端相连,因气体极易溶于水,需将尾气处理装置设计成防倒吸 C、装置③在分液前无法区分水层与有机层时,可向分液漏斗中滴水,若上层无水滴通过轨迹,则上层为水层 D、沸点为39.8℃,为增强冷凝效果,可使用装置④的蒸馏装置,对圆底烧瓶进行控制温度的温水浴加热 -
10、类比和推理是学习化学的重要方法,下列结论合理的是( )
已知
结论
A
15—冠—5(冠醚)能识别
12—冠—4(冠醚)能识别
B
酸性:三氟乙酸>三氯乙酸
酸性:氢氟酸>氢氯酸
C
溶解度:
D
晶体硅是半导体材料
晶体硅的化学键含金属键成分
A、A B、B C、C D、D -
11、《开宝本草》记载“取钢煅作叶,如笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣”。铁华粉[主要成分为]可用如下方法检测。下列相关说法不正确的是( )
 A、气体X为 B、铁华粉中含有铁单质 C、由上述实验可知,结合的能力强于 D、制备铁华粉的主要反应为
A、气体X为 B、铁华粉中含有铁单质 C、由上述实验可知,结合的能力强于 D、制备铁华粉的主要反应为 -
12、下列各组离子在给定溶液中能大量共存的是( )A、1.0mol/L氨水溶液()中:、、 B、1.0mol/L氯化钠溶液()中:、、 C、0.1mol/L碳酸钠溶液()中:、、 D、0.1mol/L酸性高锰酸钾溶液()中:、、
-
13、具有强氧化性,可发生反应:。下列说法不正确的是( )(为阿伏加德罗常数的值)A、既是氧化产物,又是还原产物 B、仅作氧化剂 C、生成1mol转移电子的数目为 D、实验室不可用加热固体的方法制备
-
14、下列表示正确的是( )A、的价层电子对互斥(VSEPR)模型:
 B、的电子式:
C、基态的价层电子轨道表示式:
B、的电子式:
C、基态的价层电子轨道表示式: D、
D、 的名称:乙二酸乙二酯
的名称:乙二酸乙二酯
-
15、碳酸氢钠常用作食用碱或工业用碱,下列说法不正确的是( )A、向碳酸氢钠固体中加入少量水后,会出现吸热现象 B、碳酸氢钠溶液呈碱性,加入溶液后,产生较多氨气 C、分别同时加热等量碳酸钠和碳酸氢钠固体,碳酸氢钠先发生分解 D、往饱和碳酸钠溶液中通入 , 会产生碳酸氢钠沉淀
-
16、常温常压下,下列物质为气态的是( )A、甲醇 B、甲醛 C、甲酸 D、水
-
17、伯舒替尼(J)是一种激酶抑制剂,可用于治疗成人慢性粒细胞性白血病。其一种合成路线如图。请回答下列问题:
 (1)、A→B的反应类型为 , 设计A→B、G→H的目的为。(2)、物质B中所含官能团的名称为 , C的结构简式为。(3)、
(1)、A→B的反应类型为 , 设计A→B、G→H的目的为。(2)、物质B中所含官能团的名称为 , C的结构简式为。(3)、 的化学名称为。 (4)、D→E的反应方程式为。(5)、K比化合物
的化学名称为。 (4)、D→E的反应方程式为。(5)、K比化合物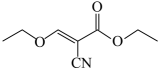 少两个H原子,K的芳香族同分异构体中,符合下列条件的结构有种,核磁共振氢谱图上只有3组峰的结构简式为(写一种即可)。
少两个H原子,K的芳香族同分异构体中,符合下列条件的结构有种,核磁共振氢谱图上只有3组峰的结构简式为(写一种即可)。a.苯环上有4个取代基 b.与苯环直接相连 c.能与氯化铁溶液发生显色反应
(6)、 是一种新型的整合酶链转移抑制剂,设计以
是一种新型的整合酶链转移抑制剂,设计以 、
、 为含碳原料制备
为含碳原料制备 的合成路线(其他无机试剂或溶剂等任选)。
的合成路线(其他无机试剂或溶剂等任选)。 -
18、为了消除含金硫精矿中硫对氰化浸出产生的不利影响,使被硫化物包裹的金得以解离,获得孔隙率较高的氧化焙烧渣,需对含金硫精矿进行氧化焙烧预处理。已知焙烧过程中发生的反应有:
反应1:
反应2:
反应3:
(1)、= , 有利于反应3自发进行的条件为(填“高温”或“低温”)。(2)、焙烧温度和时间对硫的脱除率和金的浸出率的影响如图。
最佳的焙烧温度为℃;最佳焙烧时间为2h,理由是。
(3)、在密闭容器中充入一定量的和进行反应,测得平衡时的体积分数随X的变化关系如图。
①X表示的是(填“温度”或“压强”),判断的理由是。
②下列条件能判断反应1达到平衡状态的是(填标号)。
a.的生成速率与的消耗速率相等
b.和浓度相等
c.容器中气体的平均摩尔质量不变
d.的质量保持不变
(4)、℃下,在恒压密闭容器中充入1.5mol和3.5mol进行反应,已知起始压强为140kPa,经过10min达到平衡,测得生成、的物质的量均为0.2mol。①0~10min内,分压的平均变化率为。②℃下,反应1的压强平衡常数=(为用分压表示的平衡常数,分压=总压×物质的量分数,列计算式即可)。
-
19、SrCO3可用于金属冶炼和锶盐制备等。以天青石(成分为SrSO4、BaSO4、CaSO4、SiO2)为原料制备SrCO3的工艺流程如图。

已知:常温下,Ksp(SrSO4)=3.2×10-7、Ksp(BaSO4)=1.0×10-10、Ksp(SrCO3)=1.6×10-9。
回答下列问题:
(1)、天青石磨成粉的目的是。(2)、天青石粉中的SrSO4与氨水、NH4HCO3溶液反应的离子方程式为;NH4HCO3溶液中c(NH3·H2O)+c(OH-)+c()(填“>”“<”或“=”)c(H2CO3)+c(H+);将滤液1蒸发浓缩、冷却结晶可得副产物(填化学式)。(3)、滤渣的主要成分为 (填化学式)。(4)、打浆酸溶后的滤液加热至95~100C.加NaOH溶液调pH=14的目的是。(5)、碱析后获得Sr(OH)2的操作为。(6)、以SrCO3和TiO2为原料,在1300~1500℃下煅烧,可制得优良的光学材料及人造宝石SrTiO3.SrTiO3的晶胞结构如图所示,设NA为阿伏加德罗常数的值,晶胞参数为apm。
①生成SrTiO3的化学方程式为。
②SrTiO3晶体的密度为。
-
20、钢铁表面发黑(在钢铁表面形成一层致密的氧化物膜)可提高其耐磨、耐腐蚀性能。某实验小组欲利用下列装置进行发黑实验,并探究氧化物成分。

已知:实验过程中产生了一种能使湿润的红色石蕊试纸变蓝的气体。
(1)、实验开始前需将铁粉依次放入热的碳酸钠溶液和饱和氯化铵溶液中进行处理,其目的分别是和。(2)、向圆底烧瓶中逐滴滴入、的混合溶液至过量,在140℃下处理15~90min。①盛装混合溶液的仪器为。
②下列加热方法中,最合适的为(填标号)。
A.水浴 B.油浴 C.酒精灯
(3)、用乙装置收集产生的气体,请在装置中补全仪器。(4)、试剂X可以为。(5)、探究甲装置中固体产物(无铁单质剩余)成分。取少量洗涤后的固体产物于试管中,滴入足量的稀硫酸,实验中固体全部溶解,无气体生成。将生成的溶液分成两份,分装于a、b两支试管中。
①向a试管中滴入酸性高锰酸钾溶液,溶液紫红色褪去,说明a试管中含有(填离子符号)。
②不用硝酸溶解固体的原因为。
③向b试管中滴入(填化学式)溶液,溶液变为血红色,说明b试管中含有(填离子符号)。
(6)、根据以上信息,推测圆底烧瓶中进行发黑实验时可能发生反应的化学方程式:。