相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列陈述Ⅰ和陈述Ⅱ均正确,且有因果关系的是
选项
陈述Ⅰ
陈述Ⅱ
A
使用纯碱溶液去油污
Na2CO3水解使溶液显碱性
B
丙三醇用于配制化妆品
丙三醇能与高级脂肪酸反应生成脂
C
液氨可用作制冷剂
氨气易溶于水
D
工业用电解熔融AlCl3制取金属铝
金属铝的还原性很强
A、A B、B C、C D、D -
2、反应 放热且产生气体,可用于冬天石油开采。设NA为阿伏加德罗常数的值。下列叙述正确的是A、1mol NH4Cl含有共价键目为 5NA B、1.8gH2O 含有的质子数目为 NA C、浓度均为 和 NaNO2混合溶液中,Na+数目为0.1NA D、上述反应中,每生成0.1mol N2转移的电子数目为0.6NA
-
3、下列实验装置(部分夹持装置已略去) 可以达到对应实验目的是
目的
A. 制备氢氧化铁胶体
B.实验室制备氨气
C. 推断 Cl、C、Si的非金属性强弱
D. 制备并收集NO
装置



 A、A B、B C、C D、D
A、A B、B C、C D、D -
4、科学家合成出了一种高效电解质,其结构如图所示,其中W、Y、X、Z、Q均为短周期主族元素,且原子序数依次增大,X与Q同族,Y和Z的原子序数之和与Q相等。下列说法正确的是
 A、Q的氧化物对应水化物均为强酸 B、元素非金属性的顺序为Z>Y>X C、W和X形成的化合物溶于水呈碱性 D、该电解质的阴离子中所有原子均满足8电子稳定结构
A、Q的氧化物对应水化物均为强酸 B、元素非金属性的顺序为Z>Y>X C、W和X形成的化合物溶于水呈碱性 D、该电解质的阴离子中所有原子均满足8电子稳定结构 -
5、部分含镁或含铜物质的分类与相应化合价关系如图所示,其中e为氯化物。下列推断不合理的是
 A、转化a→c→d在给定条件下均可一步反应实现 B、b可与盐酸反应生成e和a,b既有氧化性又有还原性 C、新制的d可用于检验葡萄糖中的醛基 D、经过e→d→e→a的转化可实现从海水中提取镁
A、转化a→c→d在给定条件下均可一步反应实现 B、b可与盐酸反应生成e和a,b既有氧化性又有还原性 C、新制的d可用于检验葡萄糖中的醛基 D、经过e→d→e→a的转化可实现从海水中提取镁 -
6、山奈酚是中药柴胡的药物成分之一,结构如图所示,下列有关山奈酚叙述正确的是
 A、该物质属于芳香烃 B、分子中所有碳原子一定共平面 C、不能使溴水和酸性 KMnO4溶液褪色 D、1mol 山奈酚最多与 3molNaOH 反应
A、该物质属于芳香烃 B、分子中所有碳原子一定共平面 C、不能使溴水和酸性 KMnO4溶液褪色 D、1mol 山奈酚最多与 3molNaOH 反应 -
7、下列劳动项目与所述的化学知识没有关联的是
选项
劳动项目
化学知识
A
厨师用盐卤(主要成分MgCl2)点豆腐
豆浆中的蛋白质发生聚沉
B
工人用 FeCl3溶液作腐蚀液制作印刷电路板
金属铁的还原性比金属铜强
C
面包师用小苏打粉作膨松剂烘培糕点
NaHCO3受热易分解放出CO2
D
检测员用AgNO3滴定法测定水样中 Cl-的含量
Ag+与Cl-反应生成AgCl沉淀
A、A B、B C、C D、D -
8、化学处处呈现美。下列说法不正确的是A、加热固体碘出现大量紫色蒸气时,共价键断裂 B、茉莉花的芳香扑鼻而来,体现了分子是运动的 C、烟花燃放时呈现出五颜六色,是不同金属元素的焰色所致 D、甲烷分子为正四面体结构,四个氢原子完美对称,其键角和键长均相等
-
9、下列说法或化学用语表述正确的是A、N2的电子式: N⋮⋮N B、CH2Cl2中的共价键类型:非极性键和极性键 C、CO2的空间结构: V形 D、反-2-丁烯的结构简式:

-
10、非物质文化遗产是古代劳动人民的智慧结晶。下列说法正确的是A、蒸馏酒传统酿造技艺:利用酒和水的密度不同, 蒸馏提高酒精度 B、斑铜制作技艺:在铜中掺杂金、银等金属,斑铜的熔点比纯铜高 C、桑蚕丝织技艺:蚕丝的主要成分属于高分子化合物 D、桐油纸伞制作技艺:桐油(由桐树种子压榨而得)的主要成分是烃
-
11、近年我国在科技领域不断取得新成就。下列说法正确的是A、利用CO2合成脂肪酸,实现了无机小分子向有机高分子的转变 B、“华龙一号”核反应堆所用铀棒中含有的 与 互为同位素 C、“破风 8676”的5G射频收发芯片的主要成分是 SiO2 D、“深海一号”开采深海的天然气可作清洁燃料, 实现零碳排放
-
12、文化岭南,古韵悠长。下列西汉南越王博物馆馆藏珍宝中,主要由无机非金属材料制成的是




A. 西汉文帝行玺金印
B. 漆木双面彩绘屏风
C. 透雕龙凤纹重环玉佩
D. 错金铭文铜虎节
A、A B、B C、C D、D -
13、曾侯乙编钟是战国早期的一套大型礼乐重器,在1978年出土于湖北随州擂鼓墩曾侯乙墓。下列有关曾侯乙编钟的叙述错误的是A、主要材料是合金 B、应保存在干燥通风环境中 C、在土壤中主要发生化学腐蚀 D、表面绿色物质的主要成分是
-
14、设为阿伏加德罗常数的值,下列叙述正确的是A、16g与的混合物中含氧原子数为 B、1mol Na完全转化为时,失去的电子数目为2 C、标准状况下,22.4L中含有的分子数为 D、1mol/L溶液中离子总数为3
-
15、下列变化中,需要加入氧化剂才能实现的是A、CuCl2→Cu B、Na2CO3→CaCO3 C、SO2→SO3 D、MnO4-→Mn2+
-
16、某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐渐加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的下列说法中,不正确的是
 A、AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质 B、B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 C、BC段溶液的导电能力不断增大,主要是由于过量的H2SO4电离出的离子导电 D、a时刻Ba(OH)2溶液与稀硫酸恰好完全中和
A、AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质 B、B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 C、BC段溶液的导电能力不断增大,主要是由于过量的H2SO4电离出的离子导电 D、a时刻Ba(OH)2溶液与稀硫酸恰好完全中和 -
17、为研究Na的性质,进行如下实验
装置
实验
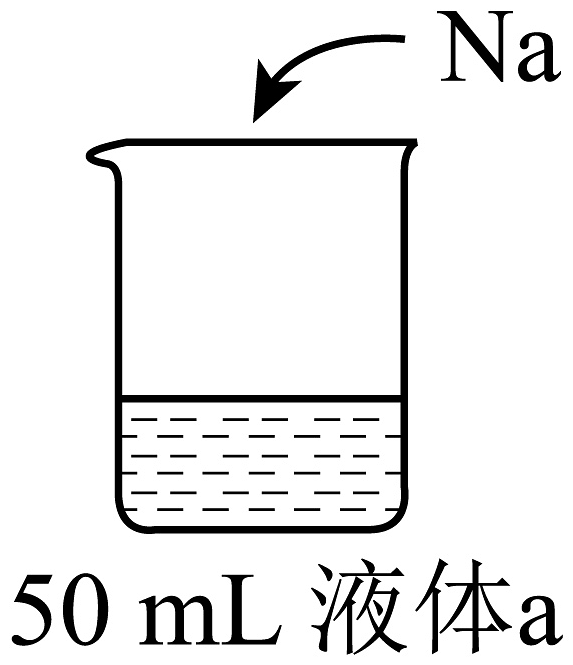
液体a
现象
蒸馏水
Ⅰ.Na浮在液面上,剧烈反应,产生少量白雾
0.1 mol·L-1 盐酸
Ⅱ.Na浮在液面上,反应比Ⅰ中剧烈,产生白雾
浓盐酸
Ⅲ.Na浮在液面上,反应比Ⅰ中缓慢,产生大量白雾,烧杯底部有白色固体
下列说法中,不正确的是
A、Ⅰ中现象说明Na与水反应放热 B、Ⅰ中反应的离子方程式为 C、Ⅲ中白雾比Ⅱ中多,说明Ⅲ中反应放热比Ⅱ中更多 D、推测Ⅲ中反应缓慢可能与c(Cl-)以及生成的白色固体有关 -
18、下列离子方程式书写正确的是A、少量二氧化碳通入澄清石灰水:Ca2++2OH-+CO2=CaCO3↓+H2O B、过氧化钠溶于水:Na2O2+H2O=2NaOH+O2↑ C、盐酸溶液中加入铁粉:6H++2Fe=2Fe3++3H2↑ D、碳酸钙和盐酸反应:+2H+=H2O+CO2↑
-
19、下列仪器不能加热的是A、
 B、
B、 C、
C、 D、
D、
-
20、有机化合物H是一种医药合成中间体,其合成路线如图所示:

回答下列问题:
(1)、A含有的官能团名称:。(2)、B的结构简式为 , C的分子式:。(3)、C→D、E→G的反应类型分别为。(4)、D→F分两步完成,其中D与NaOH反应的化学方程式为。(5)、H在酸或碱存在并加热的条件下可以发生水解反应,若在盐酸作用下水解,其生成物中属于盐的结构为。(6)、溴代乙酸乙酯()有多种同分异构体,其中与其具有相同官能团的结构还有种(不考虑立体异构、不考虑直接与相连)。(7)、 是一种常见的药物合成中间体。请参照以上合成路线,设计以
是一种常见的药物合成中间体。请参照以上合成路线,设计以 为原料合成
为原料合成 的路线(其他试剂任选)。
的路线(其他试剂任选)。