相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、核心元素的化合价及类别是研究物质性质的两个重要视角。硫及其化合物的分类与相应硫元素的化合价关系如图所示。下列说法错误的是
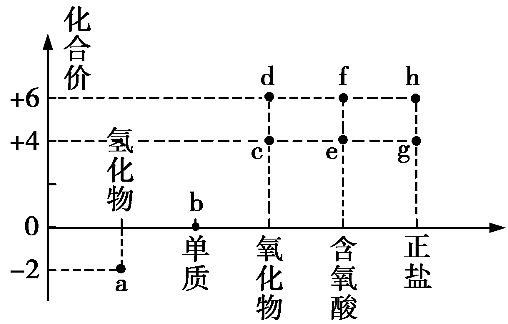 A、适量的c可作为葡萄酒的添加剂 B、常温下,a与f的浓溶液反应可生成b和c C、将c通入紫色石蕊试液中,溶液先变红后褪色 D、在自然界中,部分的c会转化成d,最后转化为f或h
A、适量的c可作为葡萄酒的添加剂 B、常温下,a与f的浓溶液反应可生成b和c C、将c通入紫色石蕊试液中,溶液先变红后褪色 D、在自然界中,部分的c会转化成d,最后转化为f或h -
2、短周期元素W、X、Y、Z的原子序数依次增大,W、Z位于同主族,四种元素组成的一种化合物的结构式为
 ,下列说法错误的是 A、X的最简单氢化物的稳定性比W的强 B、X与Y形成的是离子化合物 C、W与Y形成的化合物中可能含有共价键 D、简单离子半径:
,下列说法错误的是 A、X的最简单氢化物的稳定性比W的强 B、X与Y形成的是离子化合物 C、W与Y形成的化合物中可能含有共价键 D、简单离子半径: -
3、有四种碳架结构(氢原子未表示出来)如下的烃,下列描述不正确的是
a.
 ;b.
;b. ;c.
;c. ;d.
;d. A、a和d互为同分异构体 B、b和c是同系物 C、c与氯气光照最多生成10种有机产物 D、a可以使溴水褪色
A、a和d互为同分异构体 B、b和c是同系物 C、c与氯气光照最多生成10种有机产物 D、a可以使溴水褪色 -
4、下列实验装置不能达到相应实验目的的是
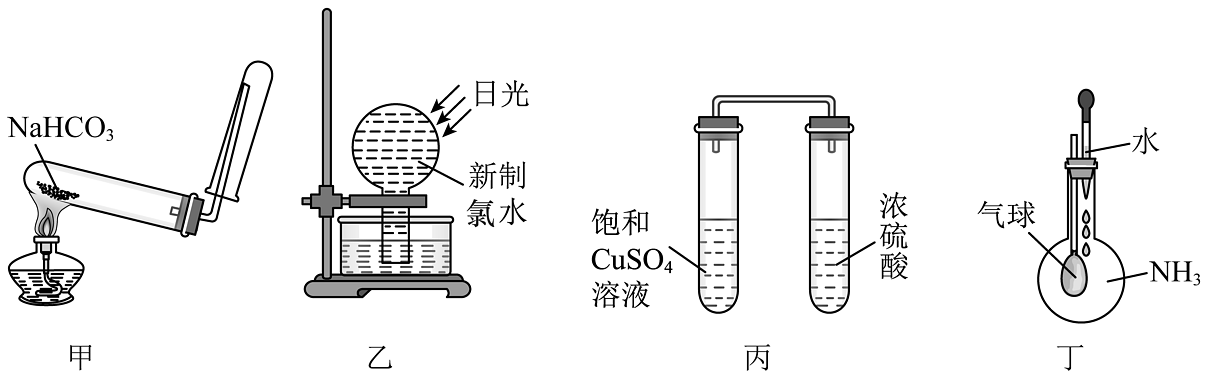 A、用甲装置制备并收集 B、用乙装置验证次氯酸的不稳定性 C、用丙装置验证浓硫酸具有吸水性 D、用丁装置验证在水中的溶解度大
A、用甲装置制备并收集 B、用乙装置验证次氯酸的不稳定性 C、用丙装置验证浓硫酸具有吸水性 D、用丁装置验证在水中的溶解度大 -
5、金属钛(Ti)抗腐蚀性能好,在高温环境下具有强还原性。以金红石(主要成分为)为原料生产钛的工艺流程如下:

下列说法错误的是
A、金属钛在常温下难与反应 B、高温下,钠可以与溶液反应制备金属钛 C、②中发生的化学反应属于置换反应 D、反应①中钛的化合价没有发生改变 -
6、下列有关基本营养物质的说法错误的是A、糖类、油脂和蛋白质均仅由C、H、O三种元素组成 B、向鸡蛋清溶液中加入几滴醋酸铅溶液,产生白色沉淀 C、植物油含不饱和脂肪酸甘油酯,能使溴的四氯化碳溶液褪色 D、在加热条件下,葡萄糖可与新制的氢氧化铜反应产生砖红色沉淀
-
7、生活中处处有化学,下列化学在生活中的应用与所涉及的化学知识相符的是
选项
实际应用
化学知识
A
白醋用来除去水壶中的水垢
酸性:醋酸>碳酸
B
用于漂白纸浆
具有还原性
C
用氢氟酸溶蚀玻璃生产磨砂玻璃
氢氟酸具有强氧化性
D
浓氨水用于检验氯气管道泄漏
具有强烈的刺激性
A、A B、B C、C D、D -
8、下列化学用语正确的是A、甲基的电子式
 B、S2-的离子结构示意图
B、S2-的离子结构示意图 C、含10个中子氧的核素符号
D、乙酸的结构简式
C、含10个中子氧的核素符号
D、乙酸的结构简式
-
9、下列关于资源开发利用的说法错误的是A、石油经分馏后得到的汽油是混合物 B、煤的干馏、气化和液化均为化学变化 C、工业上常采用铝热反应冶炼铁 D、天然气和液化石油气等清洁燃料的主要成分是烃类
-
10、书法是中华文化之瑰宝,其美尽在笔墨纸砚之间。下列关于传统文房四宝说法正确的是
A
B
C
D




制笔用的狼毫主要成分是蛋白质
墨汁是一种水溶液
宣纸是合成高分子材料
砚石的成分与水晶相同
A、A B、B C、C D、D -
11、近年来,广州持续推进碧水蓝天保卫战。下列做法不利于生态保护与建设的是A、推广新能源汽车,倡导绿色出行 B、加强城市生活污水与雨水的分流收集处理,遏制水体富营养化 C、移除人行道边遮天蔽日的大树,使人们抬头便可看到蓝天白云 D、对尾气排放超标的汽车强制加装催化处理装置,减轻氮氧化物污染及光化学烟雾
-
12、辛勤劳动才能创造美好生活。下列劳动场景中,不涉及氧化还原反应的是




A.冶炼钢铁
B.海水晒盐
C.古法酿酒
D.用过氧化物消毒
A、A B、B C、C D、D -
13、科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为。阿伏加德罗常数的值为。下列说法错误的是
 A、晶体最简化学式为 B、晶体中与最近且距离相等的有8个 C、晶胞中B和C原子构成的多面体有12个面 D、晶体的密度为
A、晶体最简化学式为 B、晶体中与最近且距离相等的有8个 C、晶胞中B和C原子构成的多面体有12个面 D、晶体的密度为 -
14、设为阿伏加德罗常数的值。下列说法正确的是A、蔗糖完全水解得到的葡萄糖分子数为 B、常温常压下,中含有的碳碳双键数目为 C、乙醇溶液与足量钠反应生成的分子数为 D、光照条件下,(标准状况下)与足量氯气反应生成的分子数小于
-
15、在实验室采用如图装置制备气体,合理的是

化学试剂
制备的气体
A
B
(浓)
C
D
(浓)
A、A B、B C、C D、D -
16、古医典中富含化学知识,下列描述与氧化还原反应无关的是A、汞的性质:汞得硫则赤如丹 B、强水(硝酸):用水入五金皆成水 C、熬制胆矾:熬胆矾铁釜,久之亦化为铜 D、制取黄铜:红铜(Cu)六斤、倭铅(Zn)四斤,先后入罐熔化,冷定取出,即成黄铜
-
17、以铁镍合金(含少量铜)为原料,生产电极材粗的部分工艺流程如下:

已知:常温下, , , , 。
回答下列问题:
(1)、基态Ni原子价层电子轨道表示式是;Cu原子位于周期表中区。(2)、“酸溶”时Ni转化为 , 该过程中温度控制在70~80℃的原因是。(3)、“氧化”时的作用是(用离子方程式表示)。(4)、“除铜”时若选用NaOH溶液,会导致部分也产生沉淀,当常温时溶液中、沉淀同时存在时,溶液中。(5)、“沉镍”时得到碳酸镍沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得 , 该反应的化学方程式是。(6)、金属镍的配合物用途广泛,其中配体CO与结构相似,CO分子内σ键与π键个数之比为。 -
18、常温下,用溶液滴定溶液所得滴定曲线如图。下列说法正确的是
 A、该滴定实验中,选择甲基橙作指示剂的滴定误差小 B、点①所示溶液中: C、点②所示溶液中: D、点③所示溶液中:
A、该滴定实验中,选择甲基橙作指示剂的滴定误差小 B、点①所示溶液中: C、点②所示溶液中: D、点③所示溶液中: -
19、溴苯可用于生产镇痛解热药和止咳药,其制备、纯化流程如图。下列说法错误的是
 A、“过滤”可除去未反应的铁粉 B、“除杂”使用饱和NaHSO3溶液可除去剩余的溴单质 C、“干燥”时可使用浓硫酸作为干燥剂 D、“蒸馏”的目的是分离苯和溴苯
A、“过滤”可除去未反应的铁粉 B、“除杂”使用饱和NaHSO3溶液可除去剩余的溴单质 C、“干燥”时可使用浓硫酸作为干燥剂 D、“蒸馏”的目的是分离苯和溴苯 -
20、用分液漏斗可以分离的一组液体混合物是A、溴和苯 B、苯和溴苯 C、水和硝基苯 D、苯和汽油