相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、甲酸(HCOOH)可在纳米级Pd表面分解为活性H2和CO2 , 经下列历程实现NO的催化还原。已知Fe(Ⅱ)、Fe(Ⅲ)表示Fe3O4中二价铁和三价铁。下列说法不正确的是
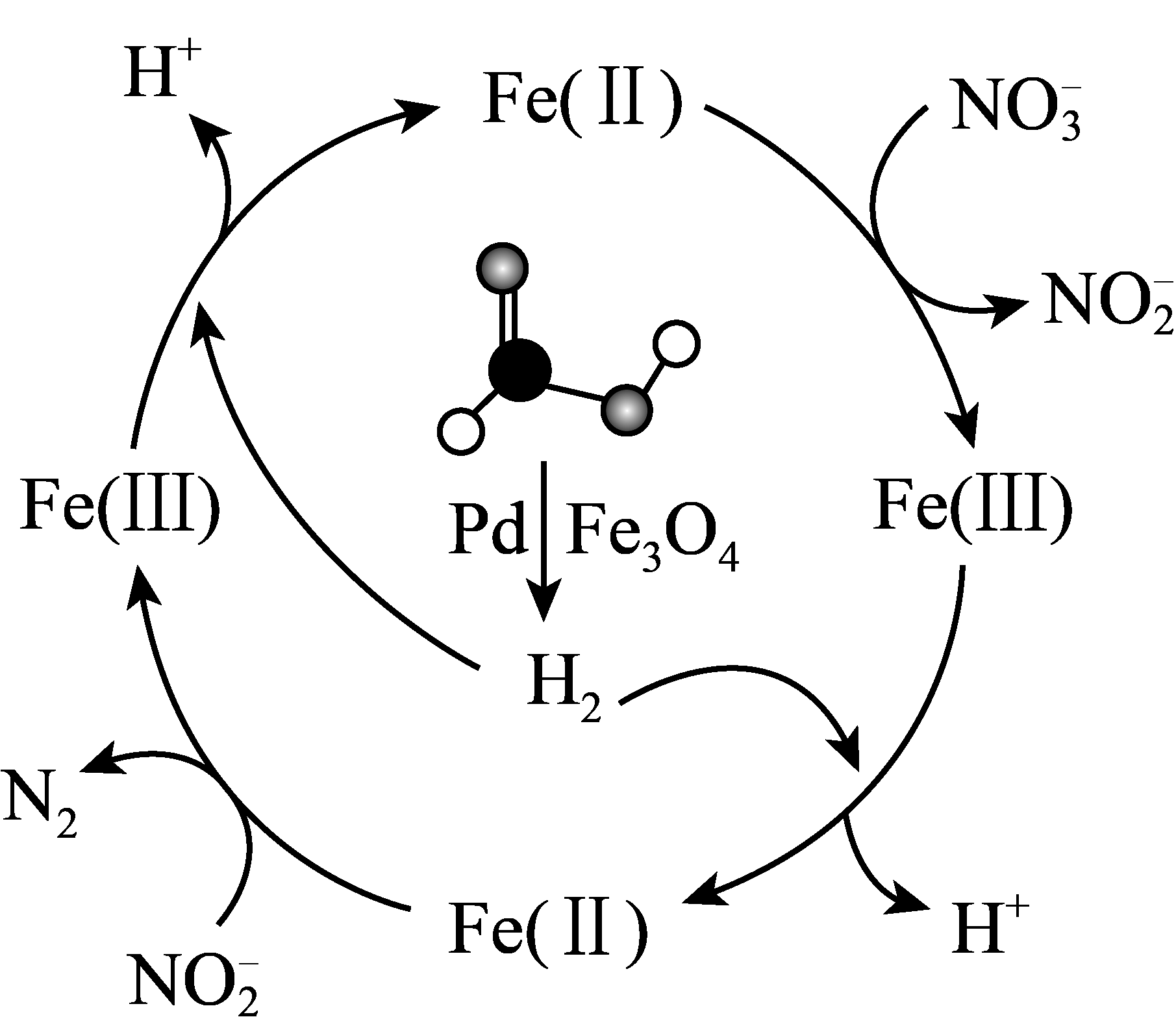 A、生产中将催化剂处理成纳米级颗粒可增大甲酸分解的速率 B、在整个历程中,每1molH2可还原2molNO C、HCOOH分解时,只有极性共价键发生了断裂 D、反应历程中生成的H+可调节体系pH,有增强NO氧化性的作用
A、生产中将催化剂处理成纳米级颗粒可增大甲酸分解的速率 B、在整个历程中,每1molH2可还原2molNO C、HCOOH分解时,只有极性共价键发生了断裂 D、反应历程中生成的H+可调节体系pH,有增强NO氧化性的作用 -
2、下列物质性质实验对应的化学反应的离子方程式书写正确的是A、Fe与FeCl3溶液反应:Fe+Fe3+=2Fe2+ B、大理石与醋酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ C、将Na2O2固体投入H218O中:2Na2O2+2H218O=4Na++218OH-+2OH-+O2↑ D、向Ba(OH)2溶液中加入过量NaHSO4溶液:Ba2++OH-+H++SO=BaSO4↓+H2O
-
3、某实验小组为制备并探究SO2的化学性质,下列装置中不能达到实验目的的是




A.制取SO2
B.验证SO2的还原性
C.验证SO2的漂白性
D.吸收尾气
A、A B、B C、C D、D -
4、“光荣属于劳动者,幸福属于劳动者。”下列劳动项目与所述化学知识没有关联的是
选项
劳动项目
化学知识
A
用食醋清除水壶中的水垢
醋酸的酸性强于碳酸
B
制作豆腐的过程中煮沸豆浆
加热条件下,蛋白质可发生变性
C
制作面点时加入食用纯碱
NaHCO3能与发酵过程中产生的酸发生反应
D
清洗铁锅后及时擦干
减缓铁锅因发生吸氧腐蚀而生锈
A、A B、B C、C D、D -
5、海带中含有碘元素,从海带中提取碘的实验过程如图所示:

下列说法正确的是
A、海带中碘元素以I2形式存在 B、操作①可除去海带中的有机物 C、操作③为过滤,操作⑥为萃取 D、操作⑤用到的玻璃仪器有普通漏斗 -
6、绿色有机合成具有原子经济性高、充分利用资源、减少污染等特点。下列说法不正确的是
 A、化合物I分子中所有碳原子可能共平面 B、1mol化合物II最多能与4molH2发生加成反应 C、化合物I和III均能使酸性KMnO4溶液褪色 D、化合物III能与FeCl3溶液发生显色反应
A、化合物I分子中所有碳原子可能共平面 B、1mol化合物II最多能与4molH2发生加成反应 C、化合物I和III均能使酸性KMnO4溶液褪色 D、化合物III能与FeCl3溶液发生显色反应 -
7、安全无小事。下列操作不符合实验安全要求的是A、眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗 B、实验中剩余的少量金属钠,可以放回原试剂瓶 C、闻气体时,用手在瓶口轻轻扇动,使少量气体飘进鼻孔 D、苯酚沾到皮肤上,立即用酒精擦洗后再用水冲洗
-
8、结构决定性质。下列性质差异与结构因素不匹配的是
选项
性质差异
结构因素
A
在CCl4中的溶解度:I2>ICl
分子极性
B
熔点:SiC(2830℃)>SiF4(-90℃)
晶体类型
C
沸点:对氨基苯甲醛>邻氨基苯甲醛
氢键类型
D
电离常数Ka:F3CCOOH>Cl3CCOOH
范德华力
A、A B、B C、C D、D -
9、化学推动着社会的进步和人类的发展。下列说法正确的是A、通过煤的干馏等物理变化可以获得多种化工原料 B、红外光谱可用于测定新型材料的相对分子质量 C、植物光合作用涉及氧化还原反应 D、光伏发电系统工作时将电能转化为化学能
-
10、文物是文化传承的重要载体。下列在深圳博物馆展出的文物中,主要材质为有机高分子的是



蟠螭纹铜编钟
彩绘仕女陶俑
龙首谷纹玉玦
唐王右丞诗集
A
B
C
D
A、A B、B C、C D、D -
11、含有冠醚环的聚合物膜能够高效吸附分离某些阳离子。一种含冠醚环的聚酰亚胺薄膜吸附分离Li+的过程如图。下列说法正确的是
 A、冠醚环与Li+之间的作用是离子键 B、冠醚环中碳氧键为π键 C、该聚酰亚胺薄膜可在强碱性环境中稳定工作 D、若要设计K+的吸附分离膜,需增大冠醚环孔径
A、冠醚环与Li+之间的作用是离子键 B、冠醚环中碳氧键为π键 C、该聚酰亚胺薄膜可在强碱性环境中稳定工作 D、若要设计K+的吸附分离膜,需增大冠醚环孔径 -
12、T℃时,恒容密闭容器中发生反应PCl3(g)+Cl2(g)PCl5(g) △H<0,下列说法正确的是A、该反应的△S<0,在高温下才能自发进行 B、反应物断键所需总能量大于生成物成键所放出总能量 C、增大反应物浓度能增加单位体积内的有效碰撞次数 D、平衡后,向该容器中充入氦气,平衡向正反应方向移动
-
13、一定条件下白磷和红磷可以相互转化,白磷转化为红磷的能量变化如图所示,下列说法错误的是
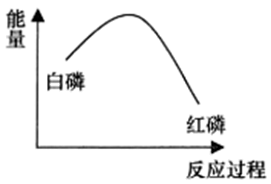 A、白磷转化为红磷是放热反应 B、红磷比白磷稳定性更高 C、等质量的红磷所含有的能量高于白磷 D、相同物质的量的白磷和红磷完全燃烧,白磷释放的热量多
A、白磷转化为红磷是放热反应 B、红磷比白磷稳定性更高 C、等质量的红磷所含有的能量高于白磷 D、相同物质的量的白磷和红磷完全燃烧,白磷释放的热量多 -
14、“能源”是人们生活中不可或缺的一部分,化学能与热能的相互转化是能量合理应用的重要途径。下列属于化学能与热能的转化过程的是
图片


转化过程
太阳能热水器烧水
燃油汽车行驶
选项
A
B
图片


转化过程
氯碱工业制氯气
水力发电
选项
C
D
A、A B、B C、C D、D -
15、下列我国古代的技术应用中,其工作原理不涉及化学反应的是


A.转轮排字
B.可燃冰作为能源


C.火药使用
D.铁的冶炼
A、A B、B C、C D、D -
16、
Ⅰ.阅读下面两段文字:
A.2019年1月3日,嫦娥四号探测器成功着陆在月球背面,嫦娥四号探测器主体部分使用钛合金①等新材料,太空舱中利用铁酸镍()②和其他物质转化呼出的二氧化碳③等废气。
B.2019年3月10日,我国长征三号乙运载火箭在西昌卫星发射中心成功发射。长征三号乙运载火箭的一子级上部是装有液氧④和四氧化二氮()⑤的氧化剂箱,下部是装有汽油⑥的燃料箱。
(1)上述短文标有序号的物质中,属于混合物的是(填序号,下同),属于单质的是 , 属于氧化物的是 , 主要成分属于有机物的是 , 属于盐的是。II.现有甲、乙、丙三名同学分别进行胶体的制备实验。
甲同学:向溶液中加入少量NaOH溶液。
乙同学:向25mL沸水中逐滴加入5~6滴饱和溶液,继续煮沸至液体呈红褐色,停止加热。
丙同学:直接加热饱和溶液。
试回答下列问题:
(2)上述操作中,(填序号)同学的能成功制得胶体。A.甲 B.乙 C.丙
(3)利用胶体的这一性质,可验证有胶体生成且操作最简便。写出生成胶体反应的化学方程式:。(4)可用如图所示的装置除去胶体中的杂质离子来提纯胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入稀硝酸酸化的溶液,若(填实验现象),则说明该胶体中的杂质离子已经完全除去。
-
17、宏观辨识与微观探析相结合是化学特有的认识物质的方法。NaCl溶于水的过程如图所示。下列说法正确的是
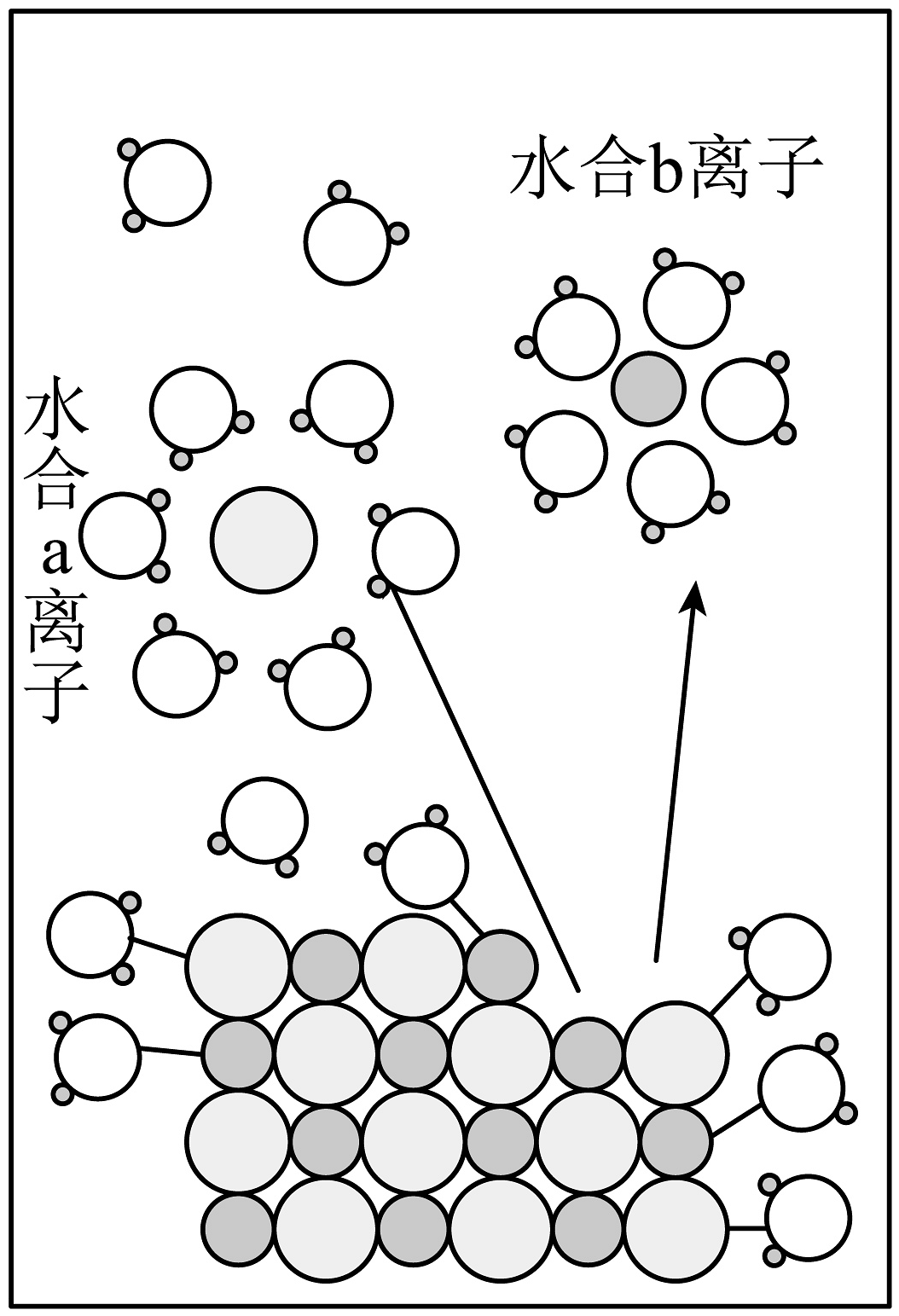 A、图中水合b离子为水合氯离子 B、NaCl溶液导电时,水合钠离子移向与电源负极相连的电极 C、固体NaCl溶于水前不能导电是因为无Na+和Cl- D、NaCl溶于水的电离过程为:NaClNa++Cl-
A、图中水合b离子为水合氯离子 B、NaCl溶液导电时,水合钠离子移向与电源负极相连的电极 C、固体NaCl溶于水前不能导电是因为无Na+和Cl- D、NaCl溶于水的电离过程为:NaClNa++Cl- -
18、化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 , 进一步处理得到产品和 , 实验流程如图:

回答下列问题:
(1)、从A~E中选择合适的仪器制备 , 正确的连接顺序是(按气流方向,用小写字母表示)。 (2)、B中使用雾化装置的优点是。(3)、生成的总反应的化学方程式为。(4)、反应完成后,将B中U形管内的混合物处理得到固体和滤液:
(2)、B中使用雾化装置的优点是。(3)、生成的总反应的化学方程式为。(4)、反应完成后,将B中U形管内的混合物处理得到固体和滤液:①对固体充分加热,产生的气体先通过足量浓硫酸,再通过足量 , 增重 , 则固体的质量为g。
②市场上销售的“苏打水"是一种非常受欢迎的饮用水,其溶质是小苏打。苏打水会因储藏温度过高而分解产生少量使口感发涩,写出一种除去中改善口感的方法(用离子方程式表示)。
③固体保存不当,会发生变质部分转化为 , 下列不能测定变质后的混合物中的质量分数的是。
a.取混合物与足量溶液充分反应,得到溶液
b.取混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到固体
c.取混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加
d.取混合物与足量溶液充分反应,过滤、洗涤、烘干,得固体
-
19、现有一定量含有杂质的试样,用下图的实验装置测定试样的纯度。(可供选用的反应物只有固体、盐酸、稀硫酸和蒸馏水)
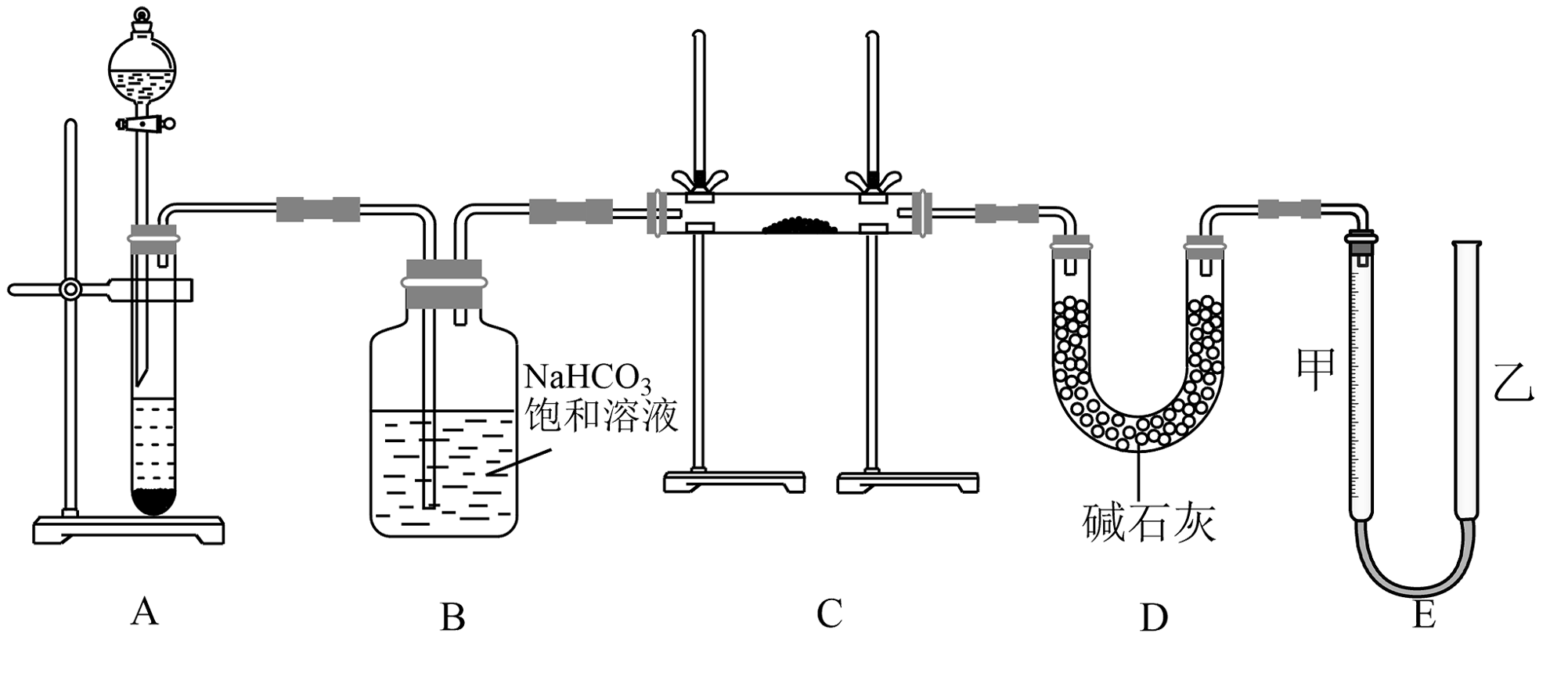
回答下列问题:
(1)、装置A中发生反应的离子方程式。(2)、装置D中碱石灰的作用是。(3)、若开始时测得样品的质量为 , 反应结束后测得气体体积为 , 该条件下此气体密度为。则试样的纯度为。(4)、为了较准确地用E装置测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数求其差值的过程中还应注意___________。A、读数时视线与凹液面最低处保持水平 B、反应结束即可立刻读数,以免氧气溶解到水中影响实验结果 C、实验开始和结束时都应上下移动乙管,使甲、乙两管液面相平再读数 D、实验结束读数时若甲管中液面高于乙管时,所测气体体积偏小(5)、a克下列物质在氧气中充分燃烧后的气体(、120℃)通过足量的充分反应后增重b克,符合的选项有___________。A、 B、 C、 D、 -
20、如图所示物质之间的转化,已知:A是金属单质,且焰色试验为黄色,X为常见温室气体。按要求回答下列问题:
 (1)、D的化学式:。(2)、A→B的离子方程式:。(3)、下列说法正确的是___________。A、氢氧化钙溶液和氯化钙溶液均可鉴别D、E两种溶液 B、若G是A在空气中加热生成的,则在一定条件下G能转化为B,但不能转化为D C、少量的A放置于敞口容器中最终可变成物质D D、将A投入到E的溶液中,也会有D生成(4)、D和E的固体混合物加热到质量不再变化时,剩余物质的质量为 , 则混合物中D的质量分数为(计算结果精确到0.1)。(5)、设计实验检验B中的阳离子。
(1)、D的化学式:。(2)、A→B的离子方程式:。(3)、下列说法正确的是___________。A、氢氧化钙溶液和氯化钙溶液均可鉴别D、E两种溶液 B、若G是A在空气中加热生成的,则在一定条件下G能转化为B,但不能转化为D C、少量的A放置于敞口容器中最终可变成物质D D、将A投入到E的溶液中,也会有D生成(4)、D和E的固体混合物加热到质量不再变化时,剩余物质的质量为 , 则混合物中D的质量分数为(计算结果精确到0.1)。(5)、设计实验检验B中的阳离子。